
Kaliumacetaat structuur, eigenschappen, gebruik, productie
De kaliumacetaat is een organische verbinding gevormd door een kalium-K-ion+ en een acetaation CH3COO-. De chemische formule is CH3COOK, of KCH3COO, of ook wel CtweeH.3KOtwee. Het is een kleurloze of witte kristallijne vaste stof, zeer oplosbaar in water..
Het wordt gebruikt om de zuurgraad van bepaalde industrieel bewerkte voedingsmiddelen te reguleren. Vanwege zijn grote affiniteit met water, wordt het in laboratoria of in bepaalde processen gebruikt om water te absorberen uit andere verbindingen, zoals om alcohol te dehydrateren..

Kaliumacetaat neemt deel aan sommige chemische reacties als versneller hiervan en aan de synthese van organische verbindingen. Het maakt het ook mogelijk om de vorming van antilichamen (natuurlijke stoffen die infecties bestrijden) te verhogen bij industriële methoden om ze te produceren..
Door zijn zeer lage temperatuureigenschappen is het een goede kandidaat voor gebruik in ijs-smeltende mengsels op betonwegen in zeer koude klimaten. Volgens geraadpleegde bronnen wordt het ook gebruikt in brandbestrijdingsmiddelen en in assemblages om cellen in microscopen te observeren..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Dichtheid
- 3.5 Oplosbaarheid
- 3,6 pH
- 3.7 Overige eigendommen
- 3.8 Gedrag bij opwarmen
- 4 Verkrijgen
- 5 toepassingen
- 5.1 In verschillende toepassingen
- 5.2 In de polymeerindustrie
- 5.3 In wetenschappelijke en medische onderzoekslaboratoria
- 5.4 Bij de industriële productie van antilichamen
- 5.5 In antivriesmengsels
- 5.6 Hoe het werkt als antivries
- 6 referenties
Structuur
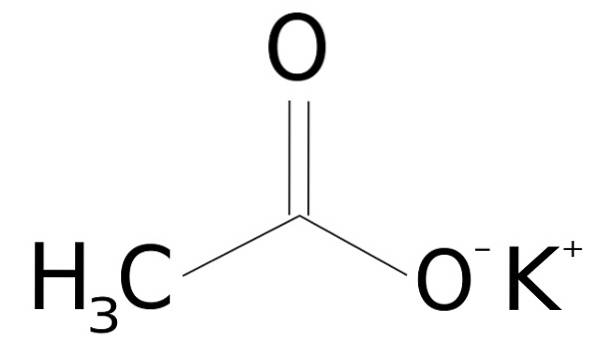
Kaliumacetaat bestaat uit een kalium K-kation+ en een acetaatanion CH3COO-. Dit laatste is de geconjugeerde base van azijnzuur CH3COOH. Het acetaat-ion CH3COO- bestaat uit een methyl-CH3 gehecht aan een carboxylaat-COO-.
De vereniging tussen beide ionen is elektrostatisch of ionisch, dat wil zeggen de vereniging tussen een positief en een negatief ion.
Nomenclatuur
- Kaliumacetaat
- Kaliumethanoaat
- Kaliumzout van azijnzuur
- AcOK
- KOAc
Eigendommen
Fysieke toestand
Kleurloze of witte kristallijne vaste stof.
Molecuulgewicht
98,14 g / mol
Smeltpunt
292 ºC
Dichtheid
1,6 g / cm3
Oplosbaarheid
Zeer oplosbaar in water: 256 g / 100 ml bij 20 ° C.
pH
Een 5% waterige oplossing van kaliumacetaat heeft een pH van 7,5-9,0.
Andere eigenschappen
Soms heeft het een vage azijngeur. In 10% -oplossing tast het geen aluminium aan bij kamertemperatuur, maar bij 60-70 ° C wordt het metaal donkerder en krijgt het putjes.
Bij concentraties van 20% of meer treedt oppervlakteaanslag op aluminium op bij elke temperatuur.
Kaliumacetaat (AcOK) is zeer goed oplosbaar in water. Het heeft een hydraat: KCH3COO.1,5HtweeOfwel, dat is de vaste stof die wordt verkregen door het te kristalliseren uit de waterige oplossingen van AcOK.
Gedrag bij verhitting
Als het gehydrateerde kaliumacetaat (AcOK) (KCH3COO.1,5HtweeO) wanneer het 40 ° C bereikt, begint het het hydratatiewater te verliezen.
KCH3COO.1,5HtweeO → KCH3COO + 1.5HtweeOf ↑
Als watervrij kaliumacetaat wordt verwarmd (zonder water: KCH3COO), begint het bij het bereiken van 340 ° C te ontbinden en vormt het kaliumcarbonaat KtweeCO3 volgens de volgende reactie:
2 KCH3COO + 4 Otwee → KtweeCO3 + 3 H.tweeO + 3 COtwee
Het verkrijgen van
Het kan worden bereid door de inwerking van kaliumhydroxide KOH op verschillende verbindingen, zoals azijnzuur CH3COOH, azijnzuuranhydride (CH3CO)tweeO en ammoniumacetaat CH3COONH4.
KOH + CH3COOH → CH3KOOK + HtweeOF
Het kan ook worden verkregen door kaliumcarbonaat K te laten reagerentweeCO3 of KHCO kaliumbicarbonaat3 met azijnzuur CH3COOH.
KHCO3 + CH3COOH → CH3KOOK + HtweeO + COtwee
Kaliumacetaat kan worden gekristalliseerd uit een waterige oplossing om een hoge zuiverheid te verkrijgen.
Toepassingen
In verschillende toepassingen
Kaliumacetaat wordt in de voedingsmiddelenindustrie gebruikt als zuurteregelaar. Het wordt gebruikt als droogmiddel in chemische methoden om de waterdampdoorlaatbaarheid van sommige weefsels te meten..
Het dient als een dehydratatiemiddel voor ethanol bij de productie van deze alcohol uitgaande van lignocellulose, een materiaal dat is afgeleid van hout..
Het wordt gebruikt om antibiotica te maken en wordt veel gebruikt in brandblusapparatuur.
In de polymeerindustrie
Het wordt gebruikt om polyurethanen te recyclen omdat het dient om de hydrolyse- en glycolysereacties van genoemde polymeren te katalyseren of te versnellen, zodat ze alcoholen en aminen worden..
Het wordt ook gebruikt bij de productie van organische siliconenharsen.
In wetenschappelijke en medische onderzoekslaboratoria
Zeer zuiver kaliumacetaat wordt in laboratoria gebruikt als reagens in de analytische chemie. Tevens om medisch-wetenschappelijk onderzoek uit te voeren.
In histopathologische laboratoria wordt het gebruikt om een neutraal pH-medium in microscoopopstellingen te garanderen..

Het wordt gebruikt voor de synthese van heterocyclische organische verbindingen, dit zijn verbindingen met cycli van verschillende grootte..
Bepaalde micro-elektroden die worden gebruikt om de elektrische eigenschappen van cellen te bestuderen, zijn gevuld met een geconcentreerde oplossing van kaliumacetaat..
Bij de industriële productie van antilichamen
Kaliumacetaat wordt gebruikt voor de grootschalige productie van monoklonale antilichamen (die afkomstig zijn van dezelfde stamcel) in celculturen. Maakt het mogelijk om de synthese of vorming van antilichamen te stimuleren.
Antilichamen zijn stoffen die door sommige cellen in het bloed worden aangemaakt om infecties door virussen of bacteriën te bestrijden..

In antivriesmengsels
Kaliumacetaat is gebruikt in antivriesmengsels. anti-ijsvorming) om ze te gebruiken om ijs op wegen en betonnen trottoirs te smelten en zo een veilig gebruik ervan mogelijk te maken.

De keuze van kaliumacetaat (AcOK) voor deze toepassing is te wijten aan het feit dat een 50 gew.% Waterige oplossing van AcOK eutectisch is en een smeltpunt van -62 ° C heeft. Dit betekent dat zelfs bij temperaturen tot -62 ° C de oplossing gesmolten blijft..
Een eutecticum is een homogeen mengsel van componenten met het laagste smeltpunt van alle mogelijke mengsels hiervan, inclusief dat van de zuivere componenten..
Hoe het werkt als antivries
Kaliumacetaat (AcOK) heeft een zeer goed vermogen om ijs te smelten.
Bij -5 ° C is het in staat om 11,5 kg ijs te smelten voor elke kg AcOK. Deze eigenschap neemt af naarmate de temperatuur daalt, maar zelfs bij -50 ° C heeft het de mogelijkheid om 1,3 kg ijs te smelten voor elke kg AcOH..
Bij -5 ° C is deze capaciteit vergelijkbaar met die van natriumchloride of keukenzout (NaCl), terwijl deze vanaf -30 ° C deze ruimschoots overschrijdt.

Bij de tests die met AcOK samen met andere verbindingen werden uitgevoerd, werd echter een zekere mate van corrosie van de cementoppervlakken waargenomen, dus werd overwogen om anticorrosieve middelen aan de antivriesmengsels toe te voegen..
Aan de andere kant is het mengsel van kaliumacetaat (CH3COOK) met kaliumformiaat (HCOOK) is een uitstekende antivries en vereist geen anticorrosief.
Referenties
- Baker, F.J. et al. (1976). Kleuringsprocedures. Waterige bergingsmiddelen. In Inleiding tot medische laboratoriumtechnologie (vijfde editie). Opgehaald van sciencedirect.com.
- Hassan, A.A. et al. (2018). Indazolen: synthese en bindingvormende heterocyclisatie. In Advances in heterocyclische chemie. Opgehaald van sciencedirect.com.
- ONS. Nationale bibliotheek van geneeskunde. (2019). Kaliumacetaat. Opgehaald van pubchem.ncbi.nlm.nih.gov.
- Das, A. en Alagirusamy, R. (2010). Vochtoverdracht. Droogmiddel omgekeerde beker-methode. In Science in Clothing Comfort. Opgehaald van sciencedirect.com.
- Vargel, C. (2004). Carboxilzuur en hun derivaten. Acetaten. In corrosie van aluminium. Opgehaald van sciencedirect.com.
- Cuevas, J. (2014). Elektrofysiologische opnametechnieken. Intracellulaire opnametechnieken. In referentiemodule in biomedische wetenschappen. Opgehaald van sciencedirect.com.
- Fink, J.K. (2018). Poly (urethaan) s. Recycling. Solvolysis. In Reactive Polymers: Fundamentals and Applications (Third Edition). Opgehaald van sciencedirect.com.
- Fong, W. et al. (1997). Optimalisatie van de productie van monoklonale antilichamen: gecombineerde effecten van kaliumacetaat en perfusie in een geroerde tankbioreactor. Cytotechnology 24: 47-54. Opgehaald van link.springer.com.
- Danilov, V.P. et al. (2012). Reagentia tegen ijsvorming bij lage temperatuur in waterige zoutsystemen die acetaten en formiaten bevatten. Theoretische grondslagen van chemische technologie, 2012, deel 46, nr. 5, blz. 528-535. Opgehaald van link.springer.com.
- Fakeev, A.A. et al. (2012). Onderzoek en ontwikkeling van methoden voor kaliumacetaat van hoge zuiverheid. Journal of Applied Chemistry, 2012, deel 85, nr. 12, blz. 1807-1813. Opgehaald van link.springer.com.



Niemand heeft nog op dit artikel gereageerd.