
Butino structuur, eigenschappen en toepassingen

De butino is een chemische verbinding die behoort tot de groep van alkynen, die voornamelijk wordt gekenmerkt door ten minste één drievoudige binding tussen twee koolstofatomen in zijn structuur.
Als het gaat om het vaststellen van regels voor de naamgeving van alkynen, heeft de IUPAC (International Union of Pure and Applied Chemistry) vastgesteld dat dezelfde regels worden gehanteerd als voor alkenen..

Het fundamentele verschil tussen de nomenclatuur van beide soorten stoffen is dat het achtervoegsel -eno wordt gewijzigd in -ino als het gaat om verbindingen met drievoudige bindingen in hun structuur..
Aan de andere kant bestaat butyn uitsluitend uit koolstof en waterstof en komt het in twee vormen voor: 1-butyn, dat zich in de gasfase bevindt onder standaard druk- en temperatuuromstandigheden (1 atm, 25 ° C); en 2-butyn, een soort in vloeibare fase geproduceerd door chemische synthese.
Artikel index
- 1 Chemische structuur
- 1.1 1-butyn
- 1.2 2-butyn
- 2 Eigenschappen
- 3 toepassingen
- 4 referenties
Chemische structuur
In het molecuul dat bekend staat als butyn, treedt het fenomeen van structurele positie-isomerie op, dat bestaat uit de aanwezigheid van dezelfde functionele groepen in beide verbindingen, maar die elk op een andere plaats in de keten worden aangetroffen..
In dit geval hebben beide vormen van butyn een identieke molecuulformule; in 1-butyn bevindt de drievoudige binding zich echter op koolstof nummer één, terwijl deze zich in 2-butyn op nummer twee bevindt. Dit zet ze om in positionele isomeren.
Vanwege de locatie van de drievoudige binding in een van de terminals van de 1-butynstructuur, wordt het beschouwd als een terminaal alkyn, terwijl de tussenpositie van de drievoudige binding in de 2-butynstructuur het de classificatie van interne alkyn geeft..
De binding kan dus alleen zijn tussen de eerste en tweede koolstof (1-butyn) of tussen de tweede en derde koolstof (2-butyn). Dit komt door de toegepaste nomenclatuur, waarbij de laagst mogelijke nummering altijd zal worden gegeven aan de positie van de drievoudige binding..
1-butyn
De verbinding genaamd 1-butyn staat ook bekend als ethylacetyleen, vanwege de structuur en de manier waarop de vier koolstofatomen zijn gerangschikt en gebonden. Echter, als we het hebben over butino alleen naar deze chemische soort wordt verwezen.
In dit molecuul bevindt de drievoudige binding zich aan een terminaal koolstofatoom, waardoor de beschikbaarheid van waterstofatomen mogelijk is die het een grote reactiviteit geven.
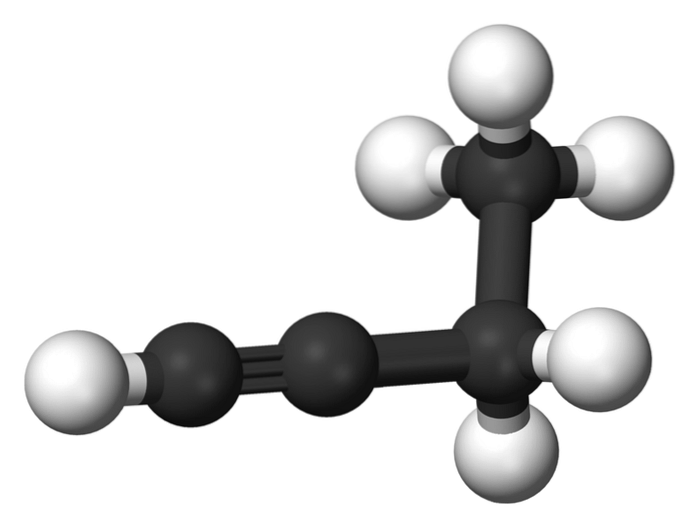
Deze stijve en sterkere binding dan een enkele of dubbele binding tussen de koolstofatomen zorgt voor een stabiele configuratie van lineaire geometrie tot 1-butyn..
Aan de andere kant is deze gasvormige stof vrij ontvlambaar, dus in aanwezigheid van hitte kan het gemakkelijk brand of explosies veroorzaken en heeft het een grote reactiviteit in aanwezigheid van lucht of water..
2-butyn
Omdat interne alkynen een grotere stabiliteit vertonen dan terminale alkynen, maken ze de omzetting van 1-butyn in 2-butyn mogelijk.
Deze isomerisatie kan plaatsvinden door 1-butyn te verhitten in aanwezigheid van een base (zoals NaOH, KOH, NaOCH3 ...) of door omlegging van 1-butyn in een oplossing van kaliumhydroxide (KOH) in ethanol (CtweeH.6OF).
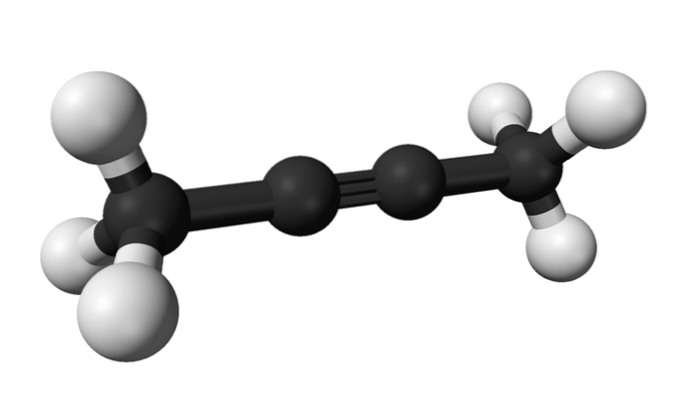
Op dezelfde manier wordt de chemische stof die bekend staat als 2-butyn ook wel dimethylacetyleen (of crotonyleen) genoemd, en presenteert zichzelf als een vloeibare en vluchtige soort die kunstmatig ontstaat..
In 2-butyn bevindt de drievoudige binding zich in het midden van het molecuul, waardoor het een grotere stabiliteit heeft dan zijn isomeer.
Bovendien heeft deze kleurloze verbinding een lagere dichtheid dan water, hoewel het als onoplosbaar wordt beschouwd en een hoge ontvlambaarheid heeft..
Eigendommen
-De structuurformule van butyn (ongeacht naar welke isomeer wordt verwezen) is C4H.6, die een lineaire structuur heeft.
-Een van de chemische reacties die het butyn-molecuul ondergaat, is isomerisatie, waarbij een herschikking en migratie van de drievoudige binding plaatsvindt binnen het molecuul..
-1-butyn bevindt zich in de gasfase, heeft een zeer hoge ontvlambaarheid en een hogere dichtheid dan lucht.
-Deze stof is ook behoorlijk reactief en kan in aanwezigheid van hitte heftige explosies veroorzaken..
-Wanneer dit kleurloze gas een onvolledige verbrandingsreactie ondergaat, kan het bovendien koolmonoxide (CO) veroorzaken.
-Wanneer beide isomeren aan hoge temperaturen worden blootgesteld, kunnen ze explosieve polymerisatiereacties ondergaan..
-2-Butyne bevindt zich in de vloeistoffase, hoewel het ook als vrij ontvlambaar wordt beschouwd onder standaardomstandigheden van druk en temperatuur..
-Deze stoffen kunnen heftige reacties ondergaan wanneer ze zich in aanwezigheid van sterk oxiderende stoffen bevinden..
-Op dezelfde manier treden exotherme reacties op met als gevolg het vrijkomen van waterstofgas wanneer ze zich in de aanwezigheid van reducerende soorten bevinden..
-Bij contact met bepaalde katalysatoren (zoals sommige zure stoffen) of initiërende soorten, kunnen exotherme polymerisatiereacties optreden.
Toepassingen
Omdat ze verschillende eigenschappen hebben, kunnen beide isomeren verschillende toepassingen en toepassingen hebben, zoals hieronder wordt weergegeven:
In de eerste plaats is een van de toepassingen van 1-butyn vaak het gebruik ervan als tussenstap in het productieproces van andere stoffen van organische aard van synthetische oorsprong..
Aan de andere kant wordt deze chemische soort gebruikt in de rubberverwerkende industrie en afgeleide verbindingen; zoals bijvoorbeeld wanneer u benzol wilt verkrijgen.
Op een vergelijkbare manier wordt het gebruikt bij het fabricageproces van een grote verscheidenheid aan plastic producten, maar ook bij de vervaardiging van veel polyethyleensubstanties die met een hoge dichtheid worden beschouwd..
Ook wordt 1-butyn vaak gebruikt als component voor de snij- en lasprocessen van sommige metaallegeringen, waaronder staal (ijzer-koolstof legering)..
In een andere zin wordt het 2-butyn-isomeer gebruikt in combinatie met een ander alkyn, propyn genaamd, bij de synthese van sommige stoffen die bekend staan als gealkyleerde hydrochinonen, wanneer het totale syntheseproces van α-tocoferol (vitamine E) wordt uitgevoerd..
Referenties
- Wikipedia. (s.f.). Butyne. Opgehaald van en.wikipedia.org
- Yoder, C. H., Leber P. A. en Thomsen, M. W. (2010). The Bridge to Organic Chemistry: Concepts and Nomenclature. Opgehaald van books.google.co.ve
- Study.com. (s.f.). Butyne: Structurele formule en isomeren. Opgehaald uit studie.
- PubChem. (s.f.). 1-Butyne. Opgehaald van pubchem.ncbi.nlm.nih.gov
- PubChem. (s.f.). 2-Butyne. Opgehaald van pubchem.ncbi.nlm.nih.gov



Niemand heeft nog op dit artikel gereageerd.