
Boterzuurformule, eigenschappen, risico's en toepassingen

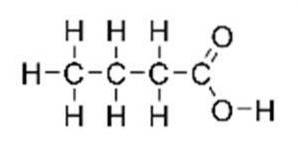
De boterzuur, ook wel n-butaanzuur genoemd (in het IUPAC-systeem), het is een carbonzuur met de structuurformule CH3CH2CH2-COOH. Het is geclassificeerd als een vetzuur met een korte keten. Het heeft een onaangename geur, een scherpe smaak en tegelijkertijd ietwat zoet (vergelijkbaar met ether). De structuur is geïllustreerd in figuur 1.
Het wordt vooral aangetroffen in ranzig boter, Parmezaanse kaas, rauwe melk, dierlijke vetten, plantaardige oliën en braaksel. De naam is afgeleid van het Griekse woord βουτυρος, wat "boter" betekent (medewerkers, 2016).
Boterzuur wordt gevormd in de menselijke dikke darm door bacteriële fermentatie van koolhydraten (inclusief voedingsvezels) en onderdrukt zogenaamd colorectale kanker.
Boterzuur is een vetzuur dat in de vorm van esters voorkomt in dierlijke vetten en plantaardige oliën. Interessant is dat esters van boterzuur met een laag molecuulgewicht, zoals methylbutyraat, meestal aangename aroma's of smaken hebben (het metabolomische inovatiecentrum, S.F.).
Artikel index
- 1 Fysische en chemische eigenschappen van boterzuur
- 2 Reactiviteit en gevaren
- 3 Gebruik en gezondheidsvoordelen
- 4 referenties
Fysische en chemische eigenschappen van boterzuur
Boterzuur is een kleurloze vloeistof met een onaangename, ranzig botergeur. Het heeft ook een zekere boterachtige smaak.
Het heeft een molecuulgewicht van 88,11 g / mol en een dichtheid van 0,9528 g / ml bij kamertemperatuur. Het smeltpunt is -5,1 ° C en het kookpunt is 163,75 ° C.
De verbinding is oplosbaar in water, ethanol en ether. Het is enigszins oplosbaar in tetrachloorkoolstof. Het is een zwak zuur, wat betekent dat het niet volledig dissocieert, de pKa is 4,82 (National Center for Biotechnology Information, S.F.).
Een isomeer, 2-methylpropaanzuur (isoboterzuur), (CH3) 2CHCO2H, wordt zowel in de vrije toestand als in zijn ethylester in enkele plantaardige oliën aangetroffen. Hoewel het commercieel minder belangrijk is dan boterzuur (Brown, 2011).
Boterzuur kan reageren met oxidatiemiddelen. Gloeilampreacties treden op met chroomtrioxide boven 100 ° C. Ze zijn ook onverenigbaar met basen en reductiemiddelen. Kan aluminium en andere lichte metalen aantasten (BUTYRIC ACID, 2016).
Reactiviteit en gevaren
Boterzuur wordt als een ontvlambare verbinding beschouwd. Onverenigbaar met sterke oxidatiemiddelen, aluminium en de meeste andere veel voorkomende metalen, alkaliën, reductiemiddelen (Royal Society of Chemistry, 2015).
De verbinding is zeer gevaarlijk in geval van huidcontact (kan brandwonden veroorzaken), in geval van inslikken, oogcontact (irriterend) en inademing (kan ernstige irritatie van de luchtwegen veroorzaken).
De vloeistof of nevel uit de aerosol kan weefselschade veroorzaken, vooral in de slijmvliezen van de ogen, mond en luchtwegen..
De stof is giftig voor de longen, het zenuwstelsel en de slijmvliezen. Herhaalde of langdurige blootstelling aan de stof kan zowel schade aan deze organen als irritatie van de luchtwegen veroorzaken, wat kan leiden tot frequente aanvallen van bronchiale infectie (Material Safety Data Sheet Boterzuur, 2013).
In geval van contact met de ogen, moet het slachtoffer worden gecontroleerd op contactlenzen en worden verwijderd. De ogen van het slachtoffer moeten gedurende 20 tot 30 minuten met water of een normale zoutoplossing worden gespoeld en tegelijkertijd een ziekenhuis bellen.
In geval van contact met de huid, moet het getroffen gebied worden ondergedompeld in water terwijl alle besmette kleding wordt verwijderd en geïsoleerd. Alle aangetaste huidgebieden worden voorzichtig gewassen met water en zeep. Er moet medische hulp worden ingeroepen.
Bij inademing de besmette ruimte op een koele plaats achterlaten. Raadpleeg een arts als zich symptomen voordoen (zoals piepende ademhaling, hoesten, kortademigheid of brandend gevoel in de mond, keel of borst)..
Bij inslikken mag braken niet worden opgewekt. Als het slachtoffer bij bewustzijn is en geen aanvallen heeft, moet 1 of 2 glazen water worden gegeven om de chemische stof te verdunnen en een ziekenhuis of antigifcentrum bellen..
Als het slachtoffer stuiptrekkingen heeft of bewusteloos is, geef dan niets via de mond, zorg ervoor dat de luchtweg van het slachtoffer open is en plaats het slachtoffer op zijn zij met het hoofd lager dan het lichaam. Roep onmiddellijk medische hulp in.
Gebruik en gezondheidsvoordelen
Esters van boterzuur met een laag molecuulgewicht, zoals methylbutyraat, hebben in het algemeen een aangename geur en smaak. Hierdoor worden ze gebruikt als voedings- en parfumadditieven..
Butyraat, de geconjugeerde base van boterzuur, komt van nature voor in veel voedingsmiddelen. Het kan ook als supplement of smaakstof in andere worden toegevoegd.
Boterzuuresters of butyraten worden gebruikt om kunstmatige smaakstoffen en essences van plantaardige olie te maken. Amylbutyraat is een hoofdingrediënt in abrikozenolie, terwijl methylbutyraat in ananasolie voorkomt..
Ananasolie wordt niet alleen gebruikt als smaakstof, maar wordt ook gebruikt om botgroei te bevorderen, tandheelkundige ingrepen te genezen en verkoudheid, keelpijn en acute sinusitis te behandelen, volgens de fabrikant van natuurlijke producten OCA Brasil (PULUGURTHA, 2015).
Bacteriën die in het maagdarmkanaal worden aangetroffen, kunnen aanzienlijke hoeveelheden fermenterend butyraat, voedingsvezels en onverteerbare koolhydraten produceren. Het eten van vezelrijk voedsel zoals gerst, havermout, bruine rijst en zemelen is een gezonde manier om butyraat in je lichaam te krijgen..
Een studie gepubliceerd in het novembernummer van het "Journal of Nutrition" geeft aan dat een avondmaaltijd van granen die rijk is aan onverteerbare koolhydraten, de butyraatconcentratie in het plasma de volgende ochtend kan verhogen..
Hij voegt eraan toe dat dit het mechanisme zou kunnen zijn waarmee de volkorengranen diabetes en hartaandoeningen helpen voorkomen..
Boterzuur, als butyraat, wordt in de menselijke dikke darm gevormd als een product van vezelgisting, en dit wordt gesuggereerd als een factor die verklaart waarom vezelrijke diëten beschermend zijn bij het voorkomen van darmkanker..
Er zijn verschillende hypothesen onderzocht over het mogelijke mechanisme van deze relatie, inclusief of butyraat belangrijk is voor het handhaven van normale fenotypische expressie van epitheelcellen, of voor het verbeteren van de eliminatie van beschadigde cellen door apoptose..
Andere voordelen van boterzuur of butyraat zijn:
- Helpt bij het afvallen.
- Verlicht geïrriteerd karteldarmsyndroom (Andrzej Załęski, 2013).
- Behandeling van de ziekte van Crohn (Axe, S.F.).
- Bestrijd insulineresistentie.
- Heeft ontstekingsremmende effecten.
Referenties
- Andrzej Załęski, A. B. (2013). Boterzuur bij prikkelbare darmsyndroom. Przegla̜d Gastroenterologiczny, 350-353. Opgehaald van ncbi.nlm.nih.gov.
- Axe, J. (S.F.). Wat is boterzuur? 6 Voordelen van boterzuur die u moet kennen. Hersteld van draxe: draxe.com.
- Brown, W. H. (2011, 2 december). Boterzuur (CH3CH2CH2CO2H). Opgehaald uit encyclopedia britannica: Hersteld van britannica.com.
- BUTYRIC ZUUR. (2016). Hersteld van cameochemicaliën: cameochemicals.noaa.gov.
- medewerkers, N. W. (2016, 22 december). Boterzuur. Opgehaald uit New World Encyclopedia: Hersteld van newworldencyclopedia.org.
- Veiligheidsinformatieblad Boterzuur. (2013, 21 mei). Opgehaald van sciencelab: sciencelab.com.
- Nationaal centrum voor informatie over biotechnologie. (S.F.). PubChem samengestelde database; CID = 264. Opgehaald van PubChem: ncbi.nlm.nih.gov.
- PULUGURTHA, S. (2015, 1 juni). Welke voedingsmiddelen bevatten veel butyraat? Opgehaald van livestrong: livestrong.com.
- Royal Society of Chemistry. (2015). Butaanzuur. Opgehaald van chemspider: chemspider.com.
- het metabolomische innovatiecentrum. (S.F.). Menselijke metaboloomdatabase Met metabocard voor boterzuur. Opgehaald van hmdb.ca: hmdb.ca.



Niemand heeft nog op dit artikel gereageerd.