
Sulfonzuurstructuur, nomenclatuur, eigenschappen, gebruik

Het heet sulfonzuur elke verbinding die behoort tot een familie van organische zuren die een of meer -SO-groepen hebben3H. Bepaalde auteurs geven aan dat de moederverbinding H-S (= O) istwee-OH of H-SO3H, ook wel "sulfonzuur" genoemd, zijn bestaan is echter niet bewezen, noch dat van zijn tautomeer HO-S (= O) -OH, bekend als "zwaveligzuur" (HtweeSW3), noch in oplossing, noch in vaste toestand.
Dit laatste is te wijten aan het feit dat zwaveldioxidegas (IV) (SOtwee) in waterige oplossing wordt omgezet in bisulfietionen (HSO3-) en pyrosulfiet (S.tweeOF5twee-) en niet H-S (= O)twee-OH noch tegen HO-S (= O) -OH, wat al door veel scheikundigen is geverifieerd.
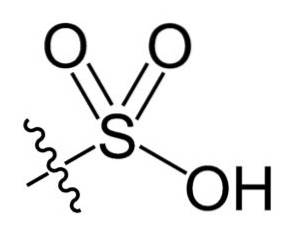
In de chemische formule R-SO3H van sulfonzuren, kan de groep R koolwaterstofskeletten vertegenwoordigen, zoals alkaan, alkeen, alkyn en / of areen. Deze kunnen onder meer secundaire functionaliteiten bevatten, zoals ester-, ether-, keton-, amino-, amido-, hydroxyl-, carboxyl- en fenolgroepen..
Sulfonzuren zijn sterke zuren, vergelijkbaar met zwavelzuur (H.tweeSW4De rest van zijn eigenschappen hangt echter grotendeels af van de aard van de R-groep..
Sommige hebben de neiging om bij hoge temperaturen te desulfoneren. Dit betekent het verlies van de -SO-groep3H, vooral als R een areen is, dat wil zeggen met een benzeenring.
Sulfonzuren hebben veel toepassingen, afhankelijk van hun chemische formule. Ze worden gebruikt om kleurstoffen, inkten, polymeren, detergenten, oppervlakteactieve stoffen en als katalysatoren te maken, naast vele andere toepassingen..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 4 Verkrijgen
- 4.1 Arylsulfonzuren
- 4.2 Alkylsulfonzuren
- 5 toepassingen
- 5.1 Sulfonzuren voor oppervlakteactieve stoffen en detergentia
- 5.2 Kleurstoffen op basis van sulfonzuren
- 5.3 Amiden op basis van sulfonzuren
- 5.4 Gefluoreerde en chloorfluor sulfonzuren
- 5.5 Bij biologische toepassingen
- 5.6 In de olie-industrie
- 5.7 Bij de formulering van smeermiddelen en corrosiewerende middelen
- 6 referenties
Structuur
Sulfonzuren hebben de volgende algemene structuur:
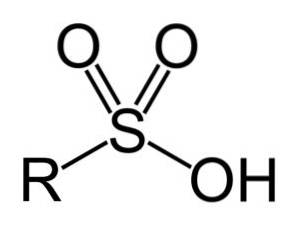
Nomenclatuur
- Sulfonylgroep: -SO3H.
- Alkyl- of arylsulfonzuur: R-SO3H.
Eigendommen
Ze zijn vast of vloeibaar, afhankelijk van de groep R. Gasvormige sulfonzuren zijn niet bekend.
Hun fysische en chemische eigenschappen hangen af van de aard van de groep R. Ter vergelijking worden enkele fysische eigenschappen van verschillende sulfonzuren weergegeven, waarbij smp. is het smeltpunt en b.v. is het kookpunt bij een druk van 1 mm Hg:
- Methaansulfonzuur: smp. 20 ° C; bijv. 122 ºC
- Ethaansulfonzuur: smp. -17 ° C; bijv. 123 ºC
- Propaansulfonzuur: smp. -37 ° C; bijv. 159 ºC
- Butaansulfonzuur: smp. -15 ° C; bijv. 149 ºC
- Pentaansulfonzuur: smp. -16 ° C; bijv. 163 ºC
- Hexaansulfonzuur: smp. 16 ° C; bijv. 174 ºC
- Benzeensulfonzuur: smp. 44 ° C; bijv. 172 ºC (bij 0,1 mm Hg)
- P-tolueensulfonzuur: smp. 106 ° C; bijv. 182 ºC (bij 0,1 mm Hg)
- 1-naftaleensulfonzuur: smp. 78 ° C; bijv. Het valt uiteen
- 2-naftaleensulfonzuur: smp. 91 ° C; bijv. Het valt uiteen
- Trifluormethaansulfonzuur: smp. geen; bijv. 162 ºC (bij 760 mm Hg)
De meeste zijn zeer oplosbaar in water.
Sulfonzuren zijn zelfs zuurder dan carbonzuren. Ze hebben een zuurgraad die vergelijkbaar is met die van zwavelzuur. Oplossen in waterig natriumhydroxide en waterig bicarbonaat.
Ze hebben de neiging om thermische ontleding te ondergaan, waardoor ze desulfoneren. Verschillende van de alkaansulfonzuren zijn echter thermisch stabiel. Met name triflzuur of trifluormethaansulfonzuur is een van de sterkste en meest stabiele zuren.
Het verkrijgen van
Arylsulfonzuren
Arylsulfonzuren worden over het algemeen verkregen door het sulfoneringsproces dat bestaat uit het toevoegen van een overmaat rokend zwavelzuur (HtweeSW4 + SW3) naar de organische verbinding die we willen sulfoneren. Bijvoorbeeld in het geval van benzeen:
C6H.6 + H.tweeSW4 <-> C6H.5SW3H + HtweeOF
ArH + HtweeSW4 <-> ArSO3H + HtweeOF
Sulfonering is een omkeerbare reactie, want als we verdund zuur aan benzeensulfonzuur toevoegen en stoom over het mengsel leiden, ontstaat de SO-eliminatiereactie.3 en het benzeen wordt gedestilleerd door verdamping met stoom, waardoor het evenwicht verschuift naar desulfonatie.
Het sulfoneringsmiddel kan ook chloorzwavelzuur, sulfaminezuur of sulfietionen zijn..
Alkylsulfonzuren
Deze worden in het algemeen bereid door sulfo-oxidatie, dat wil zeggen behandeling van alkylverbindingen met zwaveldioxide SOtwee en zuurstof Otwee, of direct met zwaveltrioxide SO3.
RH + 2SOtwee + OFtwee + H.tweeOF <--> R-SO3H + HtweeSW4
Toepassingen
Sulfonzuren voor oppervlakteactieve stoffen en detergentia
Alkylbenzeensulfonzuren worden gebruikt bij de vervaardiging van detergentia, wat een van de meest voorkomende toepassingen is.
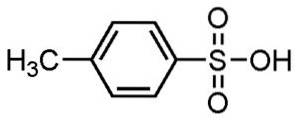
Gebruikt voor waspoeder en vloeibare wasmiddelen, lichte of zware wasmiddelen, handzepen en shampoo.
De actieve componenten zijn in het algemeen lineaire alkylbenzeensulfonaten en gesulfoneerde vetesters..
Gebruikelijke oppervlakteactieve stoffen zijn alfa-olefinesulfonaten, sulfobetaïnen, sulfosuccinaten en alkyldifenylethers-disulfonaten, die allemaal zijn afgeleid van sulfonzuren..
Deze oppervlakteactieve stoffen worden gebruikt in huishoudelijke schoonmaakproducten, cosmetica, emulsiepolymerisatie en fabricage van landbouwchemicaliën..
Lignosulfonaten zijn gesulfoneerde derivaten van lignine, een bestanddeel van hout, en worden gebruikt als dispergeermiddelen, bevochtigingsmiddelen, bindmiddelen in wegverhardingen, betonmengsels en additieven in diervoeder..
Een derivaat van 2-naftaleensulfonzuur wordt gebruikt om de vloeibaarheid en sterkte van cement te vergroten..
Kleurstoffen op basis van sulfonzuur
Deze worden over het algemeen gekenmerkt doordat ze azogroepen bevatten (R-N = N-R).
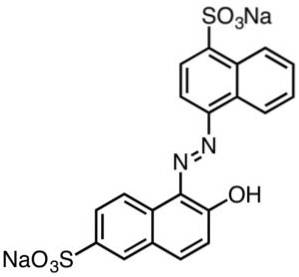
Kleurstoffen afgeleid van sulfonzuren zijn nuttig in de papierindustrie, inkten zoals inkjetprinten, textiel zoals katoen en wol, cosmetica, zeep, wasmiddelen, voedsel en leer..
Een derivaat van 2-naftaleensulfonzuur wordt ook gebruikt als ingrediënt in kleurstoffen voor polyestervezels en voor het looien van leer..
Amiden op basis van sulfonzuur
Acrylamidosulfonzuren vallen op in deze toepassing, die worden gebruikt in polymeren, in elektrodepositie van metalen, als oppervlakteactieve stoffen en in transparante anticondens-coatings..
Ze worden ook gebruikt bij verbeterde olieterugwinning, als vuilafstotende middelen, in hydraulische cementmengsels en als versnellers voor het uitharden van aminoplasthars..
Sommige sulfonamiden worden ook gebruikt in formules voor insecticiden.
Gefluoreerde en chloorfluor sulfonzuren
In deze groep trifluormethaansulfonzuur (CF3SW3H), ook wel triflzuur genoemd. Deze verbinding heeft toepassing in organische synthese en katalyse van polymerisatiereacties.
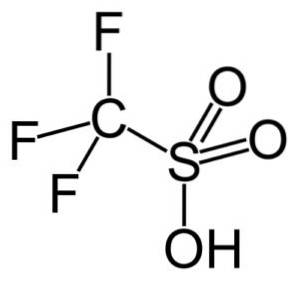
Het wordt bijvoorbeeld gebruikt bij de polymerisatie van aromatische olefinen en bij de bereiding van sterk vertakte paraffinische koolwaterstoffen met een hoog octaangetal voor gebruik als brandstofadditieven..
Een andere toepassing is bij de synthese van geleidende polymeren, door het doteren van polyacetyleen, waarbij bijvoorbeeld halfgeleiders worden geproduceerd. p.
Pentafluorethaansulfonzuur (CF3CFtweeSW3H), bekend als pentafilic acid, wordt gebruikt als organische katalysator.
Triflzuur reageert met antimoonpentafluoride (SbF5) het genereren van het zogenaamde "Magic Acid", een superzure katalysator die dient voor alkylering en polymerisatie.
Nafion-H is een ionenuitwisselingshars van een geperfluoreerd polymeer sulfonzuur. Het heeft de eigenschap inert te zijn voor sterke zuren, sterke basen en reducerende of oxiderende middelen..
In biologische toepassingen
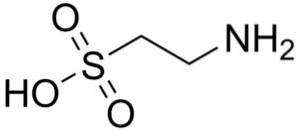
Een van de weinige sulfonzuren die in de natuur worden aangetroffen, is 2-aminoethaansulfonzuur, beter bekend als taurine, een essentieel aminozuur met name voor katten.
Synthetische en natuurlijke taurine worden gebruikt als supplementen in voer voor huisdieren en in farmaceutische producten..
Taurocholzuur is een bestanddeel van gal en neemt deel aan de vertering van vetten. 8-Anilino-1-naftaleensulfonzuur, een synthetische verbinding, wordt gebruikt bij de studie van eiwitten.
Copolymeren van ureum en bifenyldisulfonzuur zijn gebruikt als remmers van het herpes simplex-virus.
Sommige derivaten van sulfonzuren, zoals gesulfoneerd polystyreen en sommige azoverbindingen, hebben remmende eigenschappen van het humaan immunodeficiëntievirus of HIV vertoond, zonder overmatig toxisch te zijn voor gastheercellen..
In de olie-industrie
Bepaalde mengsels van aardoliederivaten, die een gevarieerde combinatie van aromaten, paraffinen en polynucleaire aromaten bevatten, kunnen worden gesulfoneerd en vervolgens op de juiste wijze worden geneutraliseerd onder vorming van zogenaamde petroleumsulfonaten..
Deze petroleumsulfonaten hebben de eigenschap de oppervlaktespanning van petroleum in water te verlagen. Bovendien is de productie ervan erg goedkoop.
Om deze reden worden petroleumsulfonaten in bestaande oliebronnen geïnjecteerd, wat helpt bij het terugwinnen van ruwe olie die vastzit tussen rotsen onder het oppervlak..
Bij de formulering van smeermiddelen en anticorrosiva
Magnesiumsulfonaten worden veel gebruikt in smeermiddelsamenstellingen als wasmiddel-dispergerende additieven en om slijtage te voorkomen..
Bariumsulfonaten worden gebruikt in smeermiddelen voor wentellagers die worden gebruikt in toepassingen met hoge snelheid. Natrium- en calciumsulfonaten worden toegepast in tandwielsmeermiddelen en -vetten om de eigenschappen bij extreme druk te verbeteren.
Magnesiumzouten van sulfonzuren zijn ook bruikbaar in corrosiewerende toepassingen zoals coatings, vetten en harsen..
Referenties
- Falk, Michael en Giguere, Paul A. (1958). Over de aard van zwavelig zuur. Canadian Journal of Chemistry, deel 36, 1958. Opgehaald van nrcresearchpress.com
- Betts, R.H. en Voss, R.H. (1970). De kinetiek van zuurstofuitwisseling tussen het sulfietion en water. Canadian Journal of Chemistry, deel 48, 1970. Opgehaald van nrcresearchpress.com
- Cotton, F.A. en Wilkinson, G. (1980). Geavanceerde anorganische chemie. Vierde druk. Hoofdstuk 16. John Wiley & Sons.
- Kirk-Othmer (1994). Encyclopedie van chemische technologie. Deel 23. Vierde editie. John Wiley & Sons.
- Kosswig, Kurt. (2012). Oppervlakteactieve stoffen. Ullmann's Encyclopedia of Industrial Chemistry, deel 35. Wiley-VCH Verlag GmbH & Co.



Niemand heeft nog op dit artikel gereageerd.