
Calciumhydroxide (Ca (OH) 2) structuur, eigenschappen, productie, gebruik

De calcium hydroxide is een anorganische verbinding waarvan de chemische formule Ca (OH) istwee. Het is een wit poeder dat al duizenden jaren in gebruik is en gedurende die tijd verschillende traditionele namen of bijnamen heeft verdiend; onder hen kunnen we gebluste, dode, chemische, gehydrateerde of fijne kalk noemen.
In de natuur is het verkrijgbaar in een zeldzaam mineraal genaamd portlandiet, van dezelfde kleur. Hierdoor Ca (OH)twee Het wordt niet rechtstreeks uit dit mineraal verkregen, maar uit een warmtebehandeling, gevolgd door hydratatie, van de kalksteen. Hieruit wordt kalk, CaO, verkregen, dat later wordt geblust of gehydrateerd om Ca (OH) te producerentwee.

Ca (OH)twee het is een relatief zwakke basis in water, omdat het nauwelijks kan oplossen in heet water; maar zijn oplosbaarheid neemt toe in koud water, omdat zijn hydratatie exotherm is. De basiciteit ervan blijft echter een reden om er voorzichtig mee te zijn tijdens het hanteren, aangezien het brandwonden kan veroorzaken aan elk deel van het lichaam..
Het is gebruikt als pH-regulator voor verschillende materialen of voedingsmiddelen, maar ook als een goede bron van calcium met betrekking tot zijn massa. Het heeft toepassingen in de papierindustrie, bij de desinfectie van rioolwater, in ontharingsproducten, in voedingsmiddelen gemaakt van maïsmeel.
Het belangrijkste gebruik ervan is echter als constructiemateriaal geweest, aangezien kalk hydrateert wanneer het wordt gemengd met de andere ingrediënten in gips of mortel. In deze geharde mengsels, Ca (OH)twee absorbeert kooldioxide uit de lucht om zandkristallen te consolideren samen met die gevormd uit calciumcarbonaat.
Momenteel wordt er nog steeds onderzoek gedaan met als doel betere constructiematerialen te ontwikkelen die Ca (OH)twee direct in zijn samenstelling als nanodeeltjes.
Artikel index
- 1 Structuur
- 1.1 Kristal en zijn ionen
- 1.2 Morfologie
- 2 Eigenschappen
- 2.1 Fysiek uiterlijk
- 2.2 Molaire massa
- 2.3 Smeltpunt
- 2.4 Dichtheid
- 2,5 pH
- 2.6 Oplosbaarheid in water
- 2,7 Kps
- 2.8 Brekingsindex
- 2.9 Stabiliteit
- 3 Verkrijgen
- 4 toepassingen
- 4.1 Voedselbehandeling
- 4.2 Riolering ontsmettingsmiddel
- 4.3 Papierindustrie
- 4.4 Gasabsorbeerder
- 4.5 Persoonlijke verzorging
- 4.6 Bouwwerkzaamheden
- 5 Risico's en bijwerkingen
- 6 referenties
Structuur
Kristal en zijn ionen
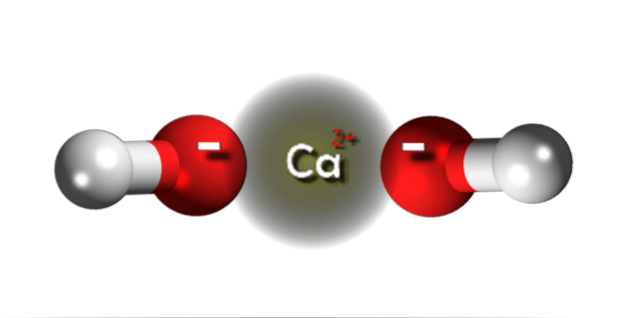
In de bovenste afbeelding hebben we de ionen waaruit calciumhydroxide bestaat. Dezelfde formule Ca (OH)twee wijst erop dat voor elk kation Catwee+ er zijn twee OH-anionen- die ermee in wisselwerking staan door middel van elektrostatische aantrekking. Het resultaat is dat beide ionen uiteindelijk een kristal vormen met een hexagonale structuur.
In dergelijke hexagonale kristallen van Ca (OH)twee de ionen zijn zeer dicht bij elkaar, waardoor het lijkt alsof ze een polymere structuur zijn; hoewel er formeel geen Ca-O covalente binding is gezien het opmerkelijke verschil in elektronegativiteit tussen de twee elementen.
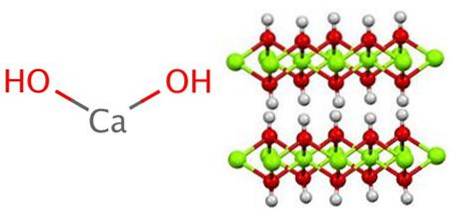
De structuur genereert octaëders CaO6, dat wil zeggen, de Catwee+ interageert met zes OH- (ACtwee+-Oh-.
Een reeks van deze octaëders vormt een laag van het kristal, die met een andere kunnen interageren via waterstofbruggen die ze intermoleculair samenhangend houden; deze interactie verdwijnt echter bij een temperatuur van 580 ºC, wanneer Ca (OH) wordt gedehydrateerdtwee naar CaO.
Aan de kant van hoge drukken is er in dit opzicht niet veel informatie, hoewel studies hebben aangetoond dat bij een druk van 6 GPa het hexagonale kristal een overgang ondergaat van de hexagonale naar de monokliene fase; en daarmee de vervorming van de octaëder CaO6 en zijn lagen.
Morfologie
De kristallen van Ca (OH)twee Ze zijn zeshoekig, maar dat is voor hen geen belemmering om enige morfologie aan te nemen. Sommige van deze structuren (zoals strengen, schilfers of rotsen) zijn poreuzer dan andere, robuust of vlak, wat een directe invloed heeft op hun uiteindelijke toepassing..
Het is dus niet hetzelfde om kristallen van het mineraal portlandiet te gebruiken als om ze te synthetiseren zodat ze bestaan uit nanodeeltjes waarbij een paar strikte parameters worden gevolgd; zoals de mate van hydratatie, de gebruikte concentratie CaO en de tijd dat het kristal mag groeien.
Eigendommen
Fysiek uiterlijk
Witte, reukloze, poederachtige vaste stof met een bittere smaak.
Molaire massa
74,093 g / mol
Smeltpunt
580 ° C. Bij deze temperatuur ontleedt het waarbij water vrijkomt, zodat het nooit verdampt:
Ca (OH)twee => CaO + HtweeOF
Dichtheid
2.211 g / cm3
pH
Een verzadigde waterige oplossing daarvan heeft een pH van 12,4 bij 25 ºC.
Oplosbaarheid in water
De oplosbaarheid van Ca (OH)twee in water neemt het af naarmate de temperatuur stijgt. Bij 0 ºC is de oplosbaarheid bijvoorbeeld 1,89 g / l; terwijl deze bij 20 ºC en 100 ºC respectievelijk 1,73 g / l en 0,66 g / l zijn.
Dit duidt op een thermodynamisch feit: de hydratatie van Ca (OH)twee is exotherm, dus gehoorzamend aan het principe van Le Chatelier zou de vergelijking zijn:
Ca (OH)twee <=> ACtwee+ + 2OH- + Q
Waar Q de warmte is die vrijkomt. Hoe heter het water, hoe meer evenwicht naar links neigt; dat wil zeggen, minder het Ca (OH) zal oplossentwee. Het is om deze reden dat het in koud water veel meer oplost dan in kokend water..
Aan de andere kant neemt de oplosbaarheid toe als de pH zuur wordt, vanwege de neutralisatie van de OH-ionen.- en de verplaatsing van het voorste evenwicht naar rechts. Bij dit proces komt zelfs meer warmte vrij dan bij neutraal water. Naast zure waterige oplossingen, Ca (OH)twee het is ook oplosbaar in glycerol.
Kps
5,5 10-6. Deze waarde wordt als klein beschouwd en komt overeen met de lage oplosbaarheid van Ca (OH)twee in het water (zelfde balans als hierboven).
Brekingsindex
1.574
Stabiliteit
Ca (OH)twee blijft stabiel zolang het niet wordt blootgesteld aan COtwee uit de lucht, omdat het het absorbeert en calciumcarbonaat, CaCO, vormt3. Daarom begint het vervuild te raken tot een vast mengsel van Ca (OH) -kristallentwee-Dief3, waar er CO-anionen zijn3twee- concurreren met de OH- om te communiceren met Catwee+
Ca (OH)twee + COtwee => CaCO3 + H.tweeOF
Dit is in feite de reden waarom geconcentreerde oplossingen van Ca (OH)twee ze worden melkachtig als een suspensie van CaCO-deeltjes verschijnt3.
Het verkrijgen van
Ca (OH)twee Het wordt commercieel verkregen door kalk, CaO, te laten reageren met een twee- tot drievoudige overmaat water:
CaO + HtweeO => Ca (OH)twee
In het proces kan echter carbonisatie van Ca (OH) optredentwee, net zoals hierboven uitgelegd.
Andere methoden om het te verkrijgen zijn het gebruik van oplosbare calciumzouten, zoals CaCltwee of Ca (NO3twee, en maak ze basisch met NaOH, zodat Ca (OH) neerslaattwee. Door parameters zoals watervolumes, temperatuur, pH, oplosmiddel, carbonisatiegraad, rijpingstijd, etc. te regelen, kunnen nanodeeltjes met verschillende morfologieën worden gesynthetiseerd.
Het kan ook worden bereid door natuurlijke en hernieuwbare grondstoffen te selecteren, of afval uit een industrie dat rijk is aan calcium, dat bij verhitting en verwerking zal bestaan uit kalk; en vanaf hier kan opnieuw het Ca (OH) worden bereidtwee door deze as te hydrateren zonder de noodzaak om kalksteen, CaCO, te verspillen3.
Hiervoor is bijvoorbeeld agave-bagasse gebruikt, waarmee een meerwaarde wordt toegekend aan afval uit de tequila-industrie..
Toepassingen
Voedselverwerking

Calciumhydroxide is aanwezig in veel voedingsmiddelen in sommige van de voorbereidingsfasen. Augurken, zoals augurken, worden bijvoorbeeld ondergedompeld in een waterige oplossing ervan om ze knapperiger te maken als ze in azijn worden verpakt. Dit komt doordat de eiwitten op het oppervlak calcium uit het medium absorberen..
Hetzelfde gebeurt met maïskorrels voordat ze in meel worden omgezet, omdat het helpt om vitamine B vrij te maken3 (niacine) en maakt het gemakkelijk te malen. Het calcium dat het levert, wordt ook gebruikt om voedingswaarde toe te voegen aan bepaalde sappen.
Ca (OH)twee Het kan in sommige broodrecepten ook bakpoeder vervangen en de suikerachtige oplossingen uit suikerriet en bieten verduidelijken..
Riolering ontsmettingsmiddel
De verhelderende werking van Ca (OH)twee Het is omdat het werkt als een uitvlokmiddel; dat wil zeggen, het vergroot de grootte van de gesuspendeerde deeltjes totdat ze vlokken vormen, die later bezinken of kunnen worden gefilterd.
Deze eigenschap is gebruikt om rioolwater te desinfecteren en de colloïden te destabiliseren die onaangenaam zijn voor het zicht (en de geur) van toeschouwers..
Papierindustrie
Ca (OH)twee het wordt gebruikt in het Kraft-proces om de NaOH te regenereren die wordt gebruikt om hout te behandelen.
Gasabsorbeerder
Ca (OH)twee gebruikt om CO te verwijderentwee van gesloten ruimtes of in omgevingen waar hun aanwezigheid contraproductief is.
Persoonlijke verzorging
In formuleringen voor ontharingscrèmes Ca (OH)twee Het wordt stilzwijgend gevonden, omdat de basiciteit ervan helpt bij het verzwakken van de keratine van de haren, en het dus gemakkelijker is om ze te verwijderen.
Bouw

Ca (OH)twee Het is aanwezig sinds onheuglijke tijden en integreert de massa gips en mortel die worden gebruikt bij de constructie van Egyptische architecturale werken zoals de piramides; ook gebouwen, mausolea, muren, trappen, vloeren, steunen en zelfs om tandcement te herbouwen.
De versterkende werking is te danken aan het feit dat bij het "inademen" COtwee, de resulterende kristallen van CaCO3 eindig de integratie van het zand en de andere componenten van dergelijke mengsels in een betere mate.
Risico's en bijwerkingen
Ca (OH)twee Het is geen sterk basische vaste stof in vergelijking met andere hydroxiden, hoewel het meer is dan Mg (OH)twee. Ondanks dat het niet reactief of ontvlambaar is, is het basiciteit ervan nog steeds agressief genoeg om kleine brandwonden te veroorzaken..
Daarom moet er met respect mee worden omgegaan, omdat het de ogen, tong en longen kan irriteren en ook andere kwalen kan veroorzaken, zoals: verlies van het gezichtsvermogen, ernstige alkalisatie van het bloed, huiduitslag, braken en keelpijn.
Referenties
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). Mc Graw Hill.
- Wikipedia. (2019). Calcium hydroxide. Hersteld van: en.wikipedia.org
- Chávez Guerrero et al. (2016). Synthese en karakterisering van calciumhydroxide verkregen uit agave bagasse en onderzoek naar de antibacteriële werking ervan. Hersteld van: scielo.org.mx
- Riko Iizuka, Takehiko Yagi, Kazuki Komatsu, Hirotada Gotou, Taku Tsuchiya, Keiji Kusaba, Hiroyuki Kagi. (2013). Kristalstructuur van de hogedrukfase van calciumhydroxide, portlandiet: in situ poeder- en enkelkristal röntgendiffractieonderzoek. Amerikaanse mineraloog; 98 (8-9): 1421-1428. doi: doi.org/10.2138/am.2013.4386
- Hans Lohninger. (05 juni 2019). Calcium hydroxide. Chemie LibreTexts. Hersteld van: chem.libretexts.org
- Aniruddha S. et al. (2015). Synthese van nano-calciumhydroxide in waterig medium. De American Ceramic Society. doi.org/10.1111/jace.14023
- Carly Vandergriendt. (12 april 2018). Hoe wordt calciumhydroxide in voedsel gebruikt en is het veilig? Hersteld van: healthline.com
- Brian Clegg. (26 mei 2015). Calcium hydroxide. Hersteld van: chemistryworld.com



Niemand heeft nog op dit artikel gereageerd.