
Amorfe vaste structuur, eigenschappen, voorbeelden
De amorfe vaste stoffen Het zijn degenen die geen ordelijke langetermijnstructuur hebben. Ze zijn het tegenovergestelde van wat bekend staat als een kristallijne vaste stof. De deeltjes zijn op een ongeordende manier met elkaar verbonden, vergelijkbaar met die van vloeistoffen, maar met voldoende kracht om samen te smelten tot een vaste structuur..
Dit amorfe karakter komt vaker voor dan u misschien denkt; het is in feite een van de mogelijke toestanden die gecondenseerde materie kan aannemen. Hiermee wordt duidelijk dat elke verbinding die kan stollen en daarom kan kristalliseren, ook op een ongeordende manier kan agglomereren als de experimentele omstandigheden dit toelaten..

Het bovenstaande is meestal van toepassing op zuivere stoffen, of het nu gaat om elementen of verbindingen. Maar het is ook geldig in het geval van mengsels. Veel vaste mengsels zijn amorf, zoals suikerspin, chocolade, mayonaise of aardappelpuree..
Het feit dat een vaste stof amorf is, maakt het niet minder waardevol dan een kristallijne. Structurele wanorde schenkt het soms unieke eigenschappen die het niet zou vertonen in een kristallijne toestand. In de fotovoltaïsche industrie heeft amorf silicium bijvoorbeeld de voorkeur boven kristallijn voor bepaalde kleinschalige toepassingen.
Artikel index
- 1 Structuur van amorfe vaste stoffen
- 2 Eigenschappen
- 3 Voorbereiding
- 4 Voorbeelden van amorfe vaste stoffen
- 4.1 Mineralen en kunststoffen
- 4.2 Biologisch weefsel
- 4.3 Bril
- 4.4 Koolstof en metalen
- 5 referenties
Structuur van amorfe vaste stoffen
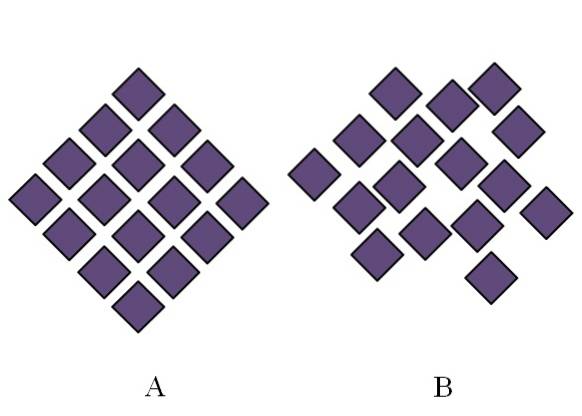
De structuur van een amorfe vaste stof is rommelig; het mist periodiciteit of structureel patroon. De afbeelding hierboven illustreert dit punt. A komt overeen met een kristallijne vaste stof, terwijl B een amorfe vaste stof voorstelt. Merk op dat in B de paarse diamanten willekeurig zijn gerangschikt, ook al zijn er zowel in A als B hetzelfde soort interacties.
Als B ook in acht wordt genomen, is te zien dat er spaties zijn die leeg lijken te zijn; dat wil zeggen, de structuur heeft gebreken of onregelmatigheden. Daarom is een deel van de microscopische of interne wanorde van een amorfe vaste stof het gevolg van het feit dat de deeltjes zodanig zijn "gerangschikt" dat de resulterende structuur veel onvolkomenheden heeft..
Als eerste werd melding gemaakt van de reikwijdte in de ordeningsgraad van amorfe vaste stoffen. In B zijn er slechts een paar ruiten die netjes uitgelijnd lijken te zijn. Er kunnen geordende regio's zijn; maar alleen op korte afstand.
Een amorfe vaste stof zou dan bestaan uit onmetelijke kleine kristallen met verschillende structuren. De som van al deze structuren wordt uiteindelijk labyrintisch en zinloos: de globale structuur wordt amorf, opgebouwd uit eindeloze kristallijne blokken die overal verspreid zijn..
Eigendommen
De eigenschappen van een amorfe vaste stof variëren afhankelijk van de aard van de samenstellende deeltjes. Er zijn echter bepaalde algemene kenmerken die kunnen worden genoemd. Amorfe vaste stoffen kunnen glasachtig zijn, wanneer ze soortgelijke aspecten vertonen als kristallen; of gelatineus, harsachtig of stoffig.
Omdat hun structuren wanordelijk zijn, genereren ze geen betrouwbare röntgendiffractiespectra en evenzo zijn hun smeltpunten niet nauwkeurig, maar bestrijken ze eerder een reeks waarden..
Het smeltpunt voor een amorfe vaste stof kan bijvoorbeeld variëren van 20 tot 60 ° C. Ondertussen smelten kristallijne vaste stoffen bij een specifieke temperatuur, of in een smal bereik als ze veel onzuiverheden bevatten..
Een ander kenmerk van amorfe vaste stoffen is dat wanneer ze breken of breken, ze geen geometrische fragmenten met platte vlakken produceren, maar onregelmatige fragmenten met gebogen vlakken. Als ze niet glasachtig zijn, zien ze eruit als stoffige en ondoorzichtige lichamen.
Voorbereiding
In plaats van een amorfe vaste stof, moet dit concept worden behandeld als een 'amorfe toestand'. Alle verbindingen (ionisch, moleculair, polymeer, metallisch, enz.) Zijn tot op zekere hoogte en indien experimentele omstandigheden dit toelaten in staat om amorfe en niet-kristallijne vaste stoffen te vormen..
Zo worden in organische syntheses vaste verbindingen aanvankelijk verkregen als poedervormige massa. Het gehalte aan onzuiverheden is zo hoog dat ze de moleculaire orde in grote mate beïnvloeden. Dat is de reden waarom wanneer het product keer op keer herkristalliseert, de vaste stof steeds kristallijn wordt; het verliest zijn amorf karakter.
Dit wil echter niet zeggen dat amorfe vaste stoffen noodzakelijkerwijs onzuivere materialen zijn; verscheidene van hen zijn amorf door hun eigen chemische aard.
Een zuivere stof kan amorf stollen als de vloeistof plotseling wordt afgekoeld, zodanig dat de deeltjes niet kristalliseren, maar een glasachtige vorm aannemen. De koeling is zo snel dat de deeltjes niet genoeg tijd hebben om de kristallijne blokken op te nemen die nauwelijks kunnen "geboren worden".
Water kan bijvoorbeeld in een glazige, amorfe toestand bestaan, en niet alleen als ijs.
Voorbeelden van amorfe vaste stoffen
Mineralen en kunststoffen

Vrijwel elk kristallijn materiaal kan zich aanpassen aan een amorfe vorm (en vice versa). Dit gebeurt met sommige mineralen, die om geochemische redenen formeel hun conventionele kristallen niet konden vestigen. Anderen daarentegen vormen geen kristallen maar glas; dat is het geval bij obsidiaan.
Aan de andere kant hebben polymeren de neiging om amorf te stollen, omdat hun moleculen te groot zijn om een geordende structuur te definiëren. Hier komen onder andere harsen, rubbers, piepschuim (anime), plastics, teflon, bakeliet binnen..
Biologisch weefsel
Biologische vaste stoffen zijn meestal amorf, zoals: orgaanweefsel, huid, haar, hoornvlies, enz. Evenzo vormen vet en eiwitten amorfe massa's; die echter met de juiste voorbereiding kunnen kristalliseren (DNA-kristallen, eiwitten, vetten).
Bril

Hoewel het bijna als laatste is achtergelaten, is de meest representatieve amorfe vaste stof verreweg het glas zelf. De samenstelling is in wezen dezelfde als die van kwarts: SiOtwee. Zowel kwartskristal als glas zijn driedimensionale covalente netwerken; alleen dat het glasrooster rommelig is, met Si-O-bindingen van verschillende lengtes.

Glas is de typische amorfe vaste stof en materialen die er ongeveer hetzelfde uitzien, zouden een glazige toestand hebben..
Koolstof en metalen
We hebben amorfe koolstof, waarvan actieve kool een van de belangrijkste is vanwege het absorberende vermogen. Evenzo is er amorf silicium en germanium, met elektronische toepassingen waar ze als halfgeleiders werken..
En tot slot zijn er amorfe legeringen die geen kristallijne structuur tot stand brengen vanwege de ongelijkheid van hun metaalatomen..
Referenties
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8e ed.). CENGAGE Leren.
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). Mc Graw Hill.
- Rachel Bernstein en Anthony Carpi. (2020). Eigenschappen van vaste stoffen. Hersteld van: visionlearning.com
- Wikipedia. (2020). Amorfe vaste stof. Hersteld van: en.wikipedia.org
- Richard Zallen, Ronald Walter Douglas en anderen. (31 juli 2019). Amorfe vaste stof. Encyclopædia Britannica. Hersteld van: britannica.com
- Elsevier B.V. (2020). Amorfe vaste stof. ScienceDirect. Hersteld van: sciencedirect.com
- Danielle Reid. (2020). Amorfe vaste stof: definitie en voorbeelden. Studie. Hersteld van: study.com
- Rubiks kubus kunstwerk. (2008). Wat is een amorf materiaal? Hersteld van: web.physics.ucsb.edu



Niemand heeft nog op dit artikel gereageerd.