
Tenecteplase waarvoor het is, structuur, werkingsmechanisme, dosis
De tenecteplase is een weefselplasminogeenactivator (tPA) gesynthetiseerd door de farmaceutische industrie met behulp van recombinant-DNA-technieken toegepast op een cellijn verkregen uit ovariumcellen van Chinese hamsters.
Het bloedstollingsproces, dat eindigt met de vorming van een trombus en het terugtrekken van het stolsel, gaat verder met een fase die fibrinolyse wordt genoemd. Deze fase wordt gekenmerkt door het oplossen van de trombus door de fragmentatie van het fibrinepolymeer in kleinere en beter oplosbare peptiden, en de herkanalisatie van het vat of de bloedvaten waar coagulatie optrad..
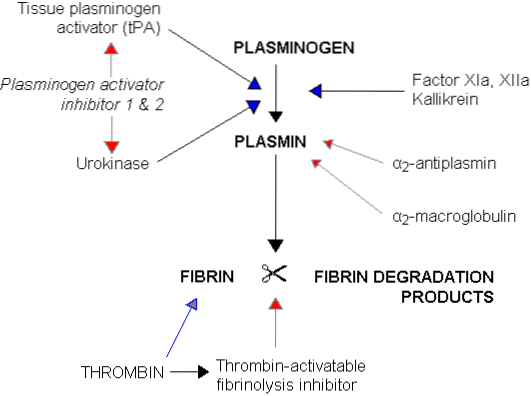
Dit fibrinolytische proces vereist de deelname van een bloedeiwit uit de groep van plasmaglobulinen, plasminogeen of profibrinolysine genaamd, van ongeveer 81 kDa, gesynthetiseerd in de lever en normaal aanwezig in circulerend bloed. Dit plasminogeen wordt tijdens coagulatie gevangen tussen de fibrinenetwerken waaruit de trombus bestaat..
Plasminogeen per se mist enige fibrinolytische werking, een werking die alleen optreedt wanneer het oorspronkelijke molecuul wordt geactiveerd en omgezet in plasmine of fibrinolysine, een serineprotease die sterk lijkt op trypsine, het belangrijkste proteolytische spijsverteringsenzym bij de afscheiding van de pancreas.
Plasmine heeft een hoge affiniteit voor fibrine, dat wordt afgebroken tot kleine oplosbare peptiden die op hun beurt de werking van trombine en de daaropvolgende productie van meer fibrine remmen. Het oefent ook een proteolytische werking uit op fibrinogeen, protrombine en stollingsfactoren V, VIII, IX, XI en XII, wat ook de stollingscapaciteit van het bloed vermindert..
Uit deze tabel kan worden afgeleid dat plasmine de bloedstollingsprocessen op twee manieren beïnvloedt, aangezien het enerzijds het oplossen van de trombus veroorzaakt door zijn fibrinolytische werking en anderzijds de stolling verstoort door zijn proteolytische werking. factoren van het stollingsproces.
Artikel index
- 1 Waar is tenecteplase voor?
- 2 Structuur van het molecuul
- 3 Werkingsmechanisme
- 4 Presentatie
- 5 dosis
- 6 referenties
Waar is tenecteplase voor?
Plasminogeenactivering vindt plaats door de individuele of gecombineerde werking van een reeks stoffen die in het algemeen plasminogeenactivatoren worden genoemd en die, afhankelijk van hun oorsprong, zijn gegroepeerd in plasminogeenactivatoren: bloed, urinewegen, weefsel en van micro-organismen.
Omdat het een weefselplasminogeenactivator is die het in plasmine omzet, en plasmine het fibrinolytische middel bij uitstek is, aangezien tenecteplase wordt gebruikt voor therapeutische fibrinolyse bij acuut myocardinfarct, trombo-embolische beroertes en pulmonale trombo-embolie..
Structuur van het molecuul
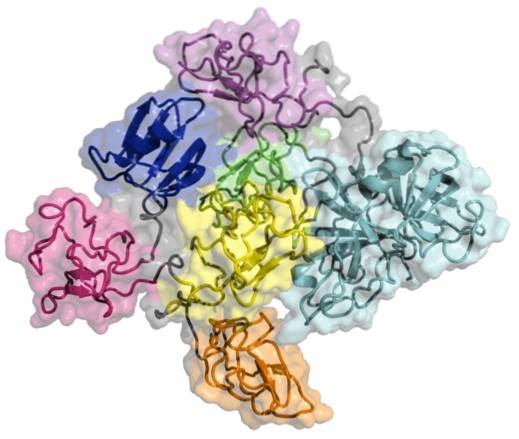
Tenecteplase is een glycoproteïne met 527 aminozuren in zijn primaire structuur en waarin twee basisdomeinen worden onderscheiden, een genaamd het kringle-domein en de andere die overeenkomt met het protease-domein..
Het kringle-domein is een gebied van het eiwit dat zich vouwt tot grote lussen die worden gestabiliseerd door disulfidebindingen. Dit type domein is erg belangrijk omdat het eiwit-eiwitinteracties mogelijk maakt die optreden met bloedstollingsfactoren en zijn naam ontleent aan een Scandinavische cake waarvan de vorm lijkt..
Het protease-domein is het gebied van het molecuul dat de proteolytische activiteit heeft die het enzym zelf zijn activerende functie geeft..
De structuur van het molecuul lijkt sterk op die van natuurlijk menselijk tPA, maar recombinant-DNA-technologie maakte de introductie mogelijk van enkele modificaties in het complementaire DNA (cDNA) die het erin gecodeerde eiwit enkele therapeutische voordelen geven..
Genoemde modificaties omvatten de vervanging van threonine op positie 103 door asparagine en asparagine 117 door glutamine, veranderingen die zich in het kringle-domein bevinden; terwijl in het protease-domein een tetra-alaninesamenstelling werd bereikt in het positionele bereik 296-299.
Werkingsmechanisme
Het werkingsmechanisme van tenecteplase is vergelijkbaar met dat van natuurlijk tPA. Zodra de trombus zich heeft gevormd, bindt plasminogeen in zijn inactieve vorm aan fibrine zonder enige proteolytische werking erop uit te oefenen..
Het door endotheelcellen geproduceerde tPA bindt zich aan fibrine en verkrijgt daarbij zijn plasminogeen-activerende eigenschap in plasmine, een stof die fibrinolyse op gang brengt..
De modificaties geproduceerd in het tPA-molecuul en opgenomen in tenecteplase maken de activerende werking van genoemde stof op plasminogeen gevoeliger voor de aanwezigheid van fibrine. Fibrinespecificiteit die de werking ervan beperkt tot trombuslocaties en de systemische plasminogeenactivering en de resulterende afbraak van plasmafibrinogeen vermindert.
Presentatie
De dosering of potentie van de stof wordt uitgedrukt in mg en in eenheden (E) tenecteplase. De eenheden vertegenwoordigen een specifieke referentiestandaard voor het medicijn en zijn niet vergelijkbaar met de eenheden van andere trombolytische middelen. Eén mg is gelijk aan 200 eenheden (U).
Een bedrijfsvorm is de Metalyse, die wordt geleverd in twee presentaties, elk met een injectieflacon met het product in de vorm van een wit poeder en een voorgevulde spuit met het oplosmiddel, transparant en kleurloos, voor reconstitutie.
In een ervan bevat de injectieflacon 8000 eenheden (40 mg) en de injectiespuit 8 ml oplosmiddel. In de andere bevat de injectieflacon 10.000 E (50 mg) en de injectiespuit 10 ml. In beide gevallen, als de oplossing eenmaal is gereconstitueerd door de inhoud van de injectiespuit aan de overeenkomstige injectieflacon toe te voegen, bevat deze 1000 eenheden (5 mg) voor elke ml en ziet deze er helder en kleurloos of lichtgeel uit..
Dosis
De behandeling met tenecteplase moet zo snel mogelijk worden gestart, binnen 6 uur na het begin van de symptomen. Vanwege de impliciete risico's van bloeding of bloeding, moet het worden voorgeschreven door artsen met ervaring in trombolytische behandeling en in instellingen die de middelen hebben om dit soort bijwerkingen te controleren en tegen te gaan..

De dosering van de stof dient gebaseerd te zijn op het lichaamsgewicht, met een minimumdosis van 6000 eenheden, overeenkomend met 30 mg opgelost in een volume van 6 ml van de gereconstitueerde oplossing, toe te dienen aan patiënten met een lichaamsgewicht van minder dan 60 kg..
De maximale dosis is 10.000 E (50 mg / 10 ml oplossing) gereserveerd voor patiënten met een lichaamsgewicht van 90 kg en meer..
Het doseringsschema voor patiënten met een gewicht tussen 60 en minder dan 90 kg is als volgt:
- ≥ 60 een < 70 = 7000 U (35 mg/7 ml)
- ≥ 70 a < 80 = 8000 U (40 mg/8 ml)
- ≥ 80 a < 90 = 9000 U (45 mg/9 ml)
De vereiste dosis moet worden toegediend als een enkele intraveneuze bolus en gedurende een periode van ongeveer 10 seconden. Het kan worden toegediend via een eerder aangesloten intraveneus circuit waardoor een fysiologische oplossing van 0,9% (9 mg / ml) natriumchloride wordt geleid.
Het medicijn is onverenigbaar met glucoseoplossingen en hoewel, volgens de huidige therapeutische criteria, adjuvante antitrombotische behandeling die plaatjesaggregatieremmers en anticoagulantia kan omvatten parallel moet worden toegediend, mag er geen ander geneesmiddel worden toegevoegd aan de injecteerbare oplossing van tenecteplase..
Referenties
- Balsera, E. C., Palomino, M. Á. P., Ordoñez, J. M., Caler, C. L., Paredes, T. G., & García, G. Q. (2011). Effectiviteit en veiligheid van alteplase versus tenecteplase bij fibrinolyse van acuut coronair syndroom met ST-elevatie. Cardiocore, 46(4), 150-154.
- Bauer C en Walzog B: Blut: ein Flüssiges Organsystem, in: Fysiologie, 6e ed; R. Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Fatovich, D. M., Dobb, G. J., & Clugston, R. A. (2004). Een gerandomiseerde pilot-studie van trombolyse bij hartstilstand (de TICA-studie). Reanimatie, 61(3), 309-313.
- Guyton AC, Hall JE: hemostase en bloedstolling, in: Textbook of Medical Physiology , 13e editie, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Haley Jr, E. C., Lyden, P. D., Johnston, K. C., Hemmen, T. M., en TNK in Stroke Investigators. (2005). Een pilot-veiligheidsstudie naar dosisverhoging van tenecteplase bij acute ischemische beroerte. Beroerte, 36(3), 607-612.
- Jelkman W: Blut, in: Physiologie des Menschen mit Pathophysiologie, 31e ed., RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.


Niemand heeft nog op dit artikel gereageerd.