
Kenmerken, structuur, functies van jodideperoxidase
De jodide peroxidase o schildklierperoxidase (TPO) is een heem-glycoproteïne behorend tot de familie van zoogdierperoxidasen (zoals myeloperoxidase, lactoperoxidase en andere) dat deelneemt aan de syntheseroute van het schildklierhormoon.
De belangrijkste functie is de "jodering" van tyrosineresiduen in thyroglobuline, en de vorming van 3-3'-5-trijoodthyronine (T3) en thyroxine (T4) door een "koppelingsreactie". Intramoleculair van gejodeerde tyrosines.
Triiodothyronine en thyroxine zijn twee hormonen die door de schildklier worden geproduceerd en die essentiële functies hebben bij de ontwikkeling, differentiatie en metabolisme van zoogdieren. Zijn werkingsmechanisme hangt af van de interactie van zijn nucleaire receptoren met specifieke gensequenties van zijn doelwitgenen..
Het bestaan van het enzym jodide peroxidase werd in de jaren zestig door verschillende auteurs bevestigd en er zijn nu aanzienlijke vorderingen gemaakt bij het bepalen van de structuur, de functies en de kenmerken van het gen dat ervoor codeert. In verschillende organismen..
In veel van de literatuur die betrekking heeft op dit enzym, staat het bekend als het microsomale "autoantigeen" en is het gerelateerd aan sommige auto-immuunziekten van de schildklier..
Dankzij zijn immunogene eigenschappen is dit enzym een doelwit of doelwitmolecuul voor de antilichamen die aanwezig zijn in het serum van veel patiënten met schildklierpathologieën en zijn defecten kunnen leiden tot hormonale tekortkomingen die pathofysiologisch gezien belangrijk kunnen zijn..
Artikel index
- 1 Kenmerken
- 1.1 Regulatie van meningsuiting
- 2 Structuur
- 3 functies
- 3.1 Wat is de synthese van schildklierhormoon?
- 4 Verwante ziekten
- 5 referenties
Kenmerken
Jodideperoxidase wordt gecodeerd door een gen op chromosoom 2 bij mensen, dat meer dan 150 kbp meet en is samengesteld uit 17 exons en 16 introns..
Dit transmembraaneiwit, met een enkel segment ondergedompeld in het membraan, is nauw verwant aan myeloperoxidase, met wie het meer dan 40% gelijkenis vertoont met aminozuursequenties..
De synthese vindt plaats in polyribosomen (een reeks ribosomen die verantwoordelijk zijn voor de vertaling van hetzelfde eiwit) en wordt vervolgens ingebracht in het membraan van het endoplasmatisch reticulum, waar het een proces van glycosylering ondergaat..
Eenmaal gesynthetiseerd en geglycosyleerd, wordt jodideperoxidase getransporteerd naar de apicale pool van thyrocyten (schildkliercellen of schildkliercellen), waar het zijn katalytische centrum kan blootstellen aan het folliculaire lumen van de schildklier..
Regulatie van meningsuiting
Expressie van het gen dat codeert voor schildklierperoxidase of jodideperoxidase wordt gecontroleerd door schildklierspecifieke transcriptiefactoren zoals TTF-1, TTF-2 en Pax-8.
De genetische elementen die het mogelijk maken de expressie van dit gen bij mensen te verhogen of te versterken, zijn beschreven in de gebieden die het 5'-uiteinde ervan flankeren, gewoonlijk tussen de eerste 140 basenparen van dit "flankerende" gebied..
Er zijn ook elementen die de expressie van dit eiwit onderdrukken of verminderen, maar in tegenstelling tot de "enhancers" zijn deze stroomafwaarts van de gensequentie beschreven..
Een groot deel van de regulatie van de genetische expressie van jodideperoxidase vindt plaats op een weefselspecifieke manier, en dit hangt af van de werking van DNA-bindende elementen die inwerken op cis, zoals TTF-1 transcriptiefactoren en andere.
Structuur
Dit eiwit met enzymatische activiteit heeft ongeveer 933 aminozuurresiduen en een extracellulair C-terminaal uiteinde van 197 aminozuren lang dat afkomstig is van de expressie van andere genmodules die coderen voor andere glycoproteïnen..
Het molecuulgewicht is ongeveer 110 kDa en maakt deel uit van de groep van type 1 geglycosyleerde transmembraaneiwitten, aangezien het een geglycosyleerd transmembraansegment en een heemgroep op zijn actieve plaats heeft..
De structuur van dit eiwit heeft ten minste één disulfidebrug in het extracellulaire gebied die een karakteristieke gesloten lus vormt die wordt blootgesteld aan het oppervlak van thyrocyten..
Kenmerken
De belangrijkste fysiologische functie van jodideperoxidase houdt verband met zijn deelname aan de synthese van schildklierhormoon, waar het de 'jodering' van tyrosineresiduen van monoiodotyrosine (MIT) en dijodotyrosine (DIT) katalyseert, naast de koppeling van de jodotyrosineresiduen in thyroglobuline.
Wat is de synthese van schildklierhormoon?
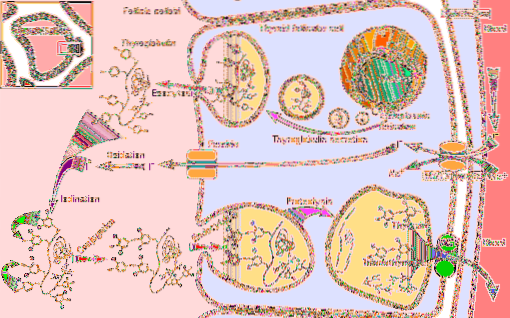
Om de functie van het schildklierperoxidase-enzym te begrijpen, is het noodzakelijk om de stappen van hormonale synthese te overwegen waaraan het deelneemt:
1-Het begint met het transport van jodide naar de schildklier en gaat verder met
2-Het genereren van een oxidatiemiddel zoals waterstofperoxide (H2O2)
3-Vervolgens wordt een receptoreiwit, thyroglobuline, gesynthetiseerd
4-Het jodide wordt geoxideerd tot een hogere valentie en vervolgens
5-jodide bindt aan tyrosineresiduen die aanwezig zijn in thyroglobuline
6-In thyroglobuline jodothyronines (een soort schildklierhormonen) worden gevormd door koppeling van jodotyrosineresiduen
7-Thyroglobuline wordt vervolgens opgeslagen en gekliefd
8-Het jodium wordt verwijderd uit de vrije jodotyrosines en tenslotte,
9-Thyroxine en trijoodthyronine komen vrij in het bloed; Deze hormonen oefenen hun effecten uit door interactie met hun specifieke receptoren, die zich op het kernmembraan bevinden en die in staat zijn om te interageren met doelwit-DNA-sequenties, die functioneren als transcriptiefactoren..
Zoals zou kunnen worden afgeleid uit de kennis van de functies van de twee hormonen in wiens synthese het deelneemt (T3 en T4), heeft jodideperoxidase belangrijke implicaties op fysiologisch niveau..
Het ontbreken van beide hormonen tijdens de menselijke ontwikkeling leidt tot groeiachterstand en mentale retardatie, evenals metabole onevenwichtigheden in het volwassen leven.
Gerelateerde ziekten
Jodideperoxidase is een van de belangrijkste auto-antigenen van de schildklier bij mensen en wordt in verband gebracht met door het complementsysteem gemedieerde cytotoxiciteit. Zijn functie als autoantigeen wordt benadrukt bij patiënten met auto-immuunziekten van de schildklier.
De jichtziekte is bijvoorbeeld het gevolg van een tekort aan jodium tijdens de hormoonsynthese in de schildklier, wat op zijn beurt weer verband houdt met een tekort aan jodering van thyroglobuline als gevolg van bepaalde defecten in jodideperoxidase..
Sommige carcinomen worden gekenmerkt door veranderde jodideperoxidase-functies, dat wil zeggen dat de activiteitsniveaus van dit enzym significant lager zijn dan bij niet-kankerpatiënten.
Studies hebben echter bevestigd dat het een zeer variabel kenmerk is, dat niet alleen afhangt van de patiënt, maar ook van het type kanker en de getroffen gebieden..
Referenties
- Degroot, L. J., en Niepomniszcze, H. (1977). Biosynthese van schildklierhormoon: fundamentele en klinische aspecten. Vooruitgang in endocrinologie en metabolisme, 26(6), 665-718.
- Fragu, P., & Nataf, B. M. (1976). Menselijke schildklierperoxidase-activiteit bij goedaardige en kwaadaardige schildklieraandoeningen. De endocriene samenleving, Vier vijf(5), 1089-1096.
- Kimura, S., en Ikeda-saito, M. (1988). Menselijke myeloperoxidase en schildklierperoxidase, twee enzymen met afzonderlijke en onderscheiden fysiologische functies, zijn evolutionair verwante leden van dezelfde genfamilie. Eiwitten: structuur, functie en bio-informatica, 3, 113-120.
- Nagasaka, A., Hidaka, H., en Ishizuki, Y. (1975). Onderzoek naar menselijk jodideperoxidase: de activiteit ervan bij verschillende schildklieraandoeningen. Chimica Acta-kliniek, 62, 1-4.
- Ruf, J., en Carayon, P. (2006). Structurele en functionele aspecten van schildklierperoxidase. Archives of Biochemistry and Biophysics, 445, 269-277.
- Ruf, J., Toubert, M., Czarnocka, B., Durand-gorde, M., Ferrand, M., & Carayon, P. (2015). Verband tussen immunologische structuur en biochemische eigenschappen van menselijke schildklierperoxidase. Endocriene beoordelingen, 125(3), 1211-1218.
- Taurog, A. (1999). Moleculaire evolutie van schildklierperoxidase. Biochimie, 81, 557-562.
- Zhang, J., & Lazar, M. A. (2000). Het werkingsmechanisme van schildklierhormonen. Annu. Rev. Physiol., 62(1), 439-466.



Niemand heeft nog op dit artikel gereageerd.