
Fosfaatbuffer (PBS) grondgedachte, bereiding en gebruik
De fosfaatbuffer, BPS of fosfaatbufferzoutoplossing Het is een buffer en isotone oplossing met als functie om de pH en osmotische druk zo dicht mogelijk bij de natuurlijke biologische (fysiologische) omgeving te houden. De afkorting PBS staat voor fosfaatgebufferde zoutoplossing..
De pH en osmolariteit zijn twee zeer belangrijke aspecten die in bepaalde laboratoriumprotocollen moeten worden gecontroleerd. In het geval van de pH is het essentieel dat deze wordt gecontroleerd, vooral bij biochemische reacties, aangezien deze kunnen variëren of niet kunnen worden uitgevoerd als de reactanten een onjuiste pH hebben.

Ondertussen is de controle van de osmolariteit essentieel, vooral bij het werken met levende cellen, omdat de plasmamembranen van de cellen reageren volgens de concentratie opgeloste stoffen waarin ze worden aangetroffen..
Als de cellen worden overgebracht naar een hypertoon medium, zullen ze uitdrogen, omdat de watergradiënt naar de kant wordt getransporteerd waar zich een hogere concentratie opgeloste stoffen bevindt. Als cellen daarentegen in een hypotoon medium worden geplaatst, zullen de cellen vloeistof opnemen totdat ze zijn gelyseerd..
Daarom wordt de PBS-buffer gebruikt voor laboratoriumprotocollen die het onderhoud van cellen vereisen. in vitro, op deze manier worden de cellen niet beschadigd.
PBS bestaat uit een combinatie van zouten, zoals natriumchloride, natriumfosfaat, kaliumchloride en kaliumfosfaat. De samenstelling van de PBS kan variëren, afhankelijk van het protocol..
Artikel index
- 1 Grondgedachte
- 2 Voorbereiding
- 2.1-stockoplossing fosfaatbuffer zoutoplossing (PBS 10X)
- 2.2-Buffer fosfaat zoutoplossing (1X PBS)
- 2.3 Oplossingen voor pH-aanpassing
- 3 toepassingen
- 4 Beperkingen
- 5 referenties
Basis
In wezen is de functie van de zoute fosfaatbuffer het handhaven van een constante fysiologische pH samen met een elektrolytconcentratie die vergelijkbaar is met die in het lichaam..
In deze omgeving kunnen cellen stabiel blijven, omdat fysiologische omstandigheden zoveel mogelijk worden nagebootst..
Andere verbindingen kunnen indien nodig aan de oorspronkelijke PBS-formulering worden toegevoegd, de toevoeging van EDTA aan de buffer is bijvoorbeeld nuttig voor het wassen van rode bloedcellen in de kruis-incompatibiliteitstest..
EDTA voorkomt dat de fractie van complement C1 die in het serum aanwezig is, wordt gesplitst en gelyseerd naar de rode bloedcellen, dat wil zeggen dat het valse incompatibiliteitsresultaten vermijdt. Bovendien helpt EDTA om cellen te dissociëren.
Voorbereiding
De hoeveelheid zouten die voor de bereiding van de PBS-fosfaatgebufferde zoutoplossing moet worden afgewogen, is afhankelijk van de hoeveelheid die moet worden bereid:
-Voorraadfosfaatgebufferde zoutoplossing (10X PBS)
Voor één liter oplossing:
Wegen:
80,6 g NaCl,
2,2 g KCl,
11,5 g NatweeHPO4,
2,0 g KHtweeHPO4
Voorbereidingstechniek
Doe de zware zouten in een bekerglas, voeg voldoende water (80%) toe en meng op de roerplaat met magneetstaaf tot de zouten zijn opgelost..

Filter om onopgeloste deeltjes te verwijderen. Gebruik filters met poriën van 0,45 µm. Autoclaaf en aseptisch verdelen in laminaire stroomkap in glazen potten met deksel.
De 10X-oplossing (geconcentreerd) past de pH niet aan. De aanpassing wordt gemaakt zodra verdund tot de 1X PBS-bufferconcentratie (1:10 verdunning).
-Fosfaatbuffer zoutoplossing (1X PBS)
1X PBS kan direct worden bereid, waarbij de overeenkomstige hoeveelheden van elk zout worden afgewogen, of het kan worden bereid door de stockoplossing (1:10) te verdunnen met steriel gedestilleerd water..
-Om direct een liter 1X PBS-fosfaatgebufferde zoutoplossing te bereiden, weegt u:
8,06 g NaCl,
0,22 g KCl,
1,15 g NatweeHPO4,
0,20 g KHtweeHPO4
Voorbereidingstechniek
Ga verder zoals uitgelegd voor de geconcentreerde oplossing. Vervolgens moet de pH worden aangepast. Meet hiervoor de pH en gebruik, afhankelijk van het resultaat, zuur (HCl) of base (NaOH) om de pH naar behoefte te verlagen of te verhogen, totdat deze 7,4 is..
Het zuur of de base wordt druppelsgewijs toegevoegd terwijl de pH-waarde van de oplossing wordt bewaakt met een pH-meter. Filter, autoclaaf en aseptisch verdeel in conische buizen of potten indien nodig.
-Om 1X PBS uit de 10X-stockoplossing te bereiden:
Maak een verdunning van 1:10. Om bijvoorbeeld 1 liter 1X PBS te bereiden, meet u 100 ml van de stockoplossing af en voegt u 700 ml steriel gedestilleerd water toe. Pas de pH aan en vul de hoeveelheid water tot 1000 ml.
De bereide PBS-buffer is kleurloos en transparant.
De dagelijkse PBS kan op kamertemperatuur worden bewaard en de rest in de koelkast.
.Oplossingen voor pH-aanpassing
HCl
Voor 100 ml 1 molair HCL (zoutzuur).
Meet 91 ml gedestilleerd water af en doe het in een bekerglas van 250 ml.
Meet 8,62 ml geconcentreerd HCl af en doe dit langzaam in het bekerglas met het water (doe het nooit andersom). Neem de relevante bioveiligheidsmaatregelen bij het omgaan met sterke zuren (sterk bijtende stof).
Meng gedurende 5 minuten bij voorkeur met een roerplaat met een magneetstaaf in het glas. Breng over in een ballon van 100 ml en vul aan tot 100 ml met H.tweeOf gedestilleerd.
NaOH
Voor 100 ml NaOH (natriumhydroxide) 10 molair.
Meet 40 ml gedestilleerd water af en doe het in een bekerglas van 250 ml. Meet 40 g NaOH af en voeg toe aan het water. Meng met behulp van een roerplaat met een magnetische staaf in het glas.
Breng over in een maatkolf van 100 ml en vul aan tot de maatstreep met gedestilleerd water. Voldoen aan bioveiligheidsvoorschriften, omdat deze reactie exotherm is (er komt energie vrij in de vorm van warmte).
Als u andere hoeveelheden fosfaatzoutoplossing wilt bereiden, kunt u de volgende tabel raadplegen:
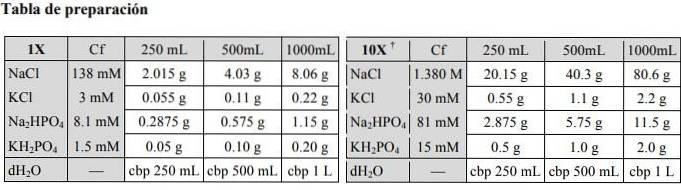
Toepassingen
Hoofdzakelijk gebruikt in celbiologie, immunologie, immunohistochemie, bacteriologie, virologie en onderzoekslaboratoria.
Het is ideaal voor het wassen van cellen door centrifugatie (rode bloedcellen), het wassen van monolagen van cellen, in spectroscopische ellipsometrie-technieken, bij de kwantificering van bacteriële biofilms, bij het in stand houden van celculturen voor virussen, als wasoplossing bij de indirecte immunofluorescentietechniek. En in technieken voor de karakterisering van monoklonale antilichamen.
Het wordt ook gebruikt om cellen of weefsels te transporteren, als verdunningsmiddel voor het tellen van cellen, de bereiding van cellulaire enzymen (trypsine), als verdunningsmiddel voor de biomolecuul-uitdroogmethode en om andere reagentia te bereiden..
Aan de andere kant hebben Martin et al. In 2006 aangetoond dat PBS nuttig is in forensische wetenschappelijke laboratoria, met name bij het herstel van sperma uit vaginale uitstrijkjes, of bij het herstel van vaginale cellen uit penisuitstrijkjes. Op deze manier kan worden vastgesteld of er een seksuele relatie is geweest.
Beperkingen
-Sommige PBS-buffers bevatten een stof genaamd natriumazide als conserveermiddel. Deze verbinding kan explosieve stoffen produceren als deze in contact komt met lood of koper. Om deze reden moet speciale aandacht worden besteed aan het afvoeren van dit reagens in de afvoer. Als het op deze manier wordt weggegooid, moet er veel water worden toegevoegd om het zoveel mogelijk te verdunnen..
-Zink mag niet aan de fosfaatbuffer worden toegevoegd, omdat hierdoor sommige zouten neerslaan.
-Wangen et al.In 2018 vastgesteld dat het gebruik van PBS niet geschikt was voor het wassen van primaire acute myeloïde leukemie (AML) -cellen die uit perifeer bloed zijn gehaald, vanwege het feit dat veel cellen verloren gaan door lysis, met een grote afname van eiwitmateriaal.
Daarom stelden ze vast dat primaire AML-cellen na opslag in vloeibare stikstof niet met PBS mogen worden gewassen..
Referenties
- Coll J. (1993). Diagnostische technieken in virologie. Ed Díaz de Santos. 360 pag
- Rodríguez M, Ortiz T. Celcultuur. Verandering van medium. Afdeling Normale en Pathologische Cytologie en Histologie Universiteit van Sevilla. Beschikbaar op personal.us.es
- Bereiding van met fosfaat gebufferde zoutoplossing (PBS). (2008). Standard Operating Procedures (SOP's) Laboratorium voor virale en menselijke genomica UASLP School of Medicine. Beschikbaar op: genomica.uaslp.mx
- "Fosfaatbuffer zoutoplossing." Wikipedia, de gratis encyclopedie. 3 april 2019, 19:36 UTC. 13 april 2019, 02:57 en.wikipedia.org.
- Pietrasanta L, Von-Bilderling C. Onderwerpen in moleculaire biofysica. Beschikbaar op: users.df.uba.ar
- Rediar. Handleiding. PBS + EDTA. Beschikbaar op: felsan.com.ar
- Martin NC, Pirie AA, Ford LV, Callaghan CL, McTurk K, Lucy D, Scrimger DG. Het gebruik van fosfaatgebufferde zoutoplossing voor het herstel van cellen en spermatozoa uit wattenstaafjes. Sci Justice. 2006; 46 (3): 179-84. Beschikbaar in: ncbi.nlm.nih.gov
- Wangen R, Aasebø E, Trentani A, et al. Bewaarmethode en wassen met fosfaatgebufferde zoutoplossing beïnvloeden het acute myeloïde leukemie-proteoom. Int J Mol Sci. 2018; 19 (1): 296. Beschikbaar in: ncbi.nlm.nih.gov
- Martínez R, Gragera R. (2008). Theoretische en praktische grondslagen van histochemie. Hoge Raad voor Wetenschappelijk Onderzoek. Madrid. Beschikbaar op: books.google.co.ve



Niemand heeft nog op dit artikel gereageerd.