
Zuurstofcycluskarakteristieken, reservoirs en stadia

De zuurstofcyclus verwijst naar de circulatiebeweging van zuurstof op aarde. Het is een gasvormige biogeochemische cyclus. Zuurstof is het tweede meest voorkomende element in de atmosfeer, na stikstof, en het tweede meest voorkomende element in de hydrosfeer, na waterstof. In die zin is de zuurstofcyclus verbonden met de watercyclus..
De circulatie van zuurstof omvat de productie van dizuurstof of twee-atoom moleculaire zuurstof (OtweeDit gebeurt als gevolg van hydrolyse tijdens fotosynthese uitgevoerd door de verschillende fotosynthetische organismen..

De Otwee Het wordt door levende organismen gebruikt bij cellulaire ademhaling, waarbij de productie van kooldioxide (COtwee), dit laatste is een van de grondstoffen voor het fotosyntheseproces.
Aan de andere kant vindt in de bovenste atmosfeer fotolyse (hydrolyse geactiveerd door zonne-energie) van waterdamp plaats, veroorzaakt door ultraviolette straling van de zon. Water wordt afgebroken waarbij waterstof vrijkomt dat verloren gaat in de stratosfeer en zuurstof wordt geïntegreerd in de atmosfeer.
Door interactie met een molecuul van Otwee Met een zuurstofatoom, ozon (O3Ozon vormt de zogenaamde ozonlaag.
Artikel index
- 1 Kenmerken
- 1.1 Herkomst
- 1.2 Primitieve atmosfeer
- 1.3 Energieën die de cyclus aandrijven
- 1.4 Relatie met andere biogeochemische cycli
- 2 reservoirs
- 2.1 Geosfeer
- 2.2 Sfeer
- 2.3 Hydrosfeer
- 2.4 Cryosphere
- 2.5 Levende organismen
- 3 stadia
- 3.1 -Milieustadium van reservoir en bron: atmosfeer-hydrosfeer-cryosfeer-geosfeer
- 3.2 - Fotosynthetische fase
- 3.3 - Atmosferische retourfase
- 3.4 -Ademhalingsfase
- 4 Belang
- 5 Wijzigingen
- 5.1 Broeikaseffect
- 6 referenties
Kenmerken
Zuurstof is een niet-metalen chemisch element. Het atoomnummer is 8, dat wil zeggen, het heeft 8 protonen en 8 elektronen in zijn natuurlijke staat. Onder normale temperatuur- en drukomstandigheden is het aanwezig in de vorm van zuurstofgas, kleurloos en geurloos. De moleculaire formule is Otwee.
De Otwee bevat drie stabiele isotopen: 16OF, 17Of en 18O. De overheersende vorm in het universum is de 16O. Op aarde vertegenwoordigt het 99,76% van de totale zuurstof. De 18Of vertegenwoordigt 0,2%. De vorm 17Of is het zeer zeldzaam (~ 0,04%).
Bron
Zuurstof is het derde meest voorkomende element in het universum. Isotopenproductie 16Of het begon met de eerste generatie zonneverbranding van helium die plaatsvond na de oerknal.
De totstandbrenging van de koolstof-stikstof-zuurstof-nucleosynthesecyclus in latere generaties sterren heeft de overheersende bron van zuurstof op de planeten opgeleverd..
Hoge temperaturen en drukken produceren water (H.tweeO) in het heelal door de reactie van waterstof met zuurstof op te wekken. Water maakt deel uit van de samenstelling van de kern van de aarde.
Magma-ontsluitingen geven water af in de vorm van stoom en dit komt in de waterkringloop. Water wordt door fotolyse afgebroken tot zuurstof en waterstof door fotosynthese en door ultraviolette straling in de bovenste niveaus van de atmosfeer..
Primitieve sfeer
De primitieve atmosfeer vóór de evolutie van fotosynthese door cyanobacteriën was anaëroob. Voor levende organismen die aan die atmosfeer waren aangepast, was zuurstof een giftig gas. Zelfs vandaag de dag veroorzaakt een atmosfeer van zuivere zuurstof onherstelbare schade aan cellen.
Fotosynthese is ontstaan in de evolutionaire lijn van de huidige cyanobacteriën. Hierdoor begon de samenstelling van de atmosfeer van de aarde ongeveer 2,3-2,7 miljard jaar geleden te veranderen..
De proliferatie van fotosynthetiserende organismen veranderde de samenstelling van de atmosfeer. Het leven evolueerde naar aanpassing aan een aerobe atmosfeer.
Energieën die de cyclus aandrijven
De krachten en energieën die werken om de zuurstofcyclus aan te drijven, kunnen geothermisch zijn, wanneer magma waterdamp verdrijft, of het kan afkomstig zijn van zonne-energie.
Dit laatste levert de fundamentele energie voor het fotosyntheseproces. Chemische energie in de vorm van koolhydraten die het resultaat zijn van fotosynthese, drijft op zijn beurt alle levende processen door de voedselketen aan. Op dezelfde manier produceert de zon differentiële planetaire verwarming en veroorzaakt ze zee- en atmosferische stromingen..
Relatie met andere biogeochemische cycli
Vanwege zijn overvloed en hoge reactiviteit, verbindt de zuurstofcyclus zich met andere cycli zoals COtwee, stikstof (Ntwee) en de waterkringloop (H.tweeOF). Dit geeft het een multicyclisch karakter.
De reservoirs van Otwee en cotwee ze zijn met elkaar verbonden door processen die de vorming (fotosynthese) en vernietiging (ademhaling en verbranding) van organisch materiaal met zich meebrengen. Op korte termijn zijn deze oxidatiereductiereacties de belangrijkste bron van variabiliteit in de O-concentratie.twee in de atmosfeer.
Denitrificerende bacteriën halen zuurstof voor hun ademhaling uit nitraten in de bodem, waardoor stikstof vrijkomt.
Reservoirs
Geosfeer
Zuurstof is een van de belangrijkste componenten van silicaten. Daarom vormt het een belangrijk deel van de aardmantel en aardkorst..
- Aarde kern: in de vloeibare buitenmantel van de aardkern bevinden zich naast ijzer nog andere elementen, waaronder zuurstof.
- Bodem: in de ruimtes tussen deeltjes of poriën van de bodem wordt de lucht verspreid. Deze zuurstof wordt gebruikt door de microbiota in de bodem.
Atmosfeer
21% van de atmosfeer bestaat uit zuurstof in de vorm van dizuurstof (OtweeDe andere vormen van aanwezigheid van zuurstof uit de lucht zijn waterdamp (H.tweeO), kooldioxide (COtwee) en ozon (O3.
- Water stoom: de waterdampconcentratie is variabel, afhankelijk van de temperatuur, atmosferische druk en atmosferische circulatiestromen (watercyclus).
- Kooldioxide: de COtwee Het vertegenwoordigt ongeveer 0,03% van het luchtvolume. Sinds het begin van de industriële revolutie is de concentratie CO toegenomentwee in de atmosfeer met 145%.
- Ozon: is een molecuul dat in een kleine hoeveelheid in de stratosfeer aanwezig is (0,03 - 0,02 volumedelen per miljoen).
Hydrosfeer
71% van het aardoppervlak is bedekt met water. Meer dan 96% van het water op het aardoppervlak is geconcentreerd in de oceanen. 89% van de massa van de oceanen bestaat uit zuurstof. De COtwee Het wordt ook opgelost in water en ondergaat een uitwisselingsproces met de atmosfeer..
Cryosphere
De cryosfeer verwijst naar de massa bevroren water die bepaalde delen van de aarde bedekt. Deze ijsmassa's bevatten ongeveer 1,74% van het water in de aardkorst. Aan de andere kant bevat ijs verschillende hoeveelheden ingesloten moleculaire zuurstof.
OFlevende organismen
De meeste moleculen waaruit de structuur van levende wezens bestaat, bevatten zuurstof. Aan de andere kant is een groot deel van de levende wezens water. Daarom is de terrestrische biomassa ook een zuurstofreserve.
Stadia
In algemene termen omvat de cyclus die zuurstof als chemisch agens volgt, twee grote gebieden die zijn karakter als biogeochemische cyclus vormen. Deze gebieden zijn vertegenwoordigd in vier fasen.
Het geomilieugebied omvat de verplaatsingen en insluiting van zuurstof in de atmosfeer, hydrosfeer, cryosfeer en geosfeer. Dit omvat het milieustadium van reservoir en bron, en het stadium van terugkeer naar het milieu..
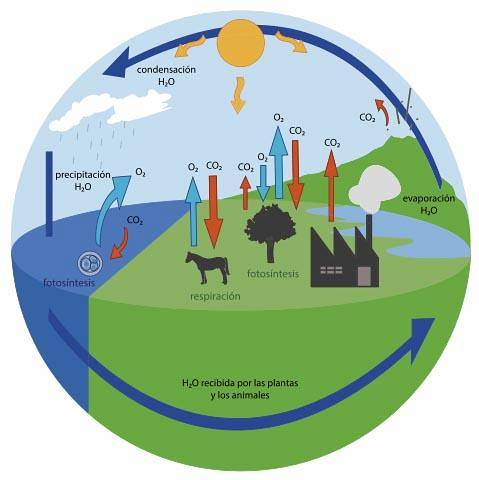
Twee fasen zijn ook opgenomen in het biologische gebied. Ze worden geassocieerd met fotosynthese en ademhaling.
-Milieutrap van reservoir en bron: atmosfeer-hydrosfeer-cryosfeer-geosfeer
Atmosfeer
De belangrijkste bron van zuurstof uit de lucht is fotosynthese. Maar er zijn andere bronnen waaruit zuurstof de atmosfeer kan binnendringen..
Een daarvan is de vloeibare buitenmantel van de aardkern. Zuurstof bereikt de atmosfeer in de vorm van waterdamp door vulkaanuitbarstingen. Waterdamp stijgt naar de stratosfeer waar het onder invloed van hoogenergetische straling van de zon fotolyse ondergaat en vrije zuurstof wordt geproduceerd..
Aan de andere kant geeft de ademhaling zuurstof af in de vorm van COtwee. Verbrandingsprocessen, vooral industriële processen, verbruiken ook moleculaire zuurstof en dragen CO bijtwee naar de atmosfeer.
Bij de uitwisseling tussen de atmosfeer en de hydrosfeer komt opgeloste zuurstof in watermassa's in de atmosfeer terecht. De COtwee Atmosferische wordt in water opgelost als koolzuur. Opgeloste zuurstof in water is voornamelijk afkomstig van de fotosynthese van algen en cyanobacteriën.
Stratosfeer
In de bovenste niveaus van de atmosfeer hydrolyseert hoogenergetische straling waterdamp. Kortegolfstraling activeert O-moleculentwee. Deze worden opgesplitst in vrije zuurstofatomen (O).
Deze vrije O-atomen reageren met O-moleculentwee en ozon produceren (O3Deze reactie is omkeerbaar. Vanwege het effect van ultraviolette straling, O3 breekt weer af in vrije zuurstofatomen.
Zuurstof als onderdeel van atmosferische lucht maakt deel uit van verschillende oxidatiereacties en wordt onderdeel van verschillende terrestrische verbindingen. Een belangrijke put voor zuurstof is de oxidatie van gassen uit vulkaanuitbarstingen..
Hydrosfeer
De grootste concentratie van water op aarde zijn de oceanen, waar sprake is van een uniforme concentratie van zuurstofisotopen. Dit komt door de constante uitwisseling van dit element met de aardkorst door middel van hydrothermische circulatieprocessen..
Aan de grenzen van de tektonische platen en de oceanische ruggen wordt een constant proces van gasuitwisseling gegenereerd.
Cryosphere
Landijsmassa's, waaronder poolijsmassa's, gletsjers en permafrost, zijn een belangrijke put voor zuurstof in de vorm van vast water..
Geosfeer
Evenzo neemt zuurstof deel aan de gasuitwisseling met de bodem. Daar vormt het het vitale element voor de ademhalingsprocessen van bodemmicro-organismen..
Een belangrijke put in de bodem zijn de processen van minerale oxidatie en het verbranden van fossiele brandstoffen..
De zuurstof die deel uitmaakt van het watermolecuul (H.tweeO) volgt de watercyclus in de processen verdamping-transpiratie en condensatie-neerslag.
-Fotosynthetische fase
Fotosynthese vindt plaats in chloroplasten. Tijdens de lichte fase van fotosynthese is een reductiemiddel nodig, dat wil zeggen een bron van elektronen. Genoemd middel is in dit geval water (H.tweeOF).
Door waterstof (H) uit water te halen, zuurstof (Otwee) als afvalproduct. Water komt via de wortels vanuit de grond de plant binnen. In het geval van algen en cyanobacteriën komt het uit het aquatisch milieu.
Alle moleculaire zuurstof (Otwee) geproduceerd tijdens fotosynthese is afkomstig van het water dat in het proces wordt gebruikt. CO wordt verbruikt bij fotosynthesetwee, zonne-energie en water (H.tweeO), en zuurstof komt vrij (Otwee.
-Atmosferische terugkeerfase
De Otwee gegenereerd in fotosynthese wordt in de atmosfeer uitgestoten via huidmondjes in het geval van planten. Algen en cyanobacteriën brengen het terug naar het milieu door membraandiffusie. Evenzo retourneren ademhalingsprocessen zuurstof naar de omgeving in de vorm van kooldioxide (COtwee.
-Ademhalingsfase
Om hun vitale functies te vervullen, moeten levende organismen de chemische energie die door fotosynthese wordt gegenereerd, effectief maken. Deze energie wordt bij planten opgeslagen in de vorm van complexe koolhydraatmoleculen (suikers). De rest van de organismen halen het uit de voeding
Het proces waarbij levende wezens chemische verbindingen ontvouwen om de vereiste energie vrij te maken, wordt ademhaling genoemd. Dit proces vindt plaats in cellen en kent twee fasen; één aëroob en één anaëroob.
Aërobe ademhaling vindt plaats in de mitochondriën bij planten en dieren. Bij bacteriën wordt het uitgevoerd in het cytoplasma, omdat ze mitochondriën missen.
Het fundamentele element voor ademhaling is zuurstof als oxidatiemiddel. Ademhaling verbruikt zuurstof (Otwee) en CO komt vrijtwee en water (H.tweeO), waardoor nuttige energie wordt geproduceerd.
De COtwee en water (waterdamp) komt vrij via huidmondjes in planten. Bij dieren COtwee het wordt vrijgegeven door de neusgaten en / of de mond, en het water door transpiratie. In algen en bacteriën COtwee wordt vrijgegeven door membraandiffusie.
Fotorespiratie
In planten ontwikkelt zich in aanwezigheid van licht een proces dat zuurstof en energie verbruikt, fotorespiratie genaamd. Fotorespiratie neemt toe met toenemende temperatuur, vanwege de toename van de CO-concentratie.twee met betrekking tot de concentratie van Otwee.
Fotorespiratie zorgt voor een negatieve energiebalans voor de plant. Consumeer Otwee en chemische energie (geproduceerd door fotosynthese) en geeft CO vrijtwee. Om deze reden hebben ze evolutionaire mechanismen ontwikkeld om het tegen te gaan (C4- en CAN-metabolisme)..
Belang
Tegenwoordig is het overgrote deel van het leven aëroob. Zonder de circulatie van Otwee in het planetaire systeem zou het leven zoals we dat nu kennen onmogelijk zijn.
Bovendien vormt zuurstof een aanzienlijk deel van de luchtmassa's op aarde. Daarom draagt het bij aan de atmosferische verschijnselen die ermee verband houden en de gevolgen ervan: erosieve effecten, klimaatregulatie, onder andere..
Het genereert rechtstreeks oxidatieprocessen in de bodem, van vulkanische gassen en op kunstmatige metalen constructies..
Zuurstof is een element met een hoog oxidatief vermogen. Hoewel zuurstofmoleculen zeer stabiel zijn omdat ze een dubbele binding vormen, omdat zuurstof een hoge elektronegativiteit heeft (vermogen om elektronen aan te trekken), heeft het een hoge reactieve capaciteit. Vanwege deze hoge elektronegativiteit grijpt zuurstof in bij veel oxidatiereacties.
Wijzigingen
De overgrote meerderheid van verbrandingsprocessen die in de natuur plaatsvinden, vereist de deelname van zuurstof. Evenzo in die gegenereerd door de mens. Deze processen vervullen in antropische termen zowel positieve als negatieve functies.
Het verbranden van fossiele brandstoffen (steenkool, olie, gas) draagt bij aan de economische ontwikkeling, maar vormt tegelijkertijd een ernstig probleem vanwege zijn bijdrage aan de opwarming van de aarde.
Grote bosbranden tasten de biodiversiteit aan, hoewel ze in sommige gevallen deel uitmaken van natuurlijke processen in bepaalde ecosystemen.
Broeikaseffect
De ozonlaag (O3) in de stratosfeer, is het beschermende schild van de atmosfeer tegen het binnendringen van overtollige ultraviolette straling. Deze zeer energetische straling verhoogt de opwarming van de aarde.
Aan de andere kant is het sterk mutageen en schadelijk voor levende weefsels. Bij mensen en andere dieren is het kankerverwekkend.
De emissie van verschillende gassen veroorzaakt de vernietiging van de ozonlaag en vergemakkelijkt daardoor het binnendringen van ultraviolette straling. Sommige van deze gassen zijn chloorfluorkoolwaterstoffen, chloorfluorkoolwaterstoffen, ethylbromide, stikstofoxiden uit meststoffen en halonen..
Referenties
- Anbar AD, Y Duan, TW Lyons, GL Arnold, B Kendall, RA Creaser, AJ Kaufman, WG Gordon, S Clinton, J Garvin en R Buick (2007) A Whiff of Oxygen Before the Great Oxidation Event? Science 317: 1903-1906.
- Bekker A, HD Holland, PL Wang, D Rumble, HJ Stein, JL Hannah, LL Coetzee en NJ Beukes. (2004) Dateren van de opkomst van zuurstof uit de lucht. Nature 427: 117-120.
- Farquhar J en DT Johnston. (2008) De zuurstofcyclus van de aardse planeten: inzichten in de verwerking en geschiedenis van zuurstof in oppervlakte-omgevingen. Recensies in mineralogie en geochemie 68: 463-492.
- Keeling RF (1995) De atmosferische zuurstofcyclus: de zuurstofisotopen van atmosferische COtwee en Otwee en de Otwee/ Ntwee Reviws of Geophysics, aanvulling. VS: Nationaal rapport aan International Union of Geodesy and Geophysics 1991-1994. pp. 1253-1262.
- Purves WK, D Sadava, GH Orians en HC Heller (2003) Life. The Science of Biology. 6e edt. Sinauer Associates, Inc. en WH Freeman and Company. 1044 blz.



Niemand heeft nog op dit artikel gereageerd.