
Kenmerken, typen en nomenclatuur van glycosidebinding
De glycosidebindingen Het zijn de covalente bindingen die voorkomen tussen suikers (koolhydraten) en andere moleculen, die andere monosacchariden of andere moleculen van diverse aard kunnen zijn. Deze verbindingen maken het bestaan van meerdere fundamentele componenten voor het leven mogelijk, niet alleen bij de vorming van reservebrandstoffen en structurele elementen, maar ook bij informatiedragende moleculen die essentieel zijn voor cellulaire communicatie..
De vorming van polysacchariden hangt fundamenteel af van het tot stand brengen van glycosidebindingen tussen de vrije alcohol- of hydroxylgroepen van de individuele monosaccharide-eenheden..
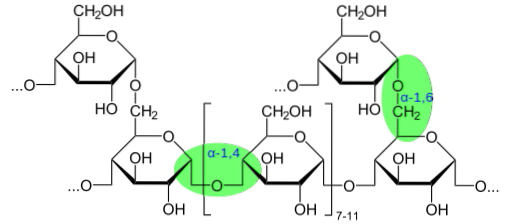
Sommige complexe polysacchariden bevatten echter gemodificeerde suikers die via glucosidebindingen aan kleine moleculen of groepen zoals amino, sulfaat en acetyl zijn gehecht en die niet noodzakelijkerwijs de afgifte van een watermolecuul door een condensatiereactie met zich meebrengen. Deze modificaties komen zeer vaak voor in de glycanen die aanwezig zijn in de extracellulaire matrix of glycocalyx..
Glycosidebindingen komen voor in meerdere cellulaire contexten, waaronder de vereniging van de polaire kopgroep van sommige sfingolipiden, essentiële bestanddelen van de celmembranen van veel organismen en de vorming van glycoproteïnen en proteoglycanen..
Belangrijke polysacchariden zoals cellulose, chitine, agar, glycogeen en zetmeel zouden niet mogelijk zijn zonder glycosidebindingen. Evenzo is eiwitglycosylering, die optreedt in het endoplasmatisch reticulum en in het Golgi-complex, van het grootste belang voor de activiteit van veel eiwitten..
Talrijke oligo- en polysacchariden fungeren als glucosereservoirs, als structurele componenten of als kleefstoffen voor celhechting in weefsels..
De relatie tussen glycosidebindingen in oligosacchariden is analoog aan die van peptidebindingen in polypeptiden en fosfodiësterbindingen in polynucleotiden, met het verschil dat er een grotere diversiteit is in glycosidebindingen..
Artikel index
- 1 Kenmerken
- 1.1 Vorming van de glycosidebinding
- 1.2 Hydrolyse van de glycosidebinding
- 1.3 Diversiteit
- 2 soorten
- 2.1 O-glucosidebindingen
- 2.2 N-glucosidebindingen
- 2.3 Andere soorten glycosidebindingen
- 3 Nomenclatuur
- 4 referenties
Kenmerken
Glycosidebindingen zijn veel gevarieerder dan hun analogen in eiwitten en nucleïnezuren, omdat in principe twee suikermoleculen op veel manieren met elkaar kunnen verbinden, omdat ze meerdere -OH-groepen hebben die kunnen deelnemen aan de vorming van de link..
Bovendien bieden de isomeren van monosacchariden, dat wil zeggen een van de twee oriëntaties die de hydroxylgroep kan hebben in de cyclische structuur ten opzichte van de anomere koolstof, een extra niveau van diversiteit..
Isomeren hebben verschillende driedimensionale structuren, evenals verschillende biologische activiteiten. Cellulose en glycogeen bestaan uit zich herhalende D-glucose-eenheden, maar verschillen in het type glycosidebinding (α1-4 voor glycogeen en β1-4 voor cellulose) en hebben daarom verschillende eigenschappen en functies..
Net zoals polypeptiden een polariteit hebben met een N- en een C-uiteinde, en polynucleotiden 5'- en 3'-uiteinden hebben, hebben oligo- of polysacchariden een polariteit die wordt bepaald door de reducerende en niet-reducerende uiteinden..
Het reducerende uiteinde heeft een vrij anomeer centrum dat geen glycosidebinding vormt met een ander molecuul, waardoor de chemische reactiviteit van het aldehyde behouden blijft.
De glycosidebinding is het meest flexibele gebied van een oligo- of polysaccharidegroep, aangezien de structurele zadelconformatie van individuele monosacchariden relatief star is..
Vorming van de glycosidebinding
De glycosidebinding kan twee monosaccharidemoleculen verbinden via de anomere koolstof van de ene en de hydroxylgroep van de andere. Dat wil zeggen, de hemiacetaalgroep van de ene suiker reageert met de alcoholgroep van een andere om een acetaal te vormen.
Over het algemeen vindt de vorming van deze bindingen plaats door condensatiereacties, waarbij een watermolecuul vrijkomt bij elke binding die wordt gevormd..
Bij sommige reacties verlaat zuurstof het suikermolecuul echter niet als water, maar als onderdeel van de difosfaatgroep van een uridinedifosfaatnucleotide..
De reacties die aanleiding geven tot de glycosidebindingen worden gekatalyseerd door een klasse van enzymen die bekend staan als glycosyltransferasen. Ze worden gevormd tussen een covalent gemodificeerde suiker door de toevoeging van een fosfaatgroep of een nucleotide (bijvoorbeeld glucose-6-fosfaat, UDP-galactose) dat zich bindt aan de groeiende polymeerketen..
Hydrolyse van de glycosidebinding
Glycosidebindingen kunnen gemakkelijk worden gehydrolyseerd in licht zure omgevingen, maar ze zijn redelijk resistent tegen alkalische omgevingen..
De enzymatische hydrolyse van de glycosidebindingen wordt gemedieerd door enzymen die bekend staan als glycosidasen. Veel zoogdieren hebben deze enzymen niet voor de afbraak van cellulose, dus ze zijn niet in staat om energie uit dit polysaccharide te halen, ondanks dat het een essentiële bron van vezels is..
Herkauwers zoals koeien hebben bijvoorbeeld bacteriën in hun darmen die enzymen produceren die de cellulose die ze binnenkrijgen kunnen afbreken, waardoor ze kunnen profiteren van de energie die in plantenweefsels wordt bewaard..
Het enzym lysozym, geproduceerd in de tranen van het oog en door sommige bacteriële virussen, kan bacteriën vernietigen dankzij zijn hydrolytische activiteit, die de glycosidebinding verbreekt tussen N-acetylglucosamine en N-acetylmuraminezuur in de celwand van bacteriën..
Diversiteit
Oligosacchariden, polysacchariden of glycanen zijn zeer diverse moleculen en dit komt door de vele manieren waarop monosacchariden aan elkaar kunnen binden om structuren van hogere orde te vormen..
Deze diversiteit is gebaseerd op het feit, zoals hierboven vermeld, dat suikers hydroxylgroepen hebben die verschillende bindingsgebieden mogelijk maken, en dat er bindingen kunnen ontstaan tussen de twee mogelijke stereo-isomeren met betrekking tot de anomere koolstof van de suiker (α of β)..
Glycosidebindingen kunnen worden gevormd tussen een suiker en elke hydroxyverbinding zoals alcoholen of aminozuren.
Bovendien kan een monosaccharide twee glycosidebindingen vormen, zodat het kan dienen als een vertakkingspunt, waardoor potentiële complexiteit in de structuur van glycanen of polysacchariden in cellen wordt geïntroduceerd..
Types
Wat de soorten glycosidebindingen betreft, kunnen twee categorieën worden onderscheiden: de glycosidebindingen tussen monosacchariden die oligo- en polysacchariden vormen, en de glycosidebindingen die voorkomen in glycoproteïnen of glycolipiden, dit zijn eiwitten of lipiden met porties koolhydraten..
O-glucosidebindingen
O-glycosidebindingen komen voor tussen monosacchariden, ze worden gevormd door de reactie tussen de hydroxylgroep van het ene suikermolecuul en het anomere koolstofatoom van een ander.
Disachariden zijn een van de meest voorkomende oligosachariden. Polysacchariden hebben meer dan 20 monosaccharide-eenheden die lineair met elkaar zijn verbonden en hebben soms meerdere vertakkingen..
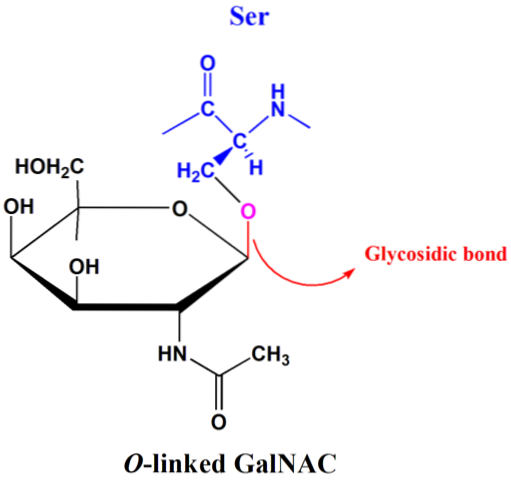
In disacchariden zoals maltose, lactose en sucrose is de meest voorkomende glycosidebinding het O-glucosidetype. Deze bindingen kunnen voorkomen tussen de koolstofatomen en -OH van de α- of β-isomere vormen..
De vorming van de glucosidebindingen in oligo- en polysacchariden zal afhangen van de stereochemische aard van de suikers die worden samengevoegd, evenals van hun aantal koolstofatomen. Over het algemeen treden bij suikers met 6 koolstofatomen lineaire bindingen op tussen koolstofatomen 1 en 4 of 1 en 6.
Er zijn twee hoofdtypen O-glycosiden die, afhankelijk van de nomenclatuur, worden gedefinieerd als α en β of 1,2-cis en 1.2-trans-glycosiden.
Residuen 1,2-cis geglycosyleerde a-glycosiden voor D-glucose, D-galactose, L-fucose, D-xylose of P-glycosiden voor D-mannose, L-arabinose; evenals de 1,2-trans (β-glycosiden voor D-glucose, D-galactose en α-glycosiden voor D-mannose, etc.), zijn van groot belang voor veel natuurlijke componenten.
O-glycosylering
Een van de meest voorkomende posttranslationele modificaties is glycosylering, die bestaat uit de toevoeging van een koolhydraatgedeelte aan een groeiend peptide of eiwit. Mucines, secretoire eiwitten, kunnen grote hoeveelheden oligosaccharideketens bevatten die zijn verbonden door O-glucosidebindingen..
Het O-glycosyleringsproces vindt plaats in het Golgi-complex van eukaryoten en bestaat uit de binding van eiwitten aan het koolhydraatgedeelte door een glycosidebinding tussen de -OH-groep van een aminozuurresidu van serine of threonine en de anomere koolstof. Van suiker..
De vorming van deze bindingen tussen koolhydraten en hydroxyproline- en hydroxylysineresiduen en met de fenolgroep van tyrosineresiduen is ook waargenomen..
N-glycosidebindingen
N-glycosidebindingen zijn de meest voorkomende onder geglycosyleerde eiwitten. N-glycosylering vindt voornamelijk plaats in het endoplasmatisch reticulum van eukaryoten, met daaropvolgende modificaties die kunnen optreden in het Golgi-complex.
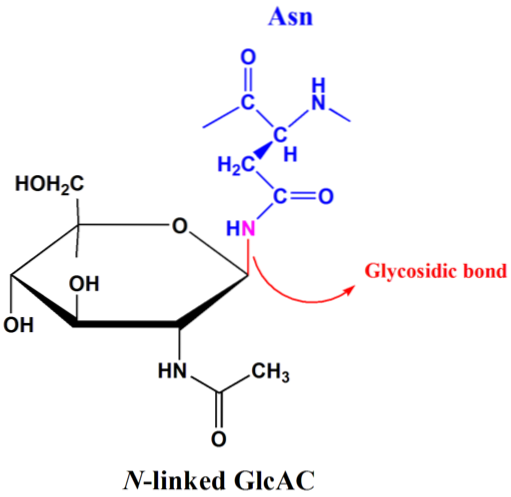
N-glycosylering hangt af van de aanwezigheid van de consensussequentie Asn-Xxx-Ser / Thr. De glycosidebinding vindt plaats tussen de amidestikstof van de zijketen van de asparagineresiduen en de anomere koolstof van de suiker die aan de peptideketen bindt..
De vorming van deze bindingen tijdens glycosylering hangt af van een enzym dat bekend staat als oligosacaryltransferase, dat de oligosacchariden van een dolicholfosfaat naar de amidestikstof van de asparagineresiduen overbrengt..
Andere soorten glycosidebindingen
S-glucosidebindingen
Ze komen ook voor tussen eiwitten en koolhydraten, ze zijn waargenomen tussen peptiden met N-terminale cysteïnen en oligosacchariden. Peptiden met dit type koppeling werden aanvankelijk geïsoleerd uit eiwitten in menselijke urine en erytrocyten gebonden aan glucose-oligosachariden..
C-glucosidebindingen
Ze werden voor het eerst waargenomen als een posttranslationele modificatie (glycosylering) in een tryptofaanresidu in RNase 2 aanwezig in menselijke urine en in RNase 2 van erytrocyten. Een mannose bindt zich aan de koolstof op positie 2 van de indoolkern van het aminozuur via een C-glucosidebinding.
Nomenclatuur
De term glycoside wordt gebruikt om elke suiker te beschrijven waarvan de anomere groep is vervangen door een groep -OR (O-glycosiden), -SR (thioglycosiden), -SeR (selenoglycosiden), -NR (N-glycosiden of glucosaminen) of zelfs -CR (C-glucosiden).
Ze kunnen op drie verschillende manieren een naam krijgen:
(1) de terminale "-o" van de naam van de overeenkomstige cyclische vorm van de monosaccharide te vervangen door "-ido" en alvorens, als een ander woord, de naam van de substituent R-groep te schrijven.
(2) het gebruik van de term "glycosyloxy" als voorvoegsel van de monosaccharidenaam.
(3) de term gebruiken OF-glycosyl, N-glycosyl, S-glycosyl of C-glycosyl als voorvoegsel voor de naam van de hydroxyverbinding.
Referenties
- Bertozzi, C. R., en Rabuka, D. (2009). Structurele basis van glycaan-diversiteit. In A. Varki, R. Cummings en J. Esko (Eds.), Essentials of Glycobiology (2e ed.). New York: Cold Spring Harbor Laboratory Press. Opgehaald van www.ncbi.nlm.nih.gov
- Biermann, C. (1988). Hydrolyse en andere splitsingen van glycosidebindingen in polysacchariden. Vooruitgang in koolhydraatchemie en biochemie, 46, 251-261.
- Demchenko, A. V. (2008). Handbook of Chemical Glycosylation: Advances in Stereoselectivity and Therapeutic Relevance. Wiley-VCH.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H.,… Martin, K. (2003). Moleculaire celbiologie (5e ed.). Freeman, W. H. & Company.
- Nelson, D. L., en Cox, M. M. (2009). Lehninger-principes van biochemie. Omega-edities (5e ed.).
- Nomenclatuur van koolhydraten (aanbevelingen 1996). (1996). Opgehaald van www.qmul.ac.uk
- Soderberg, T. (2010). Organische chemie met een biologische nadruk, deel I. Scheikunde Faculteit (Deel 1). Minnesota: Morris Digital Well van de Universiteit van Minnesota. Opgehaald van www.digitalcommons.morris.umn.edu
- Taylor, C. M. (1998). Glycopeptiden en glycoproteïnen: focus op de glycosidische koppeling. Tetraëder, 54, 11317-11362.


Niemand heeft nog op dit artikel gereageerd.