
Fosfatidylethanolamine structuur, biosynthese en functies
De fosfatidylethanolamine (PE) is een glycerofosfolipide dat overvloedig voorkomt in de plasmamembranen van prokaryote organismen. Integendeel, in eukaryote celmembranen is dit na fosfatidylcholine het tweede meest voorkomende glycerofosfolipide aan de binnenkant van het plasmamembraan..
Ondanks de overvloed aan fosfatidylethanolamine, hangt de overvloed ervan niet alleen af van het celtype, maar ook van het compartiment en het moment van de specifieke beschouwde levenscyclus van de cel..
Biologische membranen zijn barrières die cellulaire organismen definiëren. Ze hebben niet alleen beschermings- en isolatiefuncties, maar ze zijn ook de sleutel tot de vorming van eiwitten die een hydrofobe omgeving nodig hebben voor hun optimale werking..
Zowel eukaryoten als prokaryoten hebben membranen die voornamelijk zijn samengesteld uit glycerofosfolipiden en in mindere mate uit sfingolipiden en sterolen..
Glycerofosfolipiden zijn amfipatische moleculen die zijn gestructureerd op een L-glycerol-ruggengraat die op de sn-1- en sn-2-posities is veresterd door twee vetzuren van verschillende lengte en verzadigingsgraad. In de hydroxyl van de sn-3-positie wordt het veresterd door een fosfaatgroep, waaraan op hun beurt verschillende soorten moleculen kunnen worden gehecht die aanleiding geven tot de verschillende klassen van glycerofosfolipiden..
In de cellulaire wereld is er een grote verscheidenheid aan glycerofosfolipiden, maar de meest voorkomende zijn fosfatidylcholine (PC), fosfatidylethanolamine (PE), fosfatidylserine (PS), fosfatidylinositol (PI), fosfatidinezuur (PA), fosfatidylglycerol (PG) en cardiolipine (CL).
Artikel index
- 1 Structuur
- 2 Biosynthese
- 2.1 Kennedy-route
- 2.2 PSD-pad
- 3 functies
- 4 referenties
Structuur
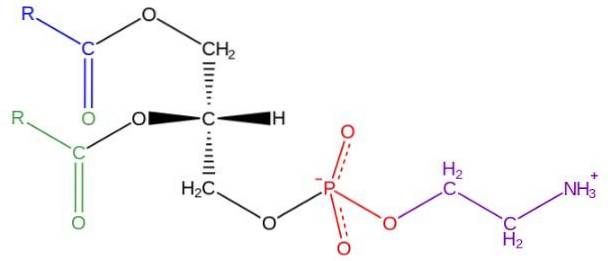
De structuur van fosfatidylethanolamine werd ontdekt door Baer et al. In 1952. Zoals experimenteel is bepaald voor alle glycerofosfolipiden, wordt fosfatidylethanolamine gevormd door een glycerolmolecuul dat op de sn-1- en sn-2-posities veresterd is met vetachtige zuurketens met tussen 16 en 20. koolstofatomen.
De vetzuren veresterd in de sn-1 hydroxylgroep zijn over het algemeen verzadigd (zonder dubbele bindingen) met maximale lengtes van 18 koolstofatomen, terwijl de ketens die verbonden zijn in de sn-2 positie langer zijn en met een of meer onverzadigingen (dubbele bindingen).
De mate van verzadiging van deze ketens draagt bij aan de elasticiteit van het membraan, wat een grote invloed heeft op het inbrengen en vastleggen van eiwitten in de dubbellaag..
Fosfatidylethanolamine wordt beschouwd als een niet-lamellaire glycerofosfolipide, omdat het een conische geometrische vorm heeft. Deze vorm wordt gegeven door de kleine omvang van de polaire groep of "kop", in verhouding tot die van de vetzuurketens die de hydrofobe "staarten" vormen..
De "kop" of polaire groep van fosfatidylethanolamine heeft een zwitterionisch karakter, dat wil zeggen, het heeft groepen die onder bepaalde pH-omstandigheden positief en negatief geladen kunnen worden..
Door deze eigenschap kan het waterstof binden met een groot aantal aminozuurresiduen en de ladingsverdeling ervan is een essentiële bepalende factor voor de domeintopologie van veel integrale membraaneiwitten..
Biosynthese
In eukaryote cellen is de synthese van structurele lipiden geografisch beperkt, waarbij de belangrijkste biosynthese-plaats het endoplasmatisch reticulum (ER) en in mindere mate het Golgi-apparaat is..
Er zijn vier onafhankelijke biosynthetische routes voor de productie van fosfatidylethanolamine: (1) de CDP-ethanolamine-route, ook bekend als de Kennedy-route; (2) de PSD-route voor decarboxylering van fosfatidylserine (PS); (3) acylering van lyso-PE en (4) baseveranderingsreacties van de polaire groep van andere glycerofosfolipiden.
Kennedy-route
De biosynthese van fosfatidylethanolamine via deze route is beperkt tot ER en er is aangetoond dat dit in hamsterlevercellen de belangrijkste productieroute is. Het bestaat uit drie opeenvolgende enzymatische stappen die worden gekatalyseerd door drie verschillende enzymen.
In de eerste stap worden fosfoethanolamine en ADP geproduceerd dankzij de werking van ethanolaminekinase, dat de ATP-afhankelijke fosforylering van ethanolamine katalyseert..
In tegenstelling tot planten zijn noch zoogdieren, noch gisten in staat om dit substraat te produceren, dus het moet in de voeding worden geconsumeerd of worden verkregen uit de afbraak van reeds bestaande fosfatidylethanolamine- of sfingosinemoleculen..
Fosfoethanolamine wordt gebruikt door CTP: fosfoethanolamine cytidyltransferase (ET) om de hoogenergetische verbinding CDP te vormen: ethanolamine en een anorganisch fosfaat.
1,2-diacylglycerol ethanolamine fosfotransferase (ETP) gebruikt de energie die in de CDP-ethanolamine binding zit om ethanolamine covalent te binden aan een membraan-ingebracht diacylglycerol molecuul, waardoor fosfatidylethanolamine ontstaat..
Route PSD
Deze route werkt zowel bij prokaryoten als bij gisten en zoogdieren. Bij bacteriën komt het voor in het plasmamembraan, maar bij eukaryoten komt het voor in een gebied van het endoplasmatisch reticulum dat nauw verwant is aan het mitochondriale membraan..
Bij zoogdieren wordt de route gekatalyseerd door een enkel enzym, fosfatidylserinedecarboxylase (PSD1p), dat is ingebed in het mitochondriale membraan, waarvan het gen wordt gecodeerd door de kern. De reactie omvat decarboxylering van PS tot fosfatidylethanolamine.
De overige twee routes (PE-lyso-acylering en polaire groepsafhankelijke calciumuitwisseling) vinden plaats in het endoplasmatisch reticulum, maar dragen niet significant bij aan de totale productie van fosfatidylethanolamine in eukaryote cellen..
Kenmerken
Glycerofosfolipiden hebben drie hoofdfuncties in de cel, waaronder de structurele functies, energieopslag en celsignalering..
Fosfatidylethanolamine wordt geassocieerd met de verankering, stabilisatie en vouwing van meerdere membraaneiwitten, evenals de conformatieveranderingen die nodig zijn voor het functioneren van veel enzymen.
Er is experimenteel bewijs dat fosfatidylethanolamine voorstelt als een cruciaal glycerofosfolipide in het late stadium van telofase, tijdens de vorming van de contractiele ring en de vorming van de fragmoplast die de deling van het membraan van de twee dochtercellen mogelijk maakt..
Het speelt ook een belangrijke rol in alle processen van fusie en splitsing (vereniging en scheiding) van de membranen van zowel het endoplasmatisch reticulum als het Golgi-apparaat..
In E. coli is aangetoond dat fosfatidylethanolamine nodig is voor de juiste vouwing en functie van het enzym lactose permease, en daarom is gesuggereerd dat het een rol speelt als moleculaire 'chaperonne'..
Fosfatidylethanolamine is de belangrijkste donor van het ethanolaminemolecuul dat nodig is voor posttranslationele modificatie van talrijke eiwitten, zoals GPI-ankers.
Dit glycerofosfolipide is de voorloper van talrijke moleculen met enzymatische activiteit. Bovendien kunnen moleculen die zijn afgeleid van het metabolisme, evenals diacylglycerol, fosfatidinezuur en sommige vetzuren, fungeren als tweede boodschappers. Bovendien is het een belangrijk substraat voor de productie van fosfatidylcholine..
Referenties
- Brouwers, J. F. H. M., Vernooij, E. A. A. M., Tielens, A. G. M., & van Golde, L. M. G. (1999). Snelle scheiding en identificatie van moleculaire fosfatidylethanolamine-soorten. Journal of Lipid Research, 40 (1), 164-169. Opgehaald van jlr.org
- Calzada, E., McCaffery, J. M., & Claypool, S. M. (2018). Fosfatidylethanolamine geproduceerd in het binnenste mitochondriale membraan is essentieel voor gistcytochroom bc1 complexe functie 3. BioRxiv, 1, 46.
- Calzada, E., Onguka, O., & Claypool, S. M. (2016). Fosfatidylethanolamine metabolisme bij gezondheid en ziekte. International Review of Cell and Molecular Biology (deel 321). Elsevier Inc..
- Gibellini, F., en Smith, T. K. (2010). De Kennedy-de novo-synthese van fosfatidylethanolamine en fosfatidylcholine. IUBMB Life, 62 (6), 414-428.
- Harayama, T., en Riezman, H. (2018). Inzicht in de diversiteit van de samenstelling van membraanlipiden. Nature Reviews Molecular Cell Biology, 19 (5), 281-296.
- Luckey, M. (2008). Membraan structurele biologie: met biochemische en biofysische grondslagen. Cambrudge University Press. Opgehaald van cambrudge.org
- Seddon, J. M., Cevc, G., Kaye, R. D., & Marsh, D. (1984). Röntgendiffractiestudie van het polymorfisme van gehydrateerde diacyl- en dialkylfosfatidylethanolaminen. Biochemistry, 23 (12), 2634-2644.
- Sendecki, A. M., Poyton, M. F., Baxter, A. J., Yang, T., & Cremer, P. S. (2017). Ondersteunde lipide-dubbellagen met fosfatidylethanolamine als de belangrijkste component. Langmuir, 33 (46), 13423-13429.
- van Meer, G., Voelker, D. R., & Feignenson, G. W. (2008). Membraanlipiden: waar ze zijn en hoe ze zich gedragen. Nature beoordelingen, 9, 112-124.
- Vance, J. E. (2003). Moleculaire en celbiologie van het metabolisme van fosfatidylserine en fosfatidylethanolamine. In K. Moldave (Ed.), Progress Nucleic Acid Research and Molecular Biology (pp. 69-111). Academische pers.
- Vance, J. E. (2008). Fosfatidylserine en fosfatidylethanolamine in zoogdiercellen: twee metabolisch verwante aminofosfolipiden. Journal of Lipid Research, 49 (7), 1377-1387.
- Vance, J. E., en Tasseva, G. (2013). Vorming en functie van fosfatidylserine en fosfatidylethanolamine in zoogdiercellen. Biochimica et Biophysica Acta - Moleculaire en celbiologie van lipiden, 1831 (3), 543-554.
- Watkins, S. M., Zhu, X., & Zeisel, S. H. (2003). Fosfatidylethanolamine-N-methyltransferase-activiteit en choline in de voeding reguleren de lipidenflux in het leverplasma en het metabolisme van essentiële vetzuren bij muizen. The Journal of Nutrition, 133 (11), 3386-3391.



Niemand heeft nog op dit artikel gereageerd.