
Anaërobe glycolysereacties en fermentatiereacties
De anaërobe glycolyse of anaëroob is een katabole route die door veel soorten cellen wordt gebruikt voor de afbraak van glucose bij afwezigheid van zuurstof. Dat wil zeggen, glucose wordt niet volledig geoxideerd tot kooldioxide en water, zoals het geval is bij aërobe glycolyse, maar er worden fermentatieve producten gegenereerd..
Het wordt anaërobe glycolyse genoemd omdat het plaatsvindt zonder de aanwezigheid van zuurstof, dat in andere gevallen fungeert als een laatste elektronenacceptor in de mitochondriale transportketen, waar grote hoeveelheden energie worden geproduceerd door de verwerking van glycolytische producten..
Afhankelijk van het organisme zal een toestand van anaerobiose of afwezigheid van zuurstof resulteren in de productie van melkzuur (bijvoorbeeld spiercellen) of ethanol (gist), uit het pyruvaat dat wordt gegenereerd door de afbraak van glucose..
Als gevolg hiervan daalt de energieopbrengst drastisch, aangezien er slechts twee mol ATP wordt geproduceerd voor elke mol glucose die wordt verwerkt, vergeleken met de 8 mol die kunnen worden verkregen tijdens aërobe glycolyse (alleen in de glycolytische fase)..
Het verschil in het aantal ATP-moleculen heeft te maken met de heroxidatie van NADH, die geen extra ATP genereert, in tegenstelling tot wat er gebeurt bij aërobe glycolyse, waarbij voor elke NADH 3 ATP-moleculen worden verkregen..
Artikel index
- 1 Reacties
- 2 fermentatieroutes
- 2.1 Melkzuurproductie
- 2.2 Ethanolproductie
- 3 Aërobe fermentatie
- 4 Glycolyse en kanker
- 5 referenties
Reacties
Anaërobe glycolyse verschilt helemaal niet van aërobe glycolyse, aangezien de term "anaëroob" eerder verwijst naar wat er gebeurt na de glycolytische route, dat wil zeggen naar het lot van de reactieproducten en tussenproducten..
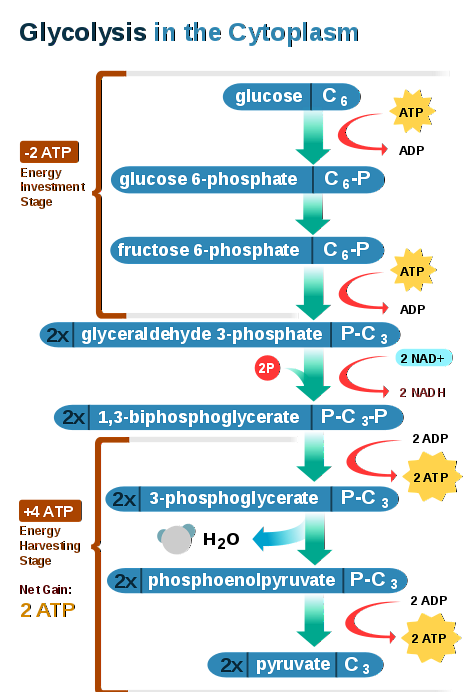
Er zijn dus tien verschillende enzymen betrokken bij anaërobe glycolysereacties, namelijk:
1-hexokinase (HK): gebruikt één ATP-molecuul voor elk glucosemolecuul. Het produceert glucose-6-fosfaat (G6P) en ADP. De reactie is onomkeerbaar en vereist magnesiumionen.
2-fosfoglucose-isomerase (PGI): isomeriseert G6P tot fructose-6-fosfaat (F6P).
3-Phosphofructokinase (PFK): fosforyleert F6P tot fructose 1,6-bisfosfaat (F1,6-BP) met behulp van één ATP-molecuul voor elke F6P, deze reactie is ook onomkeerbaar.
4-Aldolase: splitst het F1,6-BP-molecuul en produceert glyceraldehyde 3-fosfaat (GAP) en dihydroxyacetonfosfaat (DHAP).
5-Triosefosfaatisomerase (TIM): neemt deel aan de onderlinge omzetting van DHAP en GAP.
6-glyceraldehyde 3-fosfaat dehydrogenase (GAPDH): gebruikt twee moleculen van NAD+ en 2 moleculen anorganisch fosfaat (Pi) om GAP te fosforyleren, levert 1,3-bisfosfoglyceraat (1,3-BPG) en 2 NADH op.
7-fosfoglyceraatkinase (PGK): produceert twee ATP-moleculen door fosforylering op het substraatniveau van twee ADP-moleculen. Het gebruikt als fosfaatgroepdonor elk 1,3-BPG-molecuul. Produceert 2 moleculen 3-fosfoglyceraat (3PG).
8-fosfoglyceraatmutase (PGM): herschikt het 3PG-molecuul om een tussenproduct met hogere energie te produceren, 2PG.
9-Enolase: van 2PG produceert fosfoenolpyruvaat (PEP) door uitdroging van de eerste.
10-pyruvaatkinase (PYK): fosfoenolpyruvaat wordt door dit enzym gebruikt om pyruvaat te vormen. De reactie omvat de overdracht van de fosfaatgroep op positie 2 van fosfoenolpyruvaat naar een ADP-molecuul. Voor elke glucose worden 2 pyruvaten en 2 ATP geproduceerd.
Fermentatieroutes
Fermentatie is de term die wordt gebruikt om aan te geven dat glucose of andere voedingsstoffen worden afgebroken in afwezigheid van zuurstof, om energie te verkrijgen.
Bij afwezigheid van zuurstof heeft de elektronentransportketen geen uiteindelijke acceptor en daarom vindt geen oxidatieve fosforylering plaats, wat grote hoeveelheden energie in de vorm van ATP oplevert. NADH wordt niet opnieuw geoxideerd door de mitochondriale route, maar door alternatieve routes, die geen ATP produceren.
Niet genoeg NAD+ de glycolytische route wordt gestopt, aangezien de overdracht van fosfaat naar GAP een gelijktijdige reductie van deze cofactor vereist.
Sommige cellen hebben alternatieve mechanismen om met perioden van anaerobiose om te gaan, en in het algemeen behelzen deze mechanismen een of andere vorm van fermentatie. Andere cellen daarentegen zijn voor hun levensonderhoud vrijwel uitsluitend afhankelijk van fermentatieve processen..
De producten van de fermentatieroutes van veel organismen zijn economisch relevant voor de mens; Voorbeelden zijn de productie van ethanol door sommige anaërobe gisten en de vorming van melkzuur door de lactobacteriën die worden gebruikt voor de productie van yoghurt..
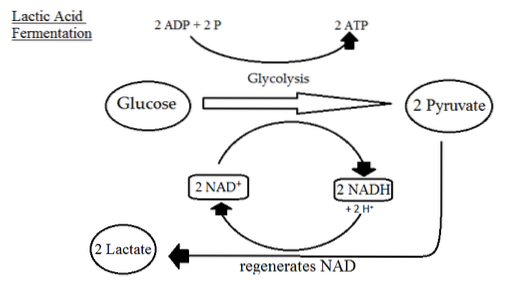
Melkzuurproductie
Veel celtypen produceren in afwezigheid van zuurstof melkzuur dankzij de reactie die wordt gekatalyseerd door het lactaatdehydrogenasecomplex, dat gebruikmaakt van de koolstofatomen van pyruvaat en het NADH geproduceerd in de GAPDH-reactie..
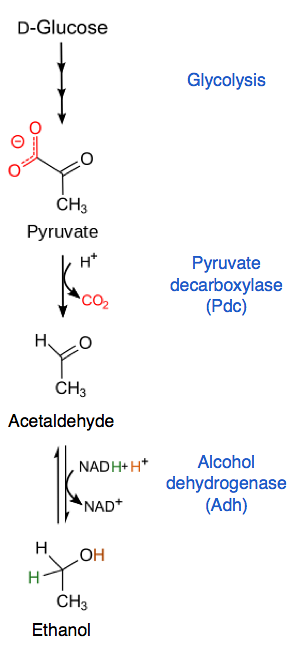
Ethanol productie
Pyruvaat wordt door pyruvaatdecarboxylase omgezet in aceetaldehyde en CO2. Acetaldehyde wordt vervolgens gebruikt door alcoholdehydrogenase, die het vermindert, ethanol produceert en een molecuul NAD regenereert.+ voor elk pyruvaatmolecuul dat op deze manier binnenkomt.
Aërobe gisting
Anaërobe glycolyse heeft als belangrijkste kenmerk dat de eindproducten niet overeenkomen met COtwee en water, zoals in het geval van aërobe glycolyse. In plaats daarvan worden typische producten van fermentatiereacties gegenereerd.
Sommige auteurs hebben een proces beschreven van "aërobe fermentatie" of aërobe glycolyse van glucose voor bepaalde organismen, waaronder enkele parasieten van de Trypanosomatidae-familie en veel kankertumorcellen..
Bij deze organismen is aangetoond dat zelfs in de aanwezigheid van zuurstof de producten van de glycolytische route overeenkomen met de producten van fermentatieroutes, en daarom wordt aangenomen dat er een 'gedeeltelijke' oxidatie van glucose plaatsvindt, aangezien niet alle energie geëxtraheerd mogelijk van zijn koolstofatomen.
Hoewel de "aërobe fermentatie" van glucose niet de totale afwezigheid van ademhalingsactiviteit impliceert, aangezien het niet een alles of niets proces is. De literatuur geeft echter de uitscheiding aan van producten zoals pyruvaat, lactaat, succinaat, malaat en andere organische zuren..
Glycolyse en kanker
Veel kankercellen vertonen een verhoogde opname van glucose en glycolytische doorstroming.
Tumoren bij kankerpatiënten groeien snel, dus de bloedvaten zijn hypoxisch. Het energiesupplement van deze cellen hangt dus voornamelijk af van anaërobe glycolyse..
Dit fenomeen wordt echter ondersteund door een hypoxie-induceerbare transcriptiefactor (HIF), die de expressie van glycolytische enzymen en glucosetransporters in het membraan verhoogt via complexe mechanismen..
Referenties
- Akram, M. (2013). Minireview over glycolyse en kanker. J. Canc. Educ., 28, 454-457.
- Bustamante, E., & Pedersen, P. (1977). Hoge aërobe glycolyse van hepatoomcellen van ratten in kweek: rol van mitochondriale hexokinase. Proc. Natl. Acad. Sci., 74(9), 3735-3739.
- Cazzulo, J. J. (1992). Aërobe fermentatie van glucose door trypanosomatiden. Het FASEB Journal, 6, 3153-3161.
- Jones, W., & Bianchi, K. (2015). Aërobe glycolyse: verder dan proliferatie. Grenzen in immunologie, 6, 1-5.
- Li, X., Gu, J., en Zhou, Q. (2015). Herziening van aërobe glycolyse en de belangrijkste enzymen - nieuwe doelen voor longkankertherapie. Thoracale kanker, 6, 17-24.
- Maris, A. J. A. Van, Abbott, Æ. D. A., Bellissimi, Æ. E., Brink, J. Van Den, Kuyper, Æ. M., Luttik, Æ. M. A. H., Pronk, J. T. (2006). Alcoholische fermentatie van koolstofbronnen in biomassahydrolysaten door Saccharomyces cerevisiae: huidige status. Antonie van Leeuwenhoek, 90, 391-418.
- Nelson, D. L., en Cox, M. M. (2009). Lehninger-principes van biochemie. Omega-edities (5e ed.).



Niemand heeft nog op dit artikel gereageerd.