
Beer-Lambert wettoepassingen en opgeloste oefeningen
De Wet van Beer-Lambert (Beer-Bouguer) is er een die de absorptie van elektromagnetische straling van een of meer chemische soorten relateert aan de concentratie en de afstand die licht aflegt in deeltjes-foton-interacties. Deze wet brengt twee wetten in één samen.
De wet van Bouguer (hoewel de erkenning meer op Heinrich Lambert is gevallen), stelt dat een monster meer straling zal absorberen wanneer de afmetingen van het absorberende medium of materiaal groter zijn; specifiek de dikte, die de afstand is l dat het licht reist bij het binnenkomen en verlaten.
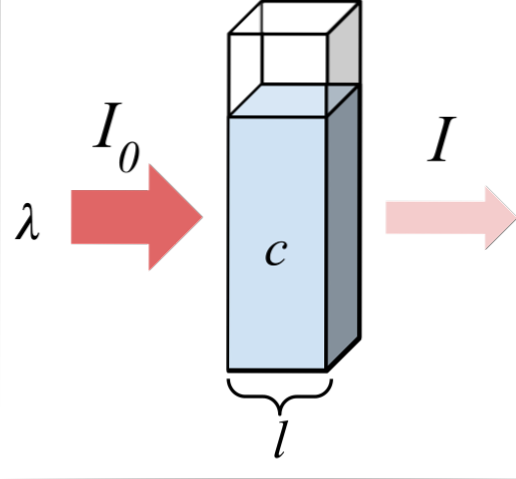
De bovenste afbeelding toont de absorptie van monochromatische straling; dat wil zeggen, samengesteld uit een enkele golflengte, λ. Het absorberende medium bevindt zich in een optische cel, waarvan de dikte is l, en bevat chemische soorten met een concentratie c.
De lichtstraal heeft een begin- en eindintensiteit, aangeduid door de symbolen I0 en ik, respectievelijk. Merk op dat ik na interactie met het absorberende medium minder ben dan ik0, waaruit blijkt dat er absorptie van straling was. Hoe ouder ze zijn c Y l, kleiner zal ik zijn met betrekking tot ik0dat wil zeggen, er zal meer absorptie zijn en minder doorlaatbaarheid.
Artikel index
- 1 Wat is de wet van Beer-Lambert?
- 1.1 Absorptie en doorlaatbaarheid
- 1.2 Afbeeldingen
- 2 Toepassingen
- 3 Opgeloste oefeningen
- 3.1 Oefening 1
- 3.2 Oefening 2
- 4 referenties
Wat is de wet van Beer-Lambert?
De afbeelding hierboven omvat perfect deze wet. De absorptie van straling in een monster neemt exponentieel toe of af als functie van c of l. Om de wet volledig en gemakkelijk te begrijpen, is het noodzakelijk om de wiskundige aspecten ervan te omzeilen.
Zoals zojuist vermeld, ik0 en ik ben de intensiteiten van de monochromatische lichtbundel voor respectievelijk na het licht. Sommige teksten geven er de voorkeur aan om de symbolen P te gebruiken0 en P, die verwijzen naar de energie van de straling en niet naar de intensiteit ervan. Hier wordt de uitleg voortgezet aan de hand van de intensiteiten.
Om de vergelijking van deze wet te lineariseren, moet de logaritme worden toegepast, meestal de grondtal 10:
Logboek (I.0/ I) = εlc
De term (I0/ I) geeft aan hoeveel de intensiteit van het stralingsproduct van absorptie afneemt. De wet van Lambert beschouwt l (εl), terwijl de wet van Beer l negeert, maar plaatsen c in plaats daarvan (εcDe bovenste vergelijking is de vereniging van beide wetten en is daarom de algemene wiskundige uitdrukking voor de wet van Beer-Lambert.
Absorptie en doorlaatbaarheid
De absorptie wordt gedefinieerd door de term Log (I.0/ I). De vergelijking wordt dus als volgt uitgedrukt:
A = εlc
Waar ε de extinctiecoëfficiënt of het molaire absorptievermogen is, wat een constante is bij een bepaalde golflengte.
Merk op dat als de dikte van het absorberende medium constant wordt gehouden, zoals ε, de absorptie A alleen afhangt van de concentratie c, van absorberende soorten. Het is ook een lineaire vergelijking, y = mx, waar Y is A, en X het is c.
Naarmate de absorptie toeneemt, neemt de transmissie af; dat wil zeggen hoeveel straling erin slaagt om na absorptie te worden overgedragen. Ze zijn dus omgekeerd. Ja ik0/ I geeft de mate van absorptie aan, I / I0 is gelijk aan doorlaatbaarheid. Dit wetende:
Ik / ik0 = T
(IK0/ I) = 1 / T
Logboek (I.0/ I) = Logboek (1 / T)
Maar Log (I0/ I) is ook gelijk aan absorptie. Dus de relatie tussen A en T is:
A = Logboek (1 / T)
En de eigenschappen van logaritmen toepassen en weten dat Log1 gelijk is aan 0:
A = -LogT
Transmissies worden meestal uitgedrukt in percentages:
% T = I / I0∙ 100
Grafieken
Zoals eerder vermeld, komen de vergelijkingen overeen met een lineaire functie; daarom wordt verwacht dat ze bij het tekenen ervan een lijn zullen geven.
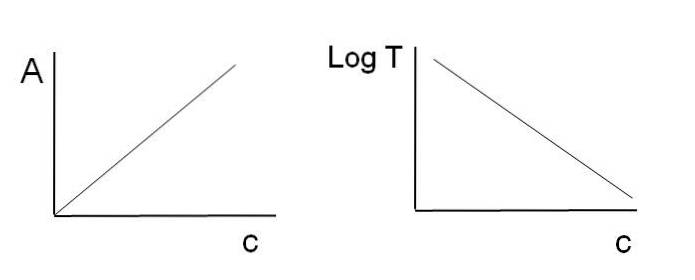
Merk op dat links van de afbeelding hierboven de lijn is die wordt verkregen door A tegen te tekenen c, en naar rechts de lijn die overeenkomt met de grafiek van LogT tegen c. De ene heeft een positieve helling en de andere negatief; hoe hoger de absorptie, hoe lager de doorlaatbaarheid.
Dankzij deze lineariteit kan de concentratie van de absorberende chemische soorten (chromoforen) worden bepaald of bekend is hoeveel straling ze absorberen (A), of hoeveel straling wordt doorgelaten (LogT). Wanneer deze lineariteit niet wordt nageleefd, wordt er gezegd dat deze wordt geconfronteerd met een afwijking, positief of negatief, van de wet van Beer-Lambert.
Toepassingen
In algemene termen worden hieronder enkele van de belangrijkste toepassingen van deze wet genoemd:
-Als een chemische soort kleur vertoont, is het een voorbeeldkandidaat om te worden geanalyseerd met colorimetrische technieken. Deze zijn gebaseerd op de wet van Beer-Lambert en maken het mogelijk om de concentratie van de analyten te bepalen als functie van de absorpties verkregen met een spectrofotometer..
-Het maakt de constructie van ijkcurves mogelijk, waarmee, rekening houdend met het matrixeffect van het monster, de concentratie van de soort van interesse wordt bepaald.
-Het wordt veel gebruikt om eiwitten te analyseren, aangezien verschillende aminozuren aanzienlijke absorpties hebben in het ultraviolette gebied van het elektromagnetische spectrum..
-Chemische reacties of moleculaire verschijnselen waarbij een kleurverandering betrokken is, kunnen worden geanalyseerd met behulp van absorptiewaarden bij een of meer golflengten..
-Met behulp van multivariate analyse kunnen complexe mengsels van chromoforen worden geanalyseerd. Op deze manier kan de concentratie van alle analyten worden bepaald, en ook kunnen de mengsels worden geclassificeerd en van elkaar worden onderscheiden; sluit bijvoorbeeld uit of twee identieke mineralen afkomstig zijn van hetzelfde continent of een bepaald land.
Opgeloste oefeningen
Oefening 1
Wat is de absorptie van een oplossing met een doorlaatbaarheid van 30% bij een golflengte van 640 nm??
Om het op te lossen, gaat u naar de definities van absorptie en transmissie.
% T = 30
T = (30/100) = 0,3
En wetende dat A = -LogT, is de berekening eenvoudig:
A = -Log 0,3 = 0,5228
Merk op dat het eenheden mist.
Oefening 2
Als de oplossing uit de vorige oefening bestaat uit een soort W waarvan de concentratie 2,30 ∙ 10 is-4 M, en aangenomen dat de cel 2 cm dik is: wat moet de concentratie zijn om een doorlaatbaarheid van 8% te verkrijgen??
Het kan direct worden opgelost met deze vergelijking:
-LogT = εlc
Maar de waarde van ε is onbekend. Daarom moet het worden berekend met de vorige gegevens, en er wordt aangenomen dat het constant blijft over een breed scala aan concentraties:
ε = -LogT / lc
= (-Log 0.3) / (2 cm x 2.3 ∙ 10-4 M)
= 1136,52 M-1∙ cm-1
En nu kunt u doorgaan met de berekening met% T = 8:
c = -LogT / εl
= (-Log 0,08) / (1136,52 M-1∙ cm-1 x 2 cm)
= 4,82 ∙ 10-4 M.
Dan is het voldoende voor de W-soort om zijn concentratie te verdubbelen (4,82 / 2,3) om zijn doorlatingspercentage te verlagen van 30% naar 8%..
Referenties
- Day, R., & Underwood, A. (1965). Kwantitatieve analytische chemie. (vijfde ed.). PEARSON Prentice Hall, p 469-474.
- Skoog D.A., West D.M. (1986). Instrumentale analyse. (tweede ed.). Interamericana., Mexico.
- Soderberg T. (18 augustus 2014). De Beer-Lambert-wet. Chemie LibreTexts. Hersteld van: chem.libretexts.org
- Clark J. (mei 2016). De Beer-Lambert-wet. Hersteld van: chemguide.co.uk
- Colorimetrische analyse: de wet van bier of spectrofotometrische analyse. Hersteld van: chem.ucla.edu
- Dr. J.M. Fernandez Alvarez. (s.f.). Analytische chemie: handleiding met opgeloste problemen. [Pdf]. Hersteld van: dadun.unav.edu



Niemand heeft nog op dit artikel gereageerd.