
Carnot-machineformules, hoe het werkt en toepassingen

De carnot machine het is een ideaal cyclisch model waarin warmte wordt gebruikt om werk te doen. Het systeem kan worden opgevat als een zuiger die in een cilinder beweegt en een gas comprimeert. De uitgeoefende cyclus is die van Carnot, verkondigd door de vader van de thermodynamica, de Franse natuurkundige en ingenieur Nicolas Léonard Sadi Carnot..
Carnot verkondigde deze cyclus in het begin van de negentiende eeuw. De machine is onderworpen aan vier toestandsvariaties, wisselende omstandigheden zoals temperatuur en constante druk, waarbij een variatie van het volume wordt aangetoond bij het comprimeren en expanderen van het gas.
Artikel index
- 1 Formules
- 1.1 Isotherme uitzetting (A → B)
- 1.2 Adiabatische uitzetting (B → C)
- 1.3 Isotherme compressie (C → D)
- 1.4 Adiabatische compressie (D → A)
- 2 Hoe werkt de Carnot-machine?
- 3 Toepassingen
- 4 referenties
Formules
Volgens Carnot is het mogelijk om de behaalde prestatie te maximaliseren door de ideale machine aan variaties in temperatuur en druk te onderwerpen.
De Carnot-cyclus moet afzonderlijk worden geanalyseerd in elk van de vier fasen: isotherme expansie, adiabatische expansie, isotherme compressie en adiabatische compressie..
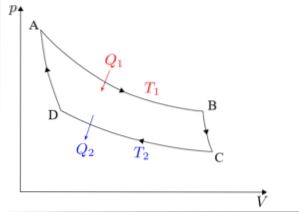
De formules die horen bij elk van de fasen van de cyclus die wordt uitgevoerd in de machine van Carnot, worden hieronder beschreven..
Isotherme uitzetting (A → B)
De uitgangspunten van deze fase zijn de volgende:
- Gasvolume: gaat van minimaal volume naar gemiddeld volume.
- Machinetemperatuur: constante temperatuur T1, hoge waarde (T1> T2).
- Machinedruk: daalt van P1 naar P2.
Het isotherme proces houdt in dat de temperatuur T1 tijdens deze fase niet varieert. Warmteoverdracht veroorzaakt gasexpansie, wat beweging op de zuiger induceert en mechanisch werk oplevert.
Naarmate het gas uitzet, heeft het de neiging af te koelen. Het absorbeert echter de warmte die wordt afgegeven door de temperatuurbron en houdt tijdens zijn uitzetting de temperatuur constant..
Omdat de temperatuur tijdens dit proces constant blijft, verandert de interne energie van het gas niet en wordt alle warmte die door het gas wordt geabsorbeerd effectief omgezet in arbeid. A) Ja:
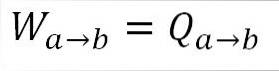
Van zijn kant is het aan het einde van deze fase van de cyclus ook mogelijk om de drukwaarde te verkrijgen met behulp van de ideale gasvergelijking. We hebben dus het volgende:
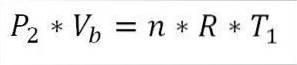
In deze uitdrukking:
P.twee: Druk aan het einde van de fase.
V.b: Volume op punt b.
n: aantal mol gas.
A: Universele constante van ideale gassen. R = 0,082 (atm * liter) / (mol * K).
T1: initiële absolute temperatuur, graden Kelvin.
Adiabatische uitzetting (B → C)
Tijdens deze fase van het proces vindt gasexpansie plaats zonder dat er warmte hoeft te worden uitgewisseld. Daarom worden de uitgangspunten hieronder gedetailleerd:
- Gasvolume: gaat van gemiddeld volume naar maximaal volume.
- Machinetemperatuur: daalt van T1 naar T2.
- Machinedruk: constante druk P2.
Het adiabatische proces houdt in dat de druk P2 tijdens deze fase niet varieert. De temperatuur daalt en het gas blijft uitzetten tot het zijn maximale volume bereikt; dat wil zeggen, de zuiger bereikt de aanslag.
In dit geval komt het verrichte werk voort uit de interne energie van het gas en is de waarde ervan negatief omdat de energie tijdens dit proces afneemt..
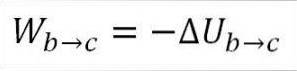
Ervan uitgaande dat het een ideaal gas is, stelt de theorie dat gasmoleculen alleen kinetische energie hebben. Volgens de principes van de thermodynamica kan dit worden afgeleid uit de volgende formule:
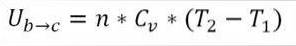
In deze formule:
∆Ub → c: Variatie van interne energie van het ideale gas tussen punten b en c.
n: aantal mol gas.
Cv: Molaire warmtecapaciteit van gas.
T1: initiële absolute temperatuur, graden Kelvin.
T2: absolute eindtemperatuur, graden Kelvin.
Isotherme compressie (C → D)
In deze fase begint de compressie van het gas; dat wil zeggen, de zuiger beweegt in de cilinder, waarmee het gas zijn volume samentrekt.
De voorwaarden die inherent zijn aan deze fase van het proces worden hieronder beschreven:
- Gasvolume: gaat van maximaal volume naar tussenvolume.
- Machinetemperatuur: constante temperatuur T2, verlaagde waarde (T2 < T1).
- Machinedruk: stijgt van P2 naar P1.
Hier neemt de druk op het gas toe, dus het begint te comprimeren. De temperatuur blijft echter constant en daarom is de variatie van de interne energie van het gas nul.
Analoog aan isotherme uitzetting is het uitgevoerde werk gelijk aan de warmte van het systeem. A) Ja:
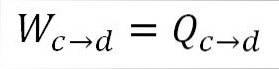
Het is ook mogelijk om de druk op dit punt te vinden met behulp van de ideale gasvergelijking.
Adiabatische compressie (D → A)
Het is de laatste fase van het proces, waarin het systeem terugkeert naar zijn oorspronkelijke toestand. Hierbij wordt aan de volgende voorwaarden gedacht:
- Gasvolume: gaat van een tussenvolume naar een minimumvolume.
- Machinetemperatuur: stijgt van T2 naar T1.
- Machinedruk: constante druk P1.
De warmtebron die in de vorige fase in het systeem was opgenomen, wordt verwijderd, zodat het ideale gas zijn temperatuur zal verhogen zolang de druk constant blijft..
Het gas keert terug naar de begintemperatuur (T1) en naar zijn volume (minimum). Nogmaals, het uitgevoerde werk komt van de interne energie van het gas, dus je moet:
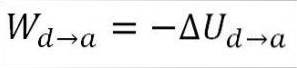
Net als bij adiabatische expansie, is het mogelijk om de variatie van de gassenergie te verkrijgen door middel van de volgende wiskundige uitdrukking:
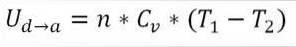
Hoe werkt de Carnot-machine?
De Carnot-motor werkt als een motor waarin de prestaties worden gemaximaliseerd door isotherme en adiabatische processen te variëren, waarbij de expansie- en compressiefasen van een ideaal gas worden afgewisseld..
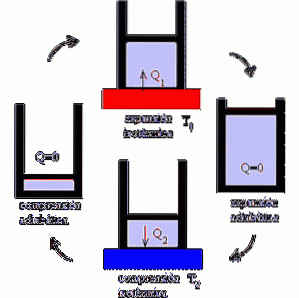
Gezien het bestaan van twee temperatuurbronnen, kan het mechanisme worden opgevat als een ideaal apparaat dat werkzaamheden verricht onder invloed van warmtevariaties.
In de eerste focus wordt het systeem blootgesteld aan een temperatuur T1. Het is een hoge temperatuur die het systeem onder druk zet en ervoor zorgt dat het gas uitzet..
Dit vertaalt zich op zijn beurt in de uitvoering van een mechanisch werk dat de mobilisatie van de zuiger uit de cilinder mogelijk maakt en waarvan de stop alleen mogelijk is door adiabatische uitzetting..
Dan komt de tweede focus, waarbij het systeem wordt blootgesteld aan een temperatuur T2, lager dan T1; dat wil zeggen dat het mechanisme wordt afgekoeld.
Dit leidt tot het onttrekken van warmte en het verbrijzelen van het gas, dat na adiabatische compressie zijn oorspronkelijke volume bereikt..
Toepassingen
De Carnot-machine is op grote schaal gebruikt dankzij zijn bijdrage aan het begrijpen van de belangrijkste aspecten van de thermodynamica.
Dit model biedt een duidelijk inzicht in de variaties van ideale gassen die onderhevig zijn aan veranderingen in temperatuur en druk, waardoor het een referentiemethode is bij het ontwerpen van echte motoren..
Referenties
- Carnot Heat Engine Cycle en de 2e wet (s.f.). Hersteld van: nptel.ac.in
- Castellano, G. (2018). Carnot-machine. Hersteld van: famaf.unc.edu.ar
- Carnot-cyclus (s.f.) Ecured. Havana Cuba. Hersteld van: ecured.cu
- De Carnot-cyclus (s.f.). Hersteld van: sc.ehu.es
- Fowler, M. (s.f.). Heat Engines: de Carnot-cyclus. Hersteld van: galileo.phys.virginia.edu
- Wikipedia, The Free Encyclopedia (2016). Carnot-machine. Hersteld van: es.wikipedia.org



Niemand heeft nog op dit artikel gereageerd.