
Siliciumoxide (SiO2) structuur, eigenschappen, gebruik, productie
De siliciumoxide Het is een anorganische vaste stof die wordt gevormd door de vereniging van een siliciumatoom en twee zuurstofatomen. De chemische formule is SiOtwee. Deze natuurlijke verbinding wordt ook wel silica of siliciumdioxide genoemd..
De SiOtwee Het is het meest voorkomende mineraal in de aardkorst, aangezien zand bestaat uit silica. Afhankelijk van de structuur kan silica kristallijn of amorf zijn. Het is onoplosbaar in water, maar lost op in alkaliën en in fluorwaterstofzuur HF.

De SiOtwee het is ook aanwezig in de structuur van bepaalde planten, bacteriën en schimmels. Ook in skeletten van mariene organismen. Naast zand zijn er ook andere soorten stenen die silica zijn.
Silica wordt veel gebruikt en vervult verschillende functies. Het meest wijdverbreide gebruik is als filtermateriaal voor vloeistoffen zoals oliën en aardolieproducten, dranken zoals bier en wijn, evenals vruchtensappen..
Maar het heeft veel andere toepassingen. Een van de meest bruikbare en belangrijkste is de fabricage van bioactieve glazen, die het mogelijk maken om "steigers" te maken waar botcellen groeien om botstukken te produceren die door een ongeluk of ziekte ontbreken..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Kookpunt
- 3.5 Dichtheid
- 3.6 Oplosbaarheid
- 3.7 Chemische eigenschappen
- 4 Aanwezigheid in de natuur
- 4.1 Andere soorten natuurlijk silica
- 5 Verkrijgen
- 6 toepassingen
- 6.1 In verschillende toepassingen
- 6.2 In de voedingsindustrie
- 6.3 In de farmaceutische industrie
- 6.4 In de cosmetica- en persoonlijke verzorgingsindustrie
- 6.5 Bij therapeutische toepassingen
- 7 Risico's
- 8 referenties
Structuur
Siliciumdioxide SiOtwee is een molecuul van drie atomen, waarin het siliciumatoom met covalente bindingen is bevestigd aan twee zuurstofatomen.
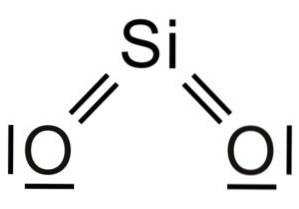
De structurele eenheid van vast silica als zodanig is een tetraëder waarin één siliciumatoom wordt omgeven door 4 zuurstofatomen.
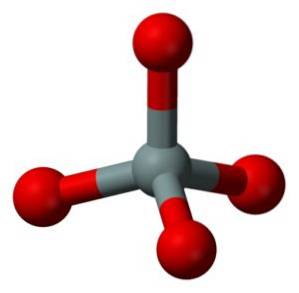
Tetraëders zijn met elkaar verbonden door de zuurstofatomen van hun aangrenzende hoekpunten te delen.
Daarom deelt een siliciumatoom elk van de 4 zuurstofatomen met de helft en dit verklaart de relatie in de verbinding van 1 siliciumatoom tot 2 zuurstofatomen (SiOtwee.

SiO-verbindingentwee zijn onderverdeeld in twee groepen: kristallijn silica en amorf silica.
Kristallijne silica-verbindingen hebben zich herhalende patroonstructuren van silicium en zuurstof.
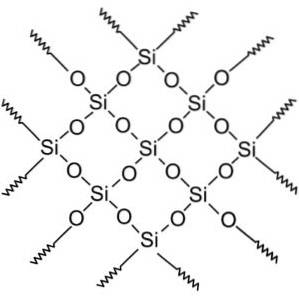
Alle silicakristallen kunnen worden beschouwd als een gigantisch molecuul waarvan het kristalrooster erg sterk is. Tetraëders kunnen op verschillende manieren met elkaar worden verbonden, waardoor verschillende kristallijne vormen ontstaan.
In amorf silica zijn de structuren willekeurig gehecht, zonder een gedefinieerd regelmatig patroon tussen de moleculen te volgen en deze staan in een verschillende ruimtelijke relatie met elkaar..
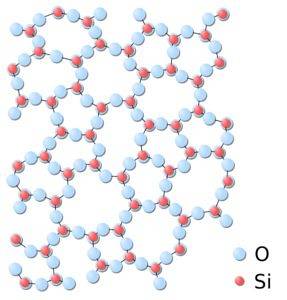
Nomenclatuur
-Siliciumoxide
-Siliciumdioxide
-Silica
-Kwarts
-Tridymite
-Cristobalita
-Dioxosilaan
Eigendommen
Fysieke toestand
Kleurloze tot grijze vaste stof.

Molecuulgewicht
60,084 g / mol
Smeltpunt
1713 ºC
Kookpunt
2230 ºC
Dichtheid
2,17-2,32 g / cm3
Oplosbaarheid
Onoplosbaar in water. Amorf silica is oplosbaar in basen, vooral als het fijn verdeeld is. Oplosbaar in fluorwaterstofzuur HF.
Amorf siliciumdioxide is minder hydrofiel, dat wil zeggen minder verwant aan water dan kristallijn.
Chemische eigenschappen
De SiOtwee o Silica is in wezen inert voor de meeste stoffen, het is zeer weinig reactief.
Weerstaat de aantasting van chloor Cltwee, broom Brtwee, waterstof Htwee en van de meeste zuren bij kamertemperatuur of iets hoger. Het wordt aangevallen door fluor Ftwee, fluorwaterstofzuur HF en basen zoals natriumcarbonaat NatweeCO3.
De SiOtwee Het kan worden gecombineerd met metalen elementen en oxiden om silicaten te vormen. Als silica wordt versmolten met alkalimetaalcarbonaten bij ongeveer 1300 ° C, worden alkalisilicaten verkregen en komt CO vrij.twee.
Het is niet brandbaar. Heeft een lage thermische geleidbaarheid.
Aanwezigheid in de natuur
De belangrijkste bron van silica in de natuur is zand.
De SiOtwee of silica heeft de vorm van drie kristallijne variëteiten: kwarts (de meest stabiele), tridymiet en cristobaliet. Amorfe vormen van silica zijn agaat, jaspis en onyx. Opal is een amorf gehydrateerd silica.
Er is ook het zogenaamde biogene silica, dat wil zeggen dat het wordt gegenereerd door levende organismen. Bronnen van dit type silica zijn bacteriën, schimmels, diatomeeën, zeesponzen en planten.
De glanzende, harde delen van bamboe en stro bevatten silica, en de skeletten van sommige mariene organismen bevatten ook een hoog gehalte aan silica; de belangrijkste zijn echter diatomeeënaarde.
Diatomeeënaarde zijn geologische producten van vergane eencellige organismen (algen).
Andere soorten natuurlijk silica
In de natuur zijn er ook de volgende soorten:
- Glasachtige siliciumdioxide die vulkanische glazen zijn
- De lechaterielieten die natuurlijke glazen zijn die worden geproduceerd door de versmelting van kiezelhoudend materiaal onder invloed van meteorieten
- Gesmolten siliciumdioxide dat siliciumdioxide is dat tot de vloeistoffase wordt verwarmd en afgekoeld zonder het te laten kristalliseren
Het verkrijgen van
Silica uit zand wordt rechtstreeks uit steengroeven gewonnen.

Diatomiet of diatomeeënaarde wordt ook op deze manier verkregen met behulp van graafmachines en soortgelijke apparatuur..
Amorf silica wordt bereid uit waterige oplossingen van alkalimetaalsilicaat (zoals natrium Na) door neutralisatie met zuur, zoals zwavelzuur HtweeSW4, zoutzuur HCl of kooldioxide COtwee.
Als de uiteindelijke pH van de oplossing neutraal of alkalisch is, wordt neergeslagen silica verkregen. Als de pH zuur is, wordt silicagel verkregen.
Pyrogeen kiezelzuur wordt bereid door verbranding van een vluchtige siliciumverbinding, gewoonlijk siliciumtetrachloride SiCl4. Neergeslagen silica wordt verkregen uit een waterige oplossing van silicaten waaraan zuur wordt toegevoegd.
Colloïdaal siliciumdioxide is een stabiele dispersie van deeltjes van amorf siliciumdioxide van colloïdale grootte in een waterige oplossing.
Toepassingen
In verschillende toepassingen
Silica of SiOtwee Het heeft een breed scala aan functies, het dient bijvoorbeeld als schurend, absorberend, antiklontermiddel, vulmiddel, opaakmakend middel en om de suspensie van andere stoffen te bevorderen, naast vele andere gebruikswijzen..
Het wordt bijvoorbeeld gebruikt:
-Bij de vervaardiging van glas, keramiek, vuurvaste materialen, schuurmiddelen en waterglas
-Verkleuring en zuivering van oliën en aardolieproducten
-In gietvormen
-Als antiklontermiddel voor alle soorten poeders
-Als ontschuimer
-Voor het filteren van vloeistoffen zoals oplosmiddelen voor chemisch reinigen, zwembadwater en gemeentelijk en industrieel afvalwater
-Bij de fabricage van warmte-isolatie, brandvertragende stenen en brand- en zuurbestendige verpakkingsmaterialen
-Als vulstof bij de vervaardiging van papier en karton, om ze resistenter te maken
-Als verfplamuur om de vloei en kleur te verbeteren
-In materialen voor het polijsten van metalen en hout, omdat het ze een schurende werking geeft
-In laboratoria voor chemische analyse in chromatografie en als absorptiemiddel
-Als antiklontermiddel in insectendodende en agrochemische formules, om wasachtige pesticiden te helpen vermalen en als drager van de werkzame stof
-Als katalysatorondersteuning
-Als vulmiddel om synthetische rubbers en rubbers te versterken
-Als vloeibare drager in diervoeder
-In drukinkten
-Als droog- en adsorptiemiddel, in de vorm van silicagel
-Als additief in cement
-Zoals kattenbakvulling
-In isolatoren voor micro-elektronica
-Op thermo-optische schakelaars

In de voedingsindustrie
Amorfe silica wordt in verschillende voedingsproducten verwerkt als een multifunctioneel direct ingrediënt in verschillende soorten voedsel. Het mag niet meer zijn dan 2% van het afgewerkte voedsel.
Het dient bijvoorbeeld als antiklontermiddel (om te voorkomen dat bepaalde etenswaren vastplakken), als stabilisator bij de bierproductie, als antiprecipitant, om wijn, bier en fruit- of groentesappen te filteren..

Het werkt als een absorberend middel voor vloeistoffen in sommige voedingsmiddelen en als een bestanddeel van microcapsules om oliën op smaak te brengen.
Naast de SiOtwee Amorf wordt via een speciaal proces aangebracht op het oppervlak van de kunststoffen van voedselverpakkingsartikelen en fungeert als een barrière.
In de farmaceutische industrie
Het wordt toegevoegd als antiklontermiddel, verdikkingsmiddel, geleermiddel en als hulpstof, dat wil zeggen als hulpmiddel bij het tabletteren van verschillende geneesmiddelen en vitamines.
In de cosmetica- en persoonlijke verzorgingsindustrie
Het wordt in een groot aantal producten gebruikt: in gezichtspoeders, oogschaduw, eyeliners, lippenstift, blush, make-up verwijderaars, poeders, voetpoeders, haarkleurmiddelen en bleekmiddelen.
Ook in oliën en badzout, schuimbaden, hand- en lichaamscrèmes, vochtinbrengende crèmes, deodorants, gezichtscrèmes of maskers (behalve scheerschuim), parfums, lotions en reinigingscrèmes.
Ook in nachtcrèmes, nagellakken en glitters, huidverfrissende lotions, haartoners, tandpasta, haarconditioners, bruiningsgels en crèmes.
In therapeutische toepassingen
De SiOtwee Het is aanwezig in bioactieve glazen of bioglazen waarvan de belangrijkste eigenschap is dat ze chemisch kunnen reageren met de biologische omgeving eromheen, waardoor ze een sterke en blijvende band vormen met levend weefsel..
Dit type materiaal wordt gebruikt om botvervangers te maken, zoals die in het gezicht, als "scaffolds" waarop botcellen zullen groeien. Ze hebben een goede biocompatibiliteit aangetoond met zowel botten als zachte weefsels.
Met deze bioglazen kunnen de botten van het gezicht worden hersteld van mensen die ze door een ongeval of ziekte zijn kwijtgeraakt.
Risico's
Zeer fijne silicadeeltjes kunnen in de lucht terechtkomen en niet-explosieve stofdeeltjes vormen. Maar dit stof kan de huid en ogen irriteren. Inademing veroorzaakt irritatie van de luchtwegen.
Bovendien veroorzaakt inademing van silicastof op lange termijn progressieve schade aan de longen, silicose genaamd..
Referenties
- ONS. Nationale bibliotheek van geneeskunde. (2019). Siliciumdioxide. Opgehaald van pubchem.ncbi.nlm.nih.gov.
- Cotton, F. Albert en Wilkinson, Geoffrey. (1980). Geavanceerde anorganische chemie. Vierde druk. John Wiley & Sons.
- Da Silva, M.R. et al. (2017). Groene extractietechnieken. Op silica gebaseerde sorptiemiddelen. In uitgebreide analytische chemie. Opgehaald van sciencedirect.com.
- Ylänen, H. (redacteur). (2018). Bioactieve glazen: materialen, eigenschappen en toepassingen (tweede editie). Elsevier. Opgehaald van books.google.co.ve.
- Windholz, M. et al. (redactie) (1983) The Merck Index. Een encyclopedie van chemicaliën, medicijnen en biologische producten. Tiende editie. Merck & CO., Inc.
- Mäkinen, J. en Suni, T. (2015). SOI-wafers met dikke film. In Handbook of Silicon Based MEMS Materials and Technologies (Second Edition). Opgehaald van sciencedirect.com.
- Sirleto, L. et al. (2010). Thermo-optische schakelaars. Silicium nanokristallen. Opgehaald van sciencedirect.com.



Niemand heeft nog op dit artikel gereageerd.