
Koolstof in natuurlocatie, eigenschappen en gebruik

De koolstof in de natuur Het is te vinden in diamanten, olie en grafiet, naast vele andere instellingen. Dit chemische element bezet de zesde plaats in het periodiek systeem en bevindt zich in de horizontale rij of periode 2 en kolom 14. Het is niet-metallisch en vierwaardig; dat wil zeggen, u kunt 4 gedeelde elektronenchemische bindingen of covalente bindingen tot stand brengen.
Koolstof is het meest voorkomende element in de aardkorst. Deze overvloed, zijn unieke diversiteit in de vorming van organische verbindingen en zijn uitzonderlijke vermogen om macromoleculen of polymeren te vormen bij temperaturen die gewoonlijk op aarde voorkomen, maakt dat het een gemeenschappelijk element is van alle bekende levensvormen..

Koolstof komt in de natuur voor als een chemisch element zonder te combineren in de vorm van grafiet en diamant. Het wordt echter voor het grootste deel gecombineerd om chemische koolstofverbindingen te vormen, zoals calciumcarbonaat (CaCO3) en andere verbindingen in olie en aardgas.
Het vormt ook verschillende mineralen zoals antraciet, steenkool, bruinkool en turf. Het grootste belang van koolstof is dat het de zogenaamde "bouwsteen van het leven" vormt en in alle levende organismen aanwezig is..
Artikel index
- 1 Waar wordt koolstof aangetroffen en in welke vorm?
- 1.1 Kristallijne vormen
- 1.2 Amorfe vormen
- 1.3 Olie, aardgas en bitumen
- 2 Fysische en chemische eigenschappen
- 2.1 Chemisch symbool
- 2.2 Atoomnummer
- 2.3 Fysieke toestand
- 2.4 Kleur
- 2.5 Atomaire massa
- 2.6 Smeltpunt
- 2.7 Kookpunt
- 2.8 Dichtheid
- 2.9 Oplosbaarheid
- 2.10 Elektronische configuratie
- 2.11 Aantal elektronen in de buitenste of valentieschil
- 2.12 Link capaciteit
- 2.13 Aanleiding
- 3 Biogeochemische cyclus
- 3.1 Fotosynthese
- 3.2 Ademhaling en ontbinding
- 3.3 Geologische processen
- 3.4 Inmenging door menselijke activiteit
- 4 toepassingen
- 4.1 Olie en aardgas
- 4.2 Grafiet
- 4.3 Diamant
- 4.4 Antraciet
- 4.5 Steenkool
- 4.6 Bruinkool
- 4.7 Turf
- 5 referenties
Waar wordt koolstof gevonden en in welke vorm?
Behalve dat het het gemeenschappelijke chemische bestanddeel is in alle vormen van leven, is koolstof in de natuur aanwezig in drie kristallijne vormen: diamant, grafiet en fullereen..
Er zijn ook verschillende amorfe minerale vormen van steenkool (antraciet, bruinkool, steenkool, turf), vloeibare vormen (oliesoorten) en gasvormig (aardgas).
Kristallijne vormen
In kristallijne vormen komen koolstofatomen samen om geordende patronen te vormen met geometrische ruimtelijke ordening.
Grafiet
Het is een zachte zwarte vaste stof met een metaalglans of glans en hittebestendig (vuurvast). De kristallijne structuur presenteert koolstofatomen die zijn samengevoegd in zeshoekige ringen die op hun beurt samenkomen met vormplaten.
Grafietafzettingen zijn zeldzaam en zijn aangetroffen in China, India, Brazilië, Noord-Korea en Canada..
Diamant
Het is een zeer harde vaste stof, transparant voor de doorgang van licht en veel dichter dan grafiet: de waarde van de dichtheid van diamant is bijna tweemaal die van grafiet.
De koolstofatomen in de diamant zijn verbonden in tetraëdrische geometrie. Evenzo wordt diamant gevormd uit grafiet dat is blootgesteld aan zeer hoge temperaturen en drukken (3000 C en 100.000 atm).
De meeste diamanten bevinden zich tussen 140 en 190 km diep in de mantel. Door diepe vulkaanuitbarstingen kan magma ze naar afstanden dicht bij het oppervlak transporteren.
Er zijn diamantafzettingen in Afrika (Namibië, Ghana, Democratische Republiek Congo, Sierra Leone en Zuid-Afrika), Amerika (Brazilië, Colombia, Venezuela, Guyana, Peru), Oceanië (Australië) en Azië (India).

Fullerenen
Het zijn moleculaire vormen van koolstof die clusters vormen van 60 en 70 koolstofatomen in bijna bolvormige moleculen, vergelijkbaar met voetballen..
Er zijn ook kleinere fullerenen met 20 koolstofatomen. Sommige vormen van fullerenen zijn onder meer koolstofnanobuisjes en koolstofvezels..

Amorfe vormen
In amorfe vormen verenigen de koolstofatomen zich niet en vormen ze een geordende en regelmatige kristallijne structuur. In plaats daarvan bevatten ze zelfs onzuiverheden van andere elementen.
Antraciet
Het is de oudste metamorfe minerale steenkool (die afkomstig is van de modificatie van gesteenten door effecten van temperatuur, druk of chemische werking van vloeistoffen), aangezien de vorming dateert uit het primaire of Paleozoïcum, het Carboon..
Antraciet is de amorfe vorm van koolstof met het hoogste gehalte aan dit element: tussen 86 en 95%. Het is grijszwart van kleur met een metaalglans, en het is zwaar en compact..
Antraciet komt over het algemeen voor in geologische vervormingszones en vormt ongeveer 1% van de steenkoolreserves in de wereld..
Geografisch wordt het gevonden in Canada, de VS, Zuid-Afrika, Frankrijk, Groot-Brittannië, Duitsland, Rusland, China, Australië en Colombia.

Steenkool
Het is een minerale steenkool, een sedimentair gesteente van organische oorsprong, waarvan de formatie dateert uit het Paleozoïcum en Mesozoïcum. Het heeft een koolstofgehalte tussen 75 en 85%.
Het is zwart van kleur, gekenmerkt doordat het ondoorzichtig is en een mat en vettig uiterlijk heeft, aangezien het een hoog gehalte aan bitumineuze stoffen bevat. Het wordt gevormd door compressie van bruinkool in het Paleozoïcum, in het Carboon en Perm.
Het is de meest voorkomende vorm van koolstof op aarde. Er zijn grote steenkoolvoorraden in de Verenigde Staten, Groot-Brittannië, Duitsland, Rusland en China.
Bruinkool
Het is een minerale fossiele steenkool die in het Tertiaire tijdperk is ontstaan uit turf door compressie (hoge drukken). Het heeft een lager koolstofgehalte dan steenkool, tussen 70 en 80%.
Het is een materiaal dat niet erg compact is, kruimelig (een kenmerk dat het onderscheidt van andere koolstofmineralen), bruin of zwart van kleur. De textuur is vergelijkbaar met die van hout en het koolstofgehalte varieert van 60 tot 75%.
Het is een gemakkelijk te ontsteken brandstof, met een lage calorische waarde en met een lager watergehalte dan turf..
Er zijn belangrijke bruinkoolmijnen in Duitsland, Rusland, Tsjechië, Italië (regio Veneto, Toscane, Umbrië) en Sardinië. In Spanje zijn de bruinkoolafzettingen in Asturië, Andorra, Zaragoza en La Coruña.
Turf
Het is een materiaal van organische oorsprong waarvan de vorming stamt uit het Kwartair tijdperk, veel recenter dan eerdere kolen.
Het is bruinachtig geel van kleur en verschijnt in de vorm van een sponsachtige massa met een lage dichtheid, waarin je plantenresten kunt zien vanaf de plaats waar het is ontstaan..
In tegenstelling tot de hierboven genoemde kolen, komt turf niet voort uit carboniseringsprocessen van houtachtig materiaal of hout, maar is het gevormd door de opeenhoping van planten - voornamelijk grassen en mossen - in moerassige gebieden door een carbonisatieproces dat niet is voltooid..
Turf heeft een hoog watergehalte; daarom moet het voor gebruik worden gedroogd en verdicht.
Het heeft een laag koolstofgehalte (slechts 55%); daarom heeft het een lage energetische waarde. Bij verbranding is het asresten overvloedig aanwezig en komt er veel rook vrij.
Er zijn belangrijke turfafzettingen in Chili, Argentinië (Tierra del Fuego), Spanje (Espinosa de Cerrato, Palencia), Duitsland, Denemarken, Nederland, Rusland, Frankrijk.

Olie, aardgas en bitumen
Olie (uit het Latijn petrae, wat betekent "steen"; Y oleum, wat 'olie' betekent: 'steenolie') is een mengsel van veel organische verbindingen - de meeste koolwaterstoffen - geproduceerd door de anaërobe bacteriële afbraak (in afwezigheid van zuurstof) van organisch materiaal.
Het werd gevormd in de ondergrond, op grote diepten en onder speciale omstandigheden zowel fysisch (hoge drukken en temperaturen) als chemisch (aanwezigheid van specifieke katalysatorverbindingen) in een proces dat miljoenen jaren in beslag nam..
Tijdens dit proces kwamen C en H vrij uit de organische weefsels en samengevoegd, opnieuw gecombineerd, om een immens aantal koolwaterstoffen te vormen die zich mengen volgens hun eigenschappen en aardgas, olie en bitumen vormen..
De olievelden van de planeet bevinden zich voornamelijk in Venezuela, Saoedi-Arabië, Irak, Iran, Koeweit, Verenigde Arabische Emiraten, Rusland, Libië, Nigeria en Canada.
Er zijn aardgasreserves in onder meer Rusland, Iran, Venezuela, Qatar, de Verenigde Staten, Saudi-Arabië en de Verenigde Arabische Emiraten.
Fysische en chemische eigenschappen
Onder de eigenschappen van koolstof kunnen we het volgende noemen:
Chemisch symbool
C.
Atoomnummer
6.
Fysieke toestand
Vaste stof, onder normale druk- en temperatuuromstandigheden (1 atmosfeer en 25 C).
Kleur
Grijs (grafiet) en transparant (diamant).
Atoom massa
12,011 g / mol.
Smeltpunt
500 C.
Kookpunt
827 C.
Dichtheid
2,62 g / cm3.
Oplosbaarheid
Onoplosbaar in water, oplosbaar in CCl-tetrachloorkoolstof4.
Elektronische configuratie
1stwee 2 sectwee 2 Blztwee.
Aantal elektronen in de buitenste of valentieschil
4.
Link capaciteit
4.
Aaneenschakeling
Heeft het vermogen om chemische verbindingen in lange ketens te vormen.
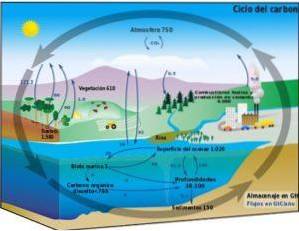
Biogeochemische cyclus
De koolstofcyclus is een biogeochemisch circulair proces waardoor koolstof kan worden uitgewisseld tussen de terrestrische biosfeer, atmosfeer, hydrosfeer en lithosfeer..
De kennis van dit cyclische koolstofproces op aarde stelt ons in staat om menselijk handelen in deze cyclus en de gevolgen ervan voor de wereldwijde klimaatverandering te demonstreren.
Koolstof kan circuleren tussen de oceanen en andere watermassa's, maar ook tussen de lithosfeer, in de bodem en ondergrond, in de atmosfeer en in de biosfeer. In de atmosfeer en hydrosfeer komt koolstof in gasvorm voor als COtwee (kooldioxide).
Fotosynthese
Koolstof uit de atmosfeer wordt opgevangen door terrestrische en in het water levende organismen van ecosystemen (fotosynthetische organismen).
Door fotosynthese kan een chemische reactie plaatsvinden tussen COtwee en water, gemedieerd door zonne-energie en chlorofyl uit planten, om koolhydraten of suikers te produceren. Dit proces transformeert eenvoudige moleculen met een lage energie-inhoud van COtwee, H.tweeO en zuurstof Otwee, in complexe hoogenergetische moleculaire vormen, die suikers zijn.
Heterotrofe organismen - die niet kunnen fotosynthetiseren en consumenten zijn in ecosystemen - verkrijgen koolstof en energie door zich te voeden met producenten en andere consumenten.
Ademhaling en ontbinding
Ademhaling en afbraak zijn biologische processen waarbij koolstof in de vorm van CO vrijkomttwee of CH4 (methaan geproduceerd bij anaërobe ontbinding; dat wil zeggen in afwezigheid van zuurstof).
Geologische processen
Door geologische processen en als gevolg van het verstrijken van de tijd kan de koolstof uit anaerobe ontbinding worden omgezet in fossiele brandstoffen zoals olie, aardgas en steenkool. Evenzo maakt koolstof ook deel uit van andere mineralen en gesteenten.
Interferentie door menselijke activiteit
Wanneer de mens de verbranding van fossiele brandstoffen gebruikt voor energie, keert koolstof terug naar de atmosfeer in de vorm van enorme hoeveelheden CO.twee die niet kan worden geassimileerd door de natuurlijke biogeochemische koolstofcyclus.
Dit teveel aan COtwee geproduceerd door menselijke activiteit heeft een negatieve invloed op de balans van de koolstofcyclus en is de hoofdoorzaak van de opwarming van de aarde.
Toepassingen
De toepassingen van koolstof en zijn verbindingen zijn zeer gevarieerd. De meest prominente met de volgende:
Olie en aardgas
Het belangrijkste economische gebruik van koolstof wordt vertegenwoordigd door het gebruik ervan als koolwaterstof op fossiele brandstof, zoals methaangas en olie.
Olie wordt in raffinaderijen gedestilleerd om meerdere derivaten te verkrijgen, zoals benzine, diesel, kerosine, asfalt, smeermiddelen, oplosmiddelen en andere, die op hun beurt weer worden gebruikt in de petrochemische industrie die grondstoffen produceert voor de kunststoffen-, kunstmest-, geneesmiddelen- en verfindustrie., onder andere.
Grafiet
Grafiet wordt gebruikt bij de volgende acties:
- Het wordt gebruikt bij de vervaardiging van potloden, gemengd met klei.
- Het maakt deel uit van de productie van vuurvaste stenen en smeltkroezen die bestand zijn tegen hitte.
- In verschillende mechanische apparaten zoals ringen, lagers, zuigers en afdichtingen.
- Het is een uitstekend vast smeermiddel.
- Vanwege zijn elektrische geleidbaarheid en zijn chemische inertie wordt het gebruikt bij de vervaardiging van elektroden, koolstofatomen voor elektromotoren..
- Het wordt gebruikt als moderator in kerncentrales.
Diamant
Diamant heeft bijzonder uitzonderlijke fysische eigenschappen, zoals de hoogste graad van hardheid en thermische geleidbaarheid die tot nu toe bekend is.
Deze eigenschappen maken industriële toepassingen mogelijk in gereedschappen die worden gebruikt voor het maken van sneden en instrumenten voor polijsten vanwege het hoge abrasieve vermogen..
Zijn optische eigenschappen - zoals transparantie en het vermogen om wit licht af te breken en licht te breken - maken het veel toepassingen in optische instrumenten, zoals bij de vervaardiging van lenzen en prisma's..
De karakteristieke glans die wordt ontleend aan zijn optische eigenschappen wordt ook hoog gewaardeerd in de sieradenindustrie..
Antraciet
Antraciet is moeilijk ontvlambaar, brandt traag en heeft veel zuurstof nodig. De verbranding produceert een kleine lichtblauwe vlam en geeft veel warmte af.
Enkele jaren geleden werd antraciet gebruikt in thermo-elektrische centrales en voor woningverwarming. Het gebruik ervan heeft voordelen zoals de productie van weinig as of stof, weinig rook en een traag verbrandingsproces..
Vanwege de hoge economische kosten en de schaarste is antraciet vervangen door aardgas in thermo-elektrische centrales en door elektriciteit in woningen.
Steenkool
Steenkool wordt gebruikt als grondstof om te verkrijgen:
- Cokes, brandstof voor hoogovens in staalfabrieken.
- Creosoot, verkregen door het mengen van teerdestillaten uit steenkool en gebruikt als beschermende kit voor hout dat aan de elementen wordt blootgesteld.
- Cresol (chemisch methylfenol) gewonnen uit steenkool en gebruikt als ontsmettingsmiddel en antisepticum,
- Andere derivaten zoals gas, teer of pek, en verbindingen die worden gebruikt bij de vervaardiging van onder meer parfums, insecticiden, kunststoffen, verf, banden en wegdek.
Bruinkool
Bruinkool is een brandstof van gemiddelde kwaliteit. Jet, een variëteit van bruinkool, wordt gekenmerkt door zijn zeer compactheid vanwege het lange carbonisatieproces en de hoge druk, en wordt gebruikt in sieraden en versieringen.
Turf
Turf wordt gebruikt bij de volgende activiteiten;
- Voor de groei, ondersteuning en transport van plantensoorten.
- Als biologische compost.
- Zoals strooisel voor dieren in stallen.
- Als brandstof van lage kwaliteit.
Referenties
- Burrows, A., Holman, J., Parsons, A., Pilling, G. en Price, G. (2017). Chemistry3: Introductie van anorganische, organische en fysische chemie. Oxford Universiteit krant.
- Deming, A. (2010). Koning van de elementen? Nanotechnologie. 21 (30): 300201. doi: 10.1088
- Dienwiebel, M., Verhoeven, G., Pradeep, N., Frenken, J., Heimberg, J. en Zandbergen, H. (2004). Supergladheid van grafiet. Fysieke beoordelingsbrieven. 92 (12): 126101. doi: 10.1103
- Irifune, T., Kurio, A., Sakamoto, S., Inoue, T. en Sumiya, H. (2003). Materialen: Ultraharde polykristallijne diamant uit grafiet. Natuur. 421 (6923): 599-600. doi: 10,1038
- Savvatimskiy, A. (2005). Metingen van het smeltpunt van grafiet en de eigenschappen van vloeibare koolstof (een overzicht uit 1963-2003). Steenkool. 43 (6): 1115. doi: 10.1016

Niemand heeft nog op dit artikel gereageerd.