
Trichloorazijnzuur Structuur, eigenschappen, synthese, gebruik, effecten

De trichloorazijnzuur is een vaste organische verbinding waarvan de chemische formule C istweeHCl3OFtwee of CCl3-COOH. Het is ook bekend als trichloorethaanzuur en als TCA. Het is een monocarbonzuur waarin de waterstofatomen van het tweede koolstofatoom zijn vervangen door chloor. De kristallen zijn kleurloos tot wit.
TCA is zeer oplosbaar in water en produceert zeer zure oplossingen. Het kan proteïnen neerslaan uit een waterige oplossing. Langdurig contact met trichloorazijnzuur kan brandwonden op de huid veroorzaken..

Dit is echter met voordeel gebruikt om huidaandoeningen te behandelen, omdat het in verdunde oplossing en op een zeer goed gecontroleerde manier wordt gebruikt. ACT wordt ook vaak gebruikt in de zogenaamde pellen chemisch product voor huidverjonging.
Aan de andere kant, omdat het een organochloorverbinding is die in kleine hoeveelheden in het milieu wordt aangetroffen, wordt het de schuld gegeven als mogelijke oorzaak van schade aan bossen..
Ondanks het gehalte aan het element chloor, zijn er geen gegevens om te bevestigen of trichloorazijnzuur al dan niet kankerverwekkend is..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Kookpunt
- 3.5 Dichtheid
- 3.6 Oplosbaarheid
- 3,7 pH
- 3.8 Dissociatieconstante
- 3.9 Chemische eigenschappen
- 4 Synthese
- 5 Gebruik bij eiwitanalyse
- 6 Therapeutische toepassingen
- 7 Gebruik bij dermatologische behandelingen
- 7.1 Voor huidaandoeningen
- 7.2 Voor cosmetische behandelingen
- 8 Effect van TCA-besmetting
- 9 referenties
Structuur
Trichloorazijnzuur is een monocarbonzuur, dat wil zeggen dat het een enkele -COOH-groep bevat. Zijn skelet bevat slechts 2 koolstofatomen. Het is vergelijkbaar met azijnzuur CH3-COOH maar in plaats van de methylgroep -CH3, is eigenaar van een -CCl-groep3, dat wil zeggen, de formule is CCl3-COOH.
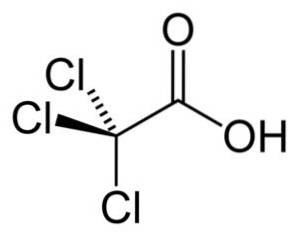
Nomenclatuur
- Trichloorazijnzuur
- Trichloorethaanzuur
- 2,2,2-trichloorazijnzuur
- TCA Trichloorazijnzuur
Eigendommen
Fysieke toestand
Kleurloze tot witte kristallijne vaste stof. De kristallen zijn rhombohedraal
Molecuulgewicht
163,38 g / mol
Smeltpunt
57,5 ºC
Kookpunt
195,5 ºC
Dichtheid
1,6 g / cm3
Oplosbaarheid
Zeer goede oplosbaarheid in water: 120 g / 100 ml bij 25 ºC.
Oplosbaar in ethanol CH3CHtweeOH en in diethylether CH3CHtweeOCHtweeCH3. Enigszins oplosbaar in CCl-tetrachloorkoolstof4.
pH
De pH van een waterige oplossing met 0,1 mol / L is 1,2.
Dissociatieconstante
pKnaar = 0,51 (betekent dat het een sterker zuur is dan azijnzuur)
Chemische eigenschappen
Trichloorazijnzuur is een hygroscopische vaste stof, het absorbeert vocht uit de lucht en vormt een stroperige vloeistof. Heeft een penetrante of penetrante geur.
Als het in water oplost, komt er warmte vrij. Het is corrosief voor metalen zoals ijzer, zink en aluminium, en voor biologische weefsels. Het is extreem corrosief voor de menselijke huid bij langdurig contact.
Het heeft de eigenschap proteïnen in oplossing neer te slaan.
Bij verhitting met basen om te ontbinden, geeft het giftige dampen van chloroform CH af3Cl, zoutzuur HCl, kooldioxide COtwee en koolmonoxide CO.
In de geraadpleegde bronnen is er geen consensus over de vraag of het al dan niet kankerverwekkend is.
Synthese
Het wordt op industrieel niveau bereid door chlorering van azijnzuur CH3-COOH, met chloor Cltwee al dan niet in aanwezigheid van katalysatoren.
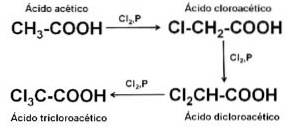
Gebruik bij eiwitanalyse
Trichloorazijnzuur wordt veel gebruikt voor de bepaling van eiwitten, zoals albumine. Het is een zeer effectief middel voor zijn neerslag, vooral uit verdunde eiwitoplossingen..
Precipitatie vindt op een specifieke en kwantitatieve manier plaats, waardoor ze kunnen worden gescheiden van andere niet-eiwitstoffen, zoals polysacchariden, kationen die aan eiwitten en zouten zijn gebonden, en waardoor proteasen kunnen worden denatureerd (enzymen die eiwitafbraak mogelijk maken).
Volgens de geraadpleegde literatuur is er niet veel bekend over het neerslagmechanisme. Er is gesuggereerd dat de dominante vorm die van hydrofobe aggregatie zou kunnen zijn, aangezien er een interval is, ongeveer 15% van trifluorazijnzuur, waarin de optimale neerslag plaatsvindt..
Therapeutische toepassingen
Verdunde TCA-oplossingen zijn met succes gebruikt bij de behandeling van acute externe otitis (oorpijn in het gebied vóór het trommelvlies of de uitwendige gehoorgang).
TCA deactiveert ontstekingscellen door hun eigenschappen te veranderen, het ontstoken gebied te drogen, oedeem te verminderen en pijn snel te verlichten. Het wordt ook zeer goed verdragen door patiënten, zowel kinderen als volwassenen..
Bovendien herstelt het de zure toestand van het gebied en remt het de proliferatie van bacteriën en schimmels in de acute fase van de ziekte. Zijn werkingsmechanisme voorkomt herhaling en progressie van de ziekte naar de chronische fase.
Gebruik bij dermatologische behandelingen
Voor huidaandoeningen
Het is gebruikt bij de behandeling van actinische keratose, een huidziekte die wordt gekenmerkt door een schilferig gebied dat zich vormt in delen van de huid die jarenlang chronisch worden blootgesteld aan UV-straling, zoals het gezicht, de leren hoofdhuid of de onderarmen..
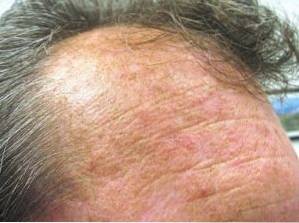
Een klein percentage van deze ziekte leidt tot huidkanker, vandaar het belang om deze vroegtijdig te behandelen.
Het wordt ook gebruikt voor rosacea, seborroïsche dermatitis, acne, xanthelasma's (kleine goedaardige vetophopingen), wratten, moedervlekken en hyperpigmentatie.
De procedure wordt chemi-exfoliatie of genoemd pellen Chemisch zuur en tricholoazijnzuur hebben de voorkeur boven andere chemische verbindingen vanwege de veiligheid, effectiviteit en systemische niet-toxiciteit.
TCA vernietigt chemisch de epidermis en de bovenste dermis van het behandelde gebied. De nieuwe epidermis migreert van de huidaanhechtingen onder het vernietigde weefsel, waarna de bovenliggende cortex binnen enkele dagen wordt afgestoten.
Dermale regeneratie is duidelijk na 2 tot 3 weken. Histologische veranderingen in de huid zijn homogenisatie van de collageenarchitectuur en een toename van elastisch weefsel in de dermis..
Deze veranderingen zijn permanent. Bovendien worden de abnormale cellen verwijderd en vervangen door normale epidermale cellen..
Voor cosmetische behandelingen
Burning-afschilfering o pellen met trichloorazijnzuur wordt ook gebruikt bij de cosmetische behandeling van verouderde, gerimpelde huid, sproeten, acnelittekens en tatoeages.

Het kan een relatief diepe huidverbranding veroorzaken zonder systemische toxiciteit te veroorzaken. Behandelingen moeten altijd worden uitgevoerd door opgeleid en ervaren personeel.
De variabelen waarmee rekening moet worden gehouden voor het succes van de techniek zijn de juiste concentratie van het zuur volgens het type en de dikte van de huid, de toepassingstechniek, de effectiviteit van de eerdere voorbereiding van de huid, dichtheid en activiteit van de talgklieren. en toepassing van keratolytische middelen vóór behandeling.
Elke patiënt moet worden geëvalueerd om de juiste concentratie te selecteren en rampzalige resultaten te voorkomen.
Effect van TCA-besmetting
Trichloorazijnzuur is een chemische verbinding die voorkomt in de lucht, regen, vegetatie en bodem. Om deze reden wordt verondersteld dat het verantwoordelijk is voor nadelige effecten op sommige bossen en oerwouden..

Er bestaat onzekerheid over de bronnen van TCA in het milieu. Hoewel er consensus bestaat dat het afkomstig kan zijn van de oxidatie van gechloreerde oplosmiddelen die in de atmosfeer aanwezig zijn, zijn de concentraties van TCA die in neerslag worden aangetroffen veel hoger dan wat zou worden verwacht als het afkomstig was van dergelijke oplosmiddelen..
TCA kan ook worden geproduceerd in en afgebroken in de bodem. Planten kunnen TCA uit zowel de lucht als de grond halen en van de bladeren naar de wortels worden getransporteerd en vice versa. Geschat wordt dat het wordt gemetaboliseerd in het gebladerte.
Bij tests die door sommige onderzoekers werden uitgevoerd op zaailingen van een soort dennen behandeld met niveaus van trichloorazijnzuur vergelijkbaar met die in de lucht in sommige delen van Europa, de VS en Canada, werd vastgesteld dat er geen zichtbare schade is aan planten of veranderingen in de groei hiervan als gevolg van eetstoornissen.
Slechts een geringe afname van het eiwitgehalte werd gevonden in met TCA behandelde planten, mogelijk als gevolg van de eigenschap van trichloorazijnzuur om eiwitten neer te slaan..
Referenties
- Novák, P. en Havlícek, V. (2016). Eiwitextractie en neerslag. In proteomische profilering en analytische chemie (tweede editie). Opgehaald van sciencedirect.com.
- ONS. Nationale bibliotheek van geneeskunde. (2019). Trichloorazijnzuur. Hersteld van: pubchem.ncbi.nlm.nih.gov
- Cape, N.J. et al. (2003). Langdurige blootstelling van sitkasparrenzaailingen aan trichloorazijnzuur. Environ. Sci Technol. 2003, 37, 2953-2957. Opgehaald van pubs.acs.org.
- Brodland, D.G. et al. (1988). Trichloorazijnzuur Chemexfoliation (chemische peeling) voor uitgebreide premaligne actinische schade aan het gezicht en de hoofdhuid. Mayo Clin Proc 63: 887-896, 1988. Opgehaald van ncbi.nlm.nih.gov.
- Collins, P.S. (1989). Trichloorazijnzuur Peels Revisited. Dermatol. Surg. Oncol. 1989; 15: 933-940. Hersteld van onlinelibrary.wiley.com.
- Kantas, I. et al. (2007). Het gebruik van trichloorazijnzuur bij de behandeling van acute externe otitis. Eur Arch Otorhinolaryngol (2007) 264: 9-14. Opgehaald van ncbi.clm.nih.gov.


Niemand heeft nog op dit artikel gereageerd.