
Karakteristieke kinasen, typen, functies
De kinasen of kinasenHet zijn eiwitten met enzymatische activiteit die verantwoordelijk zijn voor het katalyseren van de overdracht van fosfaatgroepen (PO4-3) naar verschillende soorten moleculen. Het zijn buitengewoon veel voorkomende enzymen in de natuur, waar ze transcendentale functies vervullen voor levende organismen: ze nemen deel aan het metabolisme, aan signalering en ook aan cellulaire communicatie..
Dankzij het grote aantal processen waarin ze meerdere functies vervullen, zijn kinasen een van de meest bestudeerde soorten eiwitten, niet alleen op biochemisch niveau, maar ook op structureel, genetisch en cellulair niveau..
Er is vastgesteld dat het menselijk genoom ten minste 500 genen heeft die coderen voor enzymen die tot de groep van kinasen behoren, waarvan de 'acceptorsubstraten' van fosfaatgroepen koolhydraten, lipiden, nucleosiden, eiwitten en andere soorten organische moleculen kunnen zijn..
Deze enzymen worden geclassificeerd in de groep van fosfotransferasen (EC 2.7), en gebruiken gewoonlijk als "donormoleculen" van fosfaatgroepen hoogenergetische verbindingen zoals ATP, GTP, CTP en andere gerelateerde.
Artikel index
- 1 Kenmerken
- 2 soorten
- 2.1 EC 2.7.1: fosfotransferase-enzymen met een alcohol als de fosfaatgroepacceptor
- 2.2 EC 2.7.2: fosfotransferase-enzymen met een carboxylgroep als acceptor van de fosfaatgroep
- 2.3 EC 2.7.3: fosfotransferase-enzymen met een stikstofatoom als acceptor van de fosfaatgroep
- 2.4 EC 2.7.4: fosfotransferase-enzymen met een andere fosfaatgroep als acceptor van de fosfaatgroep
- 2.5 EC 2.7.6: difosfotransferase-enzymen
- 2.6 EC 2.7.7: Nucleotide-specifieke fosfotransferasen (nucleotidylfosfotransferasen) enzymen
- 2.7 EC 2.7.8: enzymen die fosfaatgroepen overdragen met substituties
- 2.8 EC 2.7.9: Fosfotransferase-enzymen met gepaarde acceptoren
- 2.9 Fosfotransferasen die aminozuurresiduen van verschillende soorten eiwitten fosforyleren
- 2.10 Andere vormen van classificatie
- 3 functies
- 4 referenties
Kenmerken
De term "kinase", zoals is opgemerkt, verwijst gewoonlijk naar alle enzymen die verantwoordelijk zijn voor de overdracht van de eindstandige fosfaatgroep van ATP naar een andere receptor of "acceptormolecuul" van de fosfaatgroep..
Ondanks het feit dat deze enzymen in wezen dezelfde fosforylgroepoverdrachtreactie katalyseren, is er een grote diversiteit tussen hen, niet alleen in termen van structuur, maar ook in de specificiteit van substraten en de cellulaire routes waaraan ze deelnemen..
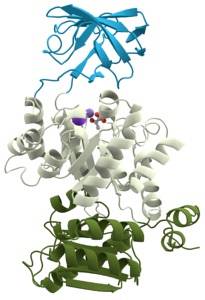
Over het algemeen bestaat de structuur uit β-gevouwen vellen en α-helices die specifiek vouwen om de actieve site te vormen, en deze actieve site bevat meestal positief geladen ionen (kationen) die de negatieve ladingen van de fosfaatgroepen die worden overgedragen stabiliseren..
Twee bindingsplaatsen voor substraten worden gevonden op of dichtbij de actieve plaats: één voor ATP of het fosfaatgroepdonormolecuul en één voor het te fosforyleren substraat..
De algemene reactie van deze enzymen (fosforylering) kan als volgt worden bekeken:
ATP + substraat → ADP + gefosforyleerd substraat
Waarbij ATP de fosfaatgroep schenkt die het substraat wint.
Types
Volgens de classificatie van het Nomenclatuurcomité van de International Union of Biochemistry and Molecular Biology (NC-IUBMB) worden kinasen aangetroffen in de groep van fosfotransferasen (EC. 2.7, enzymen die fosforhoudende groepen overdragen), die is onderverdeeld in beurt, in ongeveer 14 klassen (EC 2.7.1 - EC 2.7.14).
De fundamentele verschillen tussen deze 14 klassen van fosfotransferasen houden verband met de chemische aard van het "acceptormolecuul" van de fosfaatgroep die ze overdragen (of de aard van het deel van het molecuul dat de fosfaatgroep ontvangt)..
Binnen deze categorie (fosfotransferase-enzymen) zijn er ook enkele enzymen die fosfaatgroepen overdragen maar geen ATP-moleculen als "donor" gebruiken, maar in plaats daarvan anorganische fosfaten gebruiken..
In grote lijnen worden deze klassen als volgt beschreven:
EC 2.7.1: fosfotransferase-enzymen met een alcohol als de fosfaatgroepacceptor
Dit is een van de belangrijkste groepen voor het energiemetabolisme van veel organismen, omdat het de enzymen bevat die verantwoordelijk zijn voor de fosforylering van koolhydraten en hun derivaten, zoals glucose, galactose, fructose, mannose, glucosamine, ribose en ribulose, xylose, glycerol. pyruvaat, mevalonaat, arabinose, inositol en vele andere.
Voorbeelden van deze veel voorkomende enzymen zijn hexokinase, glucokinase, fosfofructokinase en pyruvaatkinase, die direct betrokken zijn bij de glycolytische route die verantwoordelijk is voor de oxidatie van glucose voor de productie van energie in de vorm van ATP..
EC 2.7.2: fosfotransferase-enzymen die een carboxylgroep als fosfaatgroepacceptor hebben
Binnen deze klasse van kinase- of fosfotransferase-enzymen vallen de enzymen die fosfaatgroepen overbrengen naar delen van moleculen met carboxylgroepen, zoals onder andere acetaat, carbamaat, aspartaat, fosfoglyceraat..
EC 2.7.3: fosfotransferase-enzymen die een stikstofatoom hebben als acceptor voor de fosfaatgroep
Metabolisch gezien is deze groep enzymen ook van groot belang, aangezien ze verantwoordelijk zijn voor de overdracht van fosfaatgroepen naar moleculen zoals creatinine, arginine, glutamine, guanidine-acetaat, enz..
EC 2.7.4: fosfotransferase-enzymen die een andere fosfaatgroep hebben als acceptor van de fosfaatgroep
Een groot deel van de enzymen in deze groep functioneren bij de regulering van de vorming of hydrolyse van hoogenergetische verbindingen zoals ATP, GTP, CTP en andere, aangezien ze verantwoordelijk zijn voor de toevoeging, verwijdering of uitwisseling van fosfaatgroepen tussen deze typen. van moleculen of zijn voorlopers.
Ze nemen ook deel aan de overdracht van fosfaatgroepen naar andere eerder gefosforyleerde moleculen, die lipide van aard kunnen zijn, koolhydraten of derivaten daarvan..
Voorbeelden van deze belangrijke enzymen zijn adenylaatkinase, nucleosidefosfaatkinase, nucleosidetrifosfaatadenylaatkinase, UMP / CMP-kinase en farnesylfosfaatkinase, enz..
EC 2.7.6: difosfotransferase-enzymen
Difosfotransferasen katalyseren de overdracht van twee fosfaatgroepen tegelijkertijd naar hetzelfde substraat. Voorbeelden van deze enzymen zijn ribose-fosfaatdifosfokinase, thiaminedifosfokinase en GTP-difosfokinase, een belangrijk enzym bij het metabolisme van purines..
EC 2.7.7: nucleotide-specifieke fosfotransferasen (nucleotidylfosfotransferasen) enzymen
Nucleotidylfosfotransferasen nemen deel aan veel cellulaire processen die betrokken zijn bij de activering en inactivering van andere eiwitten en enzymen, evenals bij sommige DNA-herstelmechanismen.
Zijn functie is om nucleotiden over te dragen, in het algemeen monofosfaatnucleotiden van verschillende stikstofhoudende basen. In deze klasse van enzymen bevinden zich onder andere DNA- en RNA-polymerasen (zowel afhankelijk van DNA als RNA), UDP-glucose-1-fosfaat-uridyltransferase.
EC 2.7.8: Enzymen die fosfaatgroepen met substituties overbrengen
Deze klasse heeft belangrijke functies in de routes van het vetmetabolisme, in het bijzonder hun synthese. Ze zijn verantwoordelijk voor de overdracht van gefosforyleerde moleculen (fosfaatgroepen met substituties) naar andere "acceptormoleculen"..
Voorbeelden van deze groep enzymen zijn ethanolamine-fosfotransferase, diacylglycerol-cholinefosfotransferase, sfingomyeline-synthase, enz..
EC 2.7.9: fosfotransferase-enzymen met gepaarde acceptoren
Deze enzymen gebruiken een enkele fosfaatgroepdonor (ATP of verwant) om twee verschillende acceptormoleculen te fosforyleren. Voorbeelden van deze enzymen zijn pyruvaatfosfaat dikinase (PPDK) en fosfoglycaan water dikinase..
Fosfotransferasen die aminozuurresiduen van verschillende soorten eiwitten fosforyleren
EC 2.7.10: proteïne-tyrosinekinasen
Eiwit-tyrosinekinasen zijn enzymen die de overdracht van fosfaatgroepen specifiek naar tyrosineresiduen in polypeptideketens van verschillende typen eiwitacceptoren katalyseren..
EC 2.7.11: proteïne-serine / threonine kinasen
Net als proteïne-tyrosinekinasen katalyseert deze groep enzymen de overdracht van fosfaatgroepen naar serine- of threonineresiduen in andere eiwitten..
Een bekend voorbeeld van deze eiwitten is de familie van proteïnekinasen C, die deelnemen aan meerdere routes, maar vooral in het lipidenmetabolisme..
Ook inbegrepen in deze groep zijn veel cyclische AMP en cyclische GMP-afhankelijke proteïnekinasen, met belangrijke implicaties voor celdifferentiatie, groei en communicatie..
EC 2.7.12: kinasen hebben een dubbele specificiteit (die kunnen werken op zowel serine / threonine- als tyrosineresiduen)
Mitogeen-geactiveerde proteïnekinasekinasen (MAPKK) maken deel uit van deze groep enzymen die in staat zijn om uitwisselbaar serine-, treonine- of tyrosineresiduen van andere proteïnekinasen te fosforyleren..
Eiwit-histidinekinasen (EC 2.7.13) en eiwit-arginine-kinasen (EC 2.7.14)
Er zijn andere proteïnekinasen die in sommige soorten proteïnen fosfaatgroepen kunnen overbrengen naar histidine- en arginineresiduen en dit zijn de proteïne-histidinekinasen en de proteïne-argininekinasen..
Andere vormen van classificatie
Volgens verschillende auteurs kunnen kinasen beter worden geclassificeerd volgens het type substraat dat ze gebruiken als fosfaatgroepacceptor..
Anderen zijn van mening dat de beste manier om deze enzymen te classificeren is op basis van de structuur en kenmerken van hun actieve site, dat wil zeggen volgens de conformatie en aanwezigheid van ionen of bepaalde moleculen erin..
Afhankelijk van het type substraat kunnen kinasen worden geclassificeerd als proteïnekinasen (die andere proteïnen fosforyleren), lipidekinasen (die lipiden fosforyleren), koolhydraatkinases (die verschillende soorten koolhydraten fosforyleren), nucleosidefosforylasen (die nucleosiden fosforyleren), enz..
Kenmerken
Enzymen van de kinasegroep zijn alomtegenwoordig van aard en een enkele cel kan honderden verschillende typen herbergen en reacties op meerdere cellulaire routes katalyseren..
De functies kunnen zeer divers zijn:
-Ze nemen deel aan meerdere cellulaire signalerings- en communicatieprocessen, in het bijzonder proteïnekinasen, die de opeenvolgende fosforylering van andere proteïnekinasen (fosforyleringscascades) katalyseren als reactie op interne en externe stimuli..
-Sommige van deze eiwitten met enzymatische activiteit hebben centrale functies in het metabolisme van koolhydraten, lipiden, nucleotiden, vitamines, cofactoren en aminozuren. Niets anders bij glycolyse omvat bijvoorbeeld ten minste 4 kinasen: hexokinase, fosfofructokinase, fosfoglyceraatkinase en pyruvaatkinase..
-Onder de signaleringsfuncties zijn kinasen betrokken bij de processen van regulatie van genexpressie, spiercontractie en resistentie tegen antibiotica in verschillende soorten levende organismen.
-Eiwit-tyrosinekinasen spelen een rol bij de regulatie van vele signaaltransductieroutes die gerelateerd zijn aan ontwikkeling en communicatie in meercellige metazoanen..
-De modificatie van eiwitten door fosforylering (in andere cellulaire contexten dan cellulaire signalering) is een belangrijk element bij het reguleren van de activiteit van een groot aantal enzymen die deelnemen aan verschillende metabolische processen. Dit is het voorbeeld van celcyclusregulatie door veel kinase-afhankelijke cycline-eiwitten..
-De kinasen die lipiden kunnen fosforyleren, zijn essentieel voor de hermodelleringprocessen van celmembranen, evenals voor de synthese en vorming van nieuwe membranen..
Referenties
- Cheek, S., Zhang, H., & Grishin, N. V. (2002). Volgorde en structuurclassificatie van kinasen. Journal of Molecular Biology, 2836(02), 855-881.
- Cooper, J. (2018). Encyclopaedia Britannica. Opgehaald van britannica.com
- Da Silva, G. (2012). Vooruitgang in proteïnekinasen. Rijeka, Kroatië: InTech Open.
- Krebs, E. (1983). Historische perspectieven op proteïnefosforylering en een classificatiesysteem voor proteïnekinasen. Phil. Trans. R. Soc. Lond. B, 302, 3-11.
- Krebs, E. (1985). De fosforylering van eiwitten: een belangrijk mechanisme voor biologische regulatie. Biochemical Society-transacties, 13, 813-820.
- Nomenclatuurcomité van de Internationale Unie voor Biochemie en Moleculaire Biologie (NC-IUBMB). (2019). Opgehaald van qmul.ac.uk


Niemand heeft nog op dit artikel gereageerd.