
Epimers kenmerken, formatie en voorbeelden
De epimeren het zijn diastereoisomeren waarin slechts één van hun achirale centra verschilt in ruimtelijke configuratie; in tegenstelling tot enantiomeren, waar alle achirale centra verschillende configuraties hebben en een paar spiegelbeelden vertegenwoordigen die niet op elkaar kunnen worden gelegd.
De rest van de diastereoisomeren (bijvoorbeeld geometrische isomeren) kunnen meer dan twee centra hebben met verschillende configuraties. Daarom zijn een groot percentage stereo-isomeren diastereo-isomeren; terwijl epimeren veel minder zijn, maar daarom niet minder belangrijk.
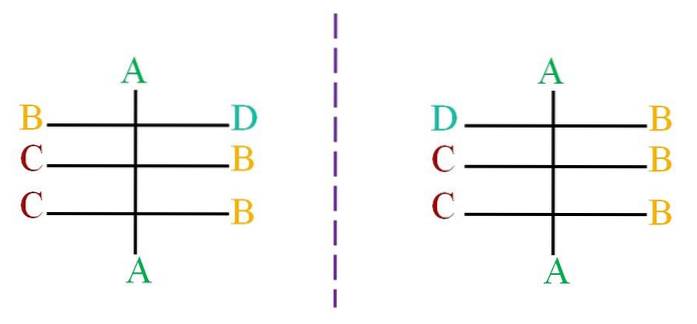
Veronderstel een structuur met een skelet van zwarte atomen gekoppeld aan de letters A, B, C en D (bovenste afbeelding). De stippellijn stelt de spiegel voor en laat zien dat het paar moleculen hierboven geen enantiomeren zijn, aangezien al hun chirale centra dezelfde configuratie hebben; behalve het eerste centrum, gekoppeld aan de letters B en D.
Het molecuul aan de linkerkant heeft de letter D naar de rechterkant gericht, terwijl de molecuulletter D aan de rechterkant naar de linkerkant is gericht. Gebruik het Cahn-Ingold-Prelog-systeem (R-S) om te weten wat de configuratie van elk zal zijn.
Artikel index
- 1 Kenmerken van epimeren
- 2 Opleiding
- 2.1 Tautomerisatie
- 3 voorbeelden
- 3.1 Glucose-anomeren
- 3.2 Isomeren van menthol
- 4 referenties
Kenmerken van epimeren
Het belangrijkste kenmerk van epimeren ligt uitsluitend in een achiraal (of stereogeen) centrum. Het veranderen van de ruimtelijke oriëntatie van D en B kan leiden tot stabielere of onstabiele conformeren; dat wil zeggen, de rotaties van de enkele bindingen zorgen ervoor dat twee atomen of groepen volumineuze atomen elkaar ontmoeten of weggaan.
Vanuit dit perspectief kan de ene epimeer veel stabieler zijn dan de andere. Degene die, door zijn bindingen te roteren, stabielere structuren genereert, zal het epimeer zijn met de grootste neiging om zich in evenwicht te vormen..
Terugkomend op de letters, D en B kunnen erg omvangrijk zijn, terwijl C een klein atoom is. Daarom is het epimeer aan de rechterkant stabieler, aangezien D en C links van de eerste twee centra minder sterische hinder ondervinden..
Microscopisch wordt dit een kenmerk van het beschouwde epimerenpaar; maar macroscopisch worden de verschillen geaccentueerd en hebben ze bijvoorbeeld verschillende smeltpunten, brekingsindices, NMR-spectra (naast vele andere eigenschappen).
Maar op het gebied van biologie en enzymgekatalyseerde reacties, is dit waar epimeren nog meer verschillen; de ene kan door het lichaam worden gemetaboliseerd, de andere niet.
Opleiding
Hoe worden epimeren gevormd? Door een chemische reactie die epimerisatie wordt genoemd. Als beide epimeren niet veel verschillen in stabiliteit, wordt een epimerisatie-evenwicht tot stand gebracht, wat niets meer is dan een onderlinge omzetting:
EpA <=> EpB
Waar EpA epimeer A is en EpB epimeer B. Als een van hen veel stabieler is dan de andere, zal het een hogere concentratie hebben en wat bekend staat als mutarotatie; dat wil zeggen, het zal in staat zijn om de richting van een gepolariseerde lichtbundel te veranderen.
Epimerisatie is mogelijk geen evenwicht en daarom onomkeerbaar. In deze gevallen wordt een racemisch mengsel van EpA / EpB-diastereoisomeren verkregen..
De syntheseroute van de epimeren varieert afhankelijk van de betrokken reagentia, het reactiemedium en de procesvariabelen (gebruik van katalysatoren, druk, temperatuur, enz.).
Om deze reden moet de vorming van elk paar epimeren afzonderlijk van de andere worden bestudeerd; elk met zijn eigen chemische mechanismen en systemen.
Tautomerisatie
Van alle epimeervormingsprocessen kan de tautomerisatie van twee diastereoisomeren als een algemeen voorbeeld worden beschouwd..
Dit bestaat uit een evenwicht waarbij het molecuul een keton (C = O) of enol (C-OH) vorm aanneemt. Zodra de ketonvorm opnieuw is omgezet, verandert de configuratie van de koolstof naast de carbonylgroep (indien chiraal), waardoor een paar epimeren ontstaat.
Een voorbeeld van het bovenstaande is het cis-decalon- en trans-decalon-paar.
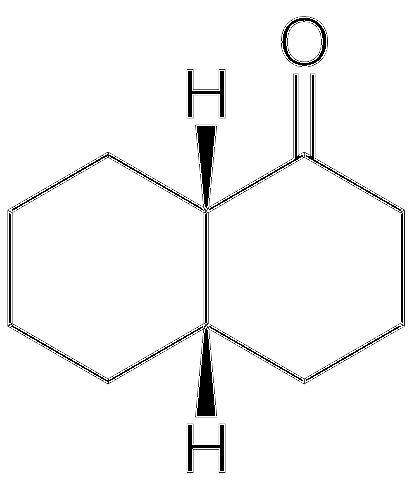
De structuur van cis-decalon is hierboven weergegeven. De H-atomen bevinden zich bovenaan de twee ringen; terwijl in de trans-decalone de ene zich boven de ringen bevindt en de andere eronder. De koolstof aan de linkerkant van de C = O-groep is het chirale centrum en daarom degene die de epimeren onderscheidt.
Voorbeelden
Glucose-anomeren
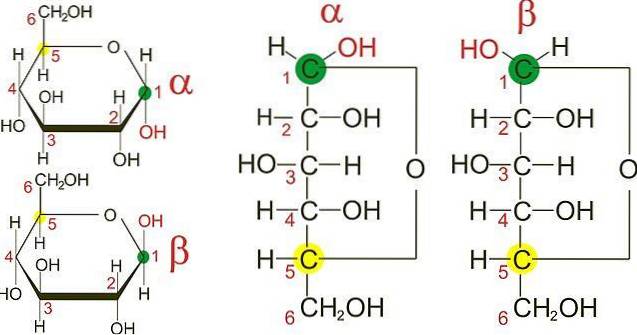
De bovenste afbeelding toont de furaanringen van de twee anomeren van D-glucose: α en β. Aan de ringen is te zien dat de OH-groepen op koolstof 1 ofwel in dezelfde richting worden gevonden als de aangrenzende OH, in het α-anomeer, of in tegengestelde richtingen, zoals in het β-anomeer..
De Fisher-projecties van beide anomeren (aan de rechterkant van de afbeelding) maken het verschil tussen de twee epimeren, die zelf anomeren zijn, nog duidelijker. Twee α-anomeren kunnen echter verschillende ruimtelijke configuraties hebben op een van de andere koolstofatomen en daarom epimeren zijn..
In de C-1 van de Fisher-projectie voor de α-anomeer "kijkt" de OH-groep naar rechts, terwijl hij in de β-anomeer naar links "kijkt"..
Isomeren van menthol

In de afbeelding heb je alle stereo-isomeren van het mentholmolecuul. Elke kolom vertegenwoordigt een paar enantiomeren (let goed op), terwijl de rijen overeenkomen met de diastereoisomeren.
Dus wat zijn epimeren? Het moeten die zijn die nauwelijks verschillen in de ruimtelijke positie van een enkele koolstof..
(+) - menthol en (-) - neoisomenthol zijn epimeren en bovendien diastereoisomeren (ze staan niet in dezelfde kolom). Indien gedetailleerd waargenomen, zowel in de -OH- als -CH-groepen3 komen uit het vlak (boven de ring), maar in de (-) - neoisomenthol wijst de isopropylgroep ook uit het vlak.
Niet alleen (+) - menthol is epimeer van (-) - neoisomenthol, maar ook (+) - neomenthol. Dit laatste verschilt alleen doordat de groep -CH3 wijst naar beneden in het vliegtuig. Andere epimeren zijn:
-(-) - isomenthol en (-) - neomenthol
-(+) - isomenthol en (+) - neomenthol
-(+) - neoisomenthol en (-) - neomenthol
-(+) - neomenthol en (-) - neoisomenthol
Deze stereo-isomeren vormen een praktisch voorbeeld om het concept van epimeren te verduidelijken, en je kunt zien dat veel van verschillende diastereo-isomeren alleen kunnen differentiëren tot een enkele asymmetrische of chirale koolstof..
Referenties
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organische chemie. (10th editie.). Wiley plus.
- Carey F. (2008). Organische chemie. (Zesde editie). Mc Graw Hill.
- Uruguay Educa klaslokalen. (s.f.). Epimers. Hersteld van: aulas.uruguayeduca.edu.uy
- Wikipedia. (2018). Epimer. Hersteld van: en.wikipedia.org/wiki/Epimer
- Fray J. M. (2014). Onderzoek naar de vorming van epimer in amidekoppelingsreacties: een experiment voor gevorderde studenten. School of Chemistry, University of Nottingham, University Park, Nottingham NG7 2RD, Verenigd Koninkrijk. J. Chem. Educ. 2014, 91, 1, 136-140
- Reist & col. (negentienvijfennegentig). Racemisatie, enantiomerisatie, diastereomerisatie en epimerisatie: hun betekenis en farmacologische betekenis. Chiraliteit 7: 396-400.



Niemand heeft nog op dit artikel gereageerd.