
Sfingomyeline-structuur, functies, synthese en metabolisme
De sfingomyeline het is het meest voorkomende sfingolipide in dierlijke weefsels: zijn aanwezigheid is gevonden in alle celmembranen die tot nu toe zijn onderzocht. Het heeft structurele overeenkomsten met fosfatidylcholine in termen van de polaire kopgroep, daarom is het ook geclassificeerd als een fosfolipide (fosfosfingolipide).
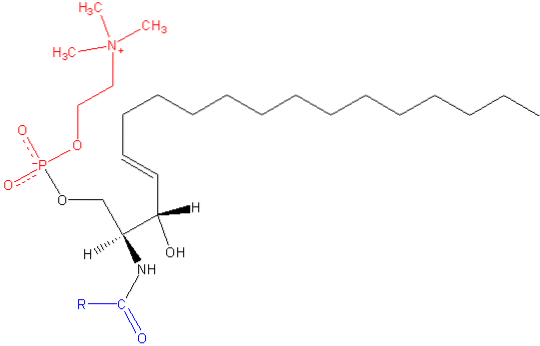
In de jaren 1880 isoleerde wetenschapper Johann Thudichum een in ether oplosbare lipidecomponent uit hersenweefsel en noemde het sfingomyeline. Later, in 1927, werd de structuur van dit sfingolipide gerapporteerd als N-acyl-sfingosine-1-fosfocholine.
Net als de andere sfingolipiden heeft sfingomyeline zowel structurele als celsignaleringsfuncties, en komt het vooral voor in zenuwweefsel, met name in myeline, een omhulsel dat de axonen van bepaalde neuronen bedekt en isoleert..
De distributie ervan is bestudeerd door middel van subcellulaire fractionering en enzymatische afbraakexperimenten met sfingomyelinases, en de resultaten geven aan dat meer dan de helft van de sfingomyeline in eukaryote cellen wordt aangetroffen in het plasmamembraan. Dit hangt echter af van het celtype. In fibroblasten is het bijvoorbeeld goed voor bijna 90% van de totale lipiden.
De ontregeling van de synthese- en metabolismeprocessen van dit lipide leidt tot de ontwikkeling van complexe pathologieën of lipidose. Een voorbeeld hiervan is de erfelijke ziekte van Niemann-Pick, gekenmerkt door hepatosplenomegalie en progressieve neurologische disfunctie.
Artikel index
- 1 Structuur
- 2 functies
- 2.1 -Signage
- 2.2 -Structuur
- 3 Synthese
- 4 Metabolisme
- 5 referenties
Structuur
Sfingomyeline is een amfipatisch molecuul dat bestaat uit een polaire kop en twee apolaire staarten. De polaire kopgroep is een fosfocholinemolecuul, dus het kan lijken op glycerofosfolipide fosfatidylcholine (PC). Er zijn echter aanzienlijke verschillen met betrekking tot het grensvlak en het hydrofobe gebied tussen deze twee moleculen..
De meest voorkomende base in een sfingomyeline-molecuul van zoogdieren is ceramide, bestaande uit sfingosine (1,3-dihydroxy-2-amino-4-octadeceen), dat een dubbele binding heeft in trans tussen de koolstofatomen op posities 4 en 5 van de koolwaterstofketen. Het verzadigde derivaat, sfinganine, komt ook veel voor, maar wordt in mindere mate aangetroffen.
De lengte van de hydrofobe staarten van sfingomyeline varieert van 16 tot 24 koolstofatomen en de vetzuursamenstelling varieert afhankelijk van het weefsel.
De sfingomyelines van de witte stof van de menselijke hersenen bevatten bijvoorbeeld nervonzuur, die van de grijze stof bevatten voornamelijk stearinezuur en de meest voorkomende vorm in bloedplaatjes is arachidonaat..
Er is over het algemeen een ongelijkheid in lengte tussen de twee vetzuurketens van sfingomyeline, wat "interdigitatiefenomenen" tussen koolwaterstoffen in tegenovergestelde monolagen lijkt te bevorderen. Dit geeft het membraan speciale stabiliteit en bijzondere eigenschappen in vergelijking met andere membranen die slechter zijn aan dit sfingolipide..
In het grensvlakgebied van het molecuul heeft sfingomyeline een amidegroep en een vrije hydroxylgroep op koolstof 3, die kunnen dienen als donoren en acceptoren van waterstofbindingen voor intra- en intermoleculaire bindingen, belangrijk bij de definitie van nevendomeinen en interactie met verschillende soorten moleculen.
Kenmerken
-Signalering
De producten van het sfingosinemetabolisme -ceramide, sfingosine, sfingosine-1-fosfaat en diacylglycerol- zijn belangrijke cellulaire effectoren en geven het een rol bij meerdere cellulaire functies, zoals apoptose, ontwikkeling en veroudering, celsignalering, onder anderen..
-Structuur
Dankzij de driedimensionale "cilindrische" structuur van sfingomyeline, kan dit lipide compactere en geordende membraandomeinen vormen, wat belangrijke functionele implicaties heeft vanuit het oogpunt van eiwitten, aangezien het specifieke domeinen kan vaststellen voor sommige integrale membraaneiwitten..
In lipide "vlotten" en caveolae
Lipide-vlotten, membraanfasen of geordende microdomeinen van sfingolipiden zoals sfingomyeline, sommige glycerofosfolipiden en cholesterol, vertegenwoordigen stabiele platforms voor de associatie van membraaneiwitten met verschillende functies (receptoren, transporters, enz.).
Caveolae zijn invaginaties van het plasmamembraan die eiwitten rekruteren met GPI-ankers en die ook rijk zijn aan sfingomyeline.
Met betrekking tot cholesterol
Cholesterol heeft, vanwege zijn structurele stijfheid, een aanzienlijke invloed op de structuur van celmembranen, vooral in aspecten die verband houden met vloeibaarheid, en daarom wordt het als een essentieel element beschouwd.
Omdat sfingomyelines zowel donoren als acceptoren van waterstofbindingen bezitten, wordt aangenomen dat ze in staat zijn om meer "stabiele" interacties te vormen met cholesterolmoleculen. Daarom wordt er gezegd dat er een positieve correlatie bestaat tussen de niveaus van cholesterol en sfingomyeline in de membranen..
Synthese
De synthese van sfingomyeline vindt plaats in het Golgi-complex, waar het ceramide dat uit het endoplasmatisch reticulum (ER) wordt getransporteerd, wordt gemodificeerd door de overdracht van een fosfocholinemolecuul uit fosfatidylcholine, met de gelijktijdige afgifte van een diacylglycerolmolecuul. De reactie wordt gekatalyseerd door SM-synthase (ceramide: fosfatidylcholine fosfocholine transferase).
Er is ook een andere route voor de productie van sfingomyeline die kan plaatsvinden door een fosfoethanolamine over te brengen van fosfatidylethanolamine (PE) naar ceramide, met daaropvolgende fosfoethanolamine-methylering. Aangenomen wordt dat dit vooral belangrijk is in sommige PE-rijke zenuwweefsels..
Sfingomyeline-synthase wordt gevonden aan de luminale zijde van het Golgi-complexmembraan, wat consistent is met de extra cytoplasmatische locatie van sfingomyeline in de meeste cellen.
Vanwege de kenmerken van de polaire groep van sfingomyeline en de schijnbare afwezigheid van specifieke translocases, hangt de topologische oriëntatie van dit lipide af van het enzymsynthase..
Metabolisme
Afbraak van sfingomyeline kan optreden in zowel het plasmamembraan als in de lysosomen. Lysosomale hydrolyse tot ceramide en fosfocholine is afhankelijk van zure sfingomyelinase, een oplosbaar lysosomaal glycoproteïne waarvan de activiteit een optimale pH heeft van ongeveer 4,5.
Hydrolyse in het plasmamembraan wordt gekatalyseerd door een sfingomyelinase dat werkt bij pH 7,4 en waarvoor tweewaardige magnesium- of mangaanionen nodig zijn voor de werking ervan. Andere enzymen die betrokken zijn bij het metabolisme en de recycling van sfingomyeline worden aangetroffen in verschillende organellen die met elkaar verbonden zijn via vesiculaire transportroutes..
Referenties
- Barenholz, Y., en Thompson, T. E. (1999). Sfingomyeline: biofysische aspecten. Chemie en fysica van lipiden, 102, 29-34.
- Kanfer, J., en Hakomori, S. (1983). Sfingolipiden biochemie. (D. Hanahan, red.), Handboek van lipidenonderzoek 3 (1e ed.). Plenum Press.
- Koval, M., en Pagano, R. (1991). Intracellulair transport en metabolisme van sfingomyeline. Biochimic, 1082, 113-125.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H., Martin, K. (2003). Moleculaire celbiologie (5e ed.). Freeman, W. H. & Company.
- Millat, G., Chikh, K., Naureckiene, S., Sleat, D. E., Fensom, A. H., Higaki, K.,… Vanier, M. T. (2001). Ziekte van Niemann-Pick Type C: spectrum van HE1-mutaties en genotype / fenotype-correlaties in de NPC2-groep. Am. J. Hum. Genet., 69, 1013-1021.
- Ramstedt, B., en Slotte, P. (2002). Membraaneigenschappen van sfingomyelines. FEBS Letters, 531, 33-37.
- Slotte, P. (1999). Sfingomyeline - cholesterolinteracties in biologische en modelmembranen. Chemie en fysica van lipiden, 102, 13-27.
- Vance, J. E., & Vance, D. E. (2008). Biochemie van lipiden, lipoproteïnen en membranen. In Nieuwe uitgebreide biochemie Vol.36 (4e ed.). Elsevier.


Niemand heeft nog op dit artikel gereageerd.