
Methoxyethaan structuur, eigenschappen, verkrijgen, gebruik, risico's

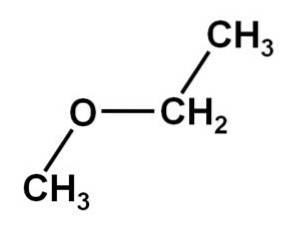
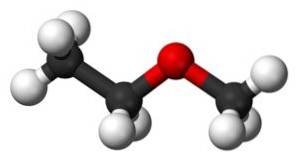
De methoxyethaan Het is een organische verbinding uit de familie van ethers of alkoxiden. De chemische formule is CH3OCHtweeCH3. Het wordt ook methylethylether of ethylmethylether genoemd. Het is een gasvormige verbinding bij kamertemperatuur en het molecuul heeft twee methylgroepen -CH3, de ene direct gehecht aan zuurstof en de andere aan ethyl-CHtweeCH3.
Methoxyethaan is een kleurloos gas, oplosbaar in water en mengbaar met ether en ethylalcohol. Omdat het een ether is, is het een laag-reactieve verbinding, maar het kan bij hoge temperaturen reageren met sommige geconcentreerde zuren..
Het wordt in het algemeen verkregen door de zogenaamde Williamson-synthese, die het gebruik van een natriumalkoxide en een alkyljodide omvat. Op zijn beurt is de afbraak ervan onder verschillende omstandigheden bestudeerd.
Methoxyethaan wordt gebruikt in onderzoekslaboratoria met verschillende doeleinden, bijvoorbeeld bij de studie van halfgeleidende nanomaterialen of bij de observatie van interstellaire materie in sterrenbeelden en grote moleculaire wolken van het heelal..
Dankzij zeer gevoelige telescopen (interferometers) is het zelfs op bepaalde plaatsen in de interstellaire ruimte gedetecteerd..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Fysieke eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Kookpunt
- 3.5 Vlampunt
- 3.6 Zelfontbrandingstemperatuur
- 3.7 Soortelijk gewicht
- 3.8 Brekingsindex
- 3.9 Oplosbaarheid
- 4 Chemische eigenschappen
- 4.1 Warmteafbraak
- 4.2 Fotosensibilisatie
- 5 Verkrijgen
- 6 Locatie in het universum
- 7 Gebruik van methoxyethaan
- 7.1 Voor onderzoek naar interstellaire materie
- 7.2 Chemische omzettingen in verschillende vakgebieden afleiden
- 7.3 Potentieel gebruik in halfgeleiders
- 8 Risico's
- 9 referenties
Structuur
De methoxyethaanverbinding heeft een methylgroep -CH3 en een ethylgroep -CHtweeCH3 beide gehecht aan een zuurstof.
Zoals te zien is, zijn er in dit molecuul twee methylgroepen, een gehecht aan de zuurstof CH3-O en de andere behorende tot ethyl -CHtwee-CH3.
In de grond of lagere energietoestand de methylgroep van -CHtwee-CH3 is in positie trans met betrekking tot methyl gebonden aan zuurstof, dat wil zeggen op een diametraal tegenovergestelde plaats, met als referentie de CH-bindingtwee-O. Dit is waarom het soms wordt genoemd trans-ethylmethylether.
Dit molecuul kan een verdraaiing ondergaan bij de CH-bindingtwee-Of, die de methyl in een andere ruimtelijke positie plaatst dan de trans , methylgroepen -CH3 zijn zeer dicht bij elkaar en deze torsie genereert een energietransitie die detecteerbaar is met gevoelige instrumenten.
Nomenclatuur
- Methoxyethaan.
- Methylethyl ether.
- trans-Ethylmethylether (voornamelijk in Engelstalige literatuur, vertaling uit het Engels trans-ethylmethylether.
Fysieke eigenschappen
Fysieke toestand
Kleurloos gas
Molecuulgewicht
60,096 g / mol
Smeltpunt
-113,0 ºC
Kookpunt
7,4 ºC
Vlampunt
1,7 ºC (methode met gesloten kroes).
Zelfontbranding temperatuur
190 ºC
Specifiek gewicht
0,7251 bij 0 ºC / 0 ºC (het is minder dicht dan water maar zwaarder dan lucht).
Brekingsindex
1.3420 bij 4 ºC
Oplosbaarheid
Oplosbaar in water: 0,83 mol / L
Oplosbaar in aceton. Mengbaar met ethylalcohol en ethylether.
Chemische eigenschappen
Methoxyethaan is een ether, dus het is relatief niet-reactief. De koolstof-zuurstof-koolstof C-O-C-binding is zeer stabiel tegen basen, oxiderende en reductiemiddelen. Het wordt alleen afgebroken door zuren, maar het verloopt alleen onder zware omstandigheden, dat wil zeggen met geconcentreerde zuren en hoge temperaturen..
Het heeft echter de neiging te oxideren in aanwezigheid van lucht, waardoor onstabiele peroxiden ontstaan. Als de containers die het bevatten worden blootgesteld aan hitte of vuur, exploderen de containers heftig.
Warmte-ontleding
Wanneer methoxyethaan wordt verwarmd tussen 450 en 550 ° C, ontleedt het tot aceetaldehyde, ethaan en methaan. Deze reactie wordt gekatalyseerd door de aanwezigheid van ethyljodide, dat over het algemeen aanwezig is in laboratoriummonsters van methoxyethaan omdat het wordt gebruikt om het te verkrijgen..
Fotosensibilisatie
Methoxyethaan bestraald met een kwikdamplamp (2537 Å golflengte) ontleedt en genereert een grote verscheidenheid aan verbindingen, waaronder: waterstof, 2,3-dimethoxybutaan, 1-ethoxy-2-methoxypropaan en methylvinylether..
De eindproducten zijn afhankelijk van de bestralingstijd van het monster, aangezien naarmate de bestraling voortduurt, de aanvankelijk gevormde producten aanleiding geven tot nieuwe verbindingen..
Door de bestralingstijd te verlengen kunnen ook propaan, methanol, ethanol, aceton, 2-butanon, koolmonoxide, ethyl-n-propylether en methyl-sec-butylether worden gevormd..
Het verkrijgen van
Omdat het een niet-symmetrische ether is, kan methoxyethaan worden verkregen door de reactie tussen natriummethoxide CH3ONa en ethyljodide CH3CHtweeI. Dit type reactie wordt een Williamson-synthese genoemd.
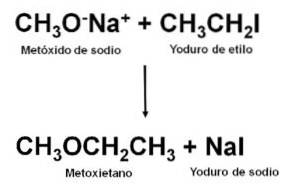
Nadat de reactie is uitgevoerd, wordt het mengsel gedestilleerd om de ether te verkrijgen.
Het kan ook worden verkregen met natriumethoxide CH3CHtweeONa en methylsulfaat (CH3tweeSW4.
Locatie in het universum
De trans-Ethylmethylether is gedetecteerd in het interstellaire medium in regio's zoals het Orion-sterrenbeeld KL en in de gigantische moleculaire wolk W51e2.

De detectie van deze verbinding in de interstellaire ruimte, samen met de analyse van zijn overvloed, helpt bij het bouwen van modellen van interstellaire chemie..
Maakt gebruik van methoxyethaan
Methoxyethaan of methylethylether wordt meestal gebruikt in laboratoriumexperimenten voor wetenschappelijk onderzoek.
Voor studies over interstellaire materie
Omdat methoxyethaan een organisch molecuul is met interne rotaties, is het een chemische verbinding die van belang is voor onderzoek naar interstellaire materie..
De interne rotaties van zijn methylgroepen produceren energie-overgangen in het microgolfgebied.
Daarom kunnen ze worden gedetecteerd door zeer gevoelige telescopen zoals het Atacama Large Millimeter / submillimeter Ensemble of ALMA. Atacama Grote millimeter / submillimeter-array.

Dankzij de interne rotatie en de grote ruimteobservatoria is de trans-Methylethyl ether is gevonden in het sterrenbeeld Orion en in de gigantische moleculaire wolk W51e2.
Chemische transformaties in verschillende vakgebieden afleiden
Sommige onderzoekers observeerden de vorming van methoxyethaan of methylethylether wanneer een mengsel van ethyleen CH wordt bestraald met elektronen.twee= CHtwee en methanol CH3Oh.
Het reactiemechanisme verloopt via de vorming van de radicale CH3O •, dat de elektronenrijke dubbele binding van CH aanvalttwee= CHtwee. Het resulterende adduct CH3-O-CHtwee-CHtwee• vangt een waterstof op uit een CH3OH en vormt de methylethylether CH3-O-CHtwee-CH3.
De studie van dit soort reacties geïnduceerd door de bestraling van elektronen is nuttig op het gebied van biochemie, aangezien is vastgesteld dat ze schade aan het DNA kunnen veroorzaken, of op het gebied van organometaalchemie omdat het de vorming van nanostructuren bevordert..
Bovendien is bekend dat grote hoeveelheden secundaire elektronen worden geproduceerd wanneer elektromagnetische of deeltjesvormige straling in wisselwerking staat met gecondenseerde materie in de ruimte..
Daarom wordt geschat dat deze elektronen chemische transformaties kunnen initiëren in interstellair stof. Vandaar het belang van het bestuderen van methylethyl ether in deze reacties..
Potentieel gebruik in halfgeleiders
Door middel van computationele berekeningsmethoden ontdekten sommige wetenschappers dat methoxyethaan of methylethylether kan worden geadsorbeerd door grafeen gedoteerd met gallium (Ga) (merk op dat adsorptie verschilt van absorptie).
Grafeen is een nanomateriaal dat bestaat uit koolstofatomen die in een hexagonaal patroon zijn gerangschikt..

De adsorptie van methoxyethaan op gedoteerd grafeen vindt plaats door de interactie tussen de zuurstof in de ether en het galliumatoom op het oppervlak van het nanomateriaal. Door deze adsorptie is er een netto ladingsoverdracht van ether naar gallium..
Na adsorptie van methylethyl ether en door deze ladingsoverdracht vertoont gallium-gedoteerd grafeen p-type halfgeleider eigenschappen.
Risico's
Methoxyethaan is licht ontvlambaar.
Bij contact met lucht heeft het de neiging om onstabiele en explosieve peroxiden te vormen.
Referenties
- ONS. Nationale bibliotheek van geneeskunde. (2019). Ethyl methylether. Hersteld van: pubchem.ncbi.nlm.nih.gov.
- Irvine W.M. (2019) Ethylmethylether (C.tweeH.5OCH3In: Gargaud M. et al. (eds). Encyclopedia of Astrobiology. Springer, Berlijn, Heidelberg. Opgehaald van link.springer.com.
- Ten derde, B. et al. (2015). Zoeken naar trans-ethylmethylether in Orion KL. Astronomie en astrofysica. 582, L1 (2015). Opgehaald van ncbi.nlm.nih.gov.
- Filseth, S.V. (1969). De Mercury 6 (3P.1) Fotosensibilisatie van methylethylether. The Journal of Physical Chemistry. Jaargang 73, nummer 4, april 1969, 793-797. Opgehaald van pubs.acs.org.
- Casanova, J.Jr. (1963). Student Voorbereiding en manipulatie van een gas-methylethyl ether. Journal of Chemical Education. Jaargang 40, nummer 1, januari 1963. Opgehaald van pubs.acs.org.
- Ure, W. en Young, J.T. (1933a). Over het mechanisme van gasvormige reacties. I. De thermische ontleding van methylethylether. The Journal of Physical Chemistry, deel XXXVII, nr. 9: 1169-1182. Opgehaald van pubs.acs.org.
- Ure, W. en Young, J.T. (1933b). Over het mechanisme van gasvormige reacties. II. Homogene katalyse bij de afbraak van methylethylether. The Journal of Physical Chemistry, 37, 9, 1183-1190. Opgehaald van pubs.acs.org.
- Shokuhi Rad, A. et al. (2017). DFT-onderzoek naar de adsorptie van diethyl-, ethylmethyl- en dimethylethers op het oppervlak van met gallium gedoteerd grafeen. Toegepaste Surface Science. Volume 401, 15 april 2017, pagina's 156-161. Opgehaald van sciencedirect.com.
- Schmidt, F. et al. (2019). Door elektronen geïnduceerde vorming van ethylmethylether in gecondenseerde mengsels van methanol en ethyleen. J. Phys. Chem. A 2019, 123, 1, 37-47. Opgehaald van pubs.acs.org.



Niemand heeft nog op dit artikel gereageerd.