
Wat is vervluchtiging?

De vervluchtiging is het proces waarbij een chemische stof wordt omgezet van een vloeibare of vaste toestand naar een gasvormige of dampvormige toestand. Andere termen die worden gebruikt om hetzelfde proces te beschrijven, zijn verdamping, destillatie en sublimatie..
De ene stof kan vaak van de andere worden gescheiden door vervluchtiging en kan vervolgens worden teruggewonnen door dampcondensatie..

De stof kan sneller vervluchtigen door deze te verwarmen om de dampspanning te verhogen of door de damp te verwijderen met behulp van een inerte gasstroom of een vacuümpomp..
Verwarmingsprocedures omvatten vervluchtiging van water, kwik of arseentrichloride om deze stoffen te scheiden van storende elementen..
Chemische reacties worden soms gebruikt om vluchtige producten te produceren, zoals bij het vrijkomen van kooldioxide uit carbonaten, ammoniak bij de Kjeldahl-methode voor de bepaling van stikstof en zwaveldioxide bij de bepaling van zwavel in staal.
De vervluchtigingsmethoden worden over het algemeen gekenmerkt door grote eenvoud en bedieningsgemak, behalve wanneer hoge temperaturen of materialen nodig zijn die zeer corrosiebestendig zijn (Louis Gordon, 2014).
Verdamping van de dampspanning
Weet u dat de kooktemperatuur van water 100 ° C is, heeft u zich ooit afgevraagd waarom regenwater verdampt??
Is het 100 ° C? Zo ja, waarom word ik dan niet warm? Heb je je ooit afgevraagd wat het karakteristieke aroma geeft aan alcohol, azijn, hout of plastic? (Dampdruk, S.F.)
Verantwoordelijk voor dit alles is een eigenschap die bekend staat als dampspanning, de druk die wordt uitgeoefend door een damp die in evenwicht is met de vaste of vloeibare fase van dezelfde stof..
Ook de partiële druk van de stof in de atmosfeer op de vaste stof of vloeistof (Anne Marie Helmenstine, 2014).
Dampspanning is een maat voor de neiging van een materiaal om over te gaan naar de gasvormige of damptoestand, dat wil zeggen een maat voor de vluchtigheid van stoffen.
Naarmate de dampspanning toeneemt, des te groter het vermogen van de vloeistof of vaste stof om te verdampen, en dus vluchtiger is..
De dampspanning neemt toe met de temperatuur. De temperatuur waarbij de dampdruk op het oppervlak van een vloeistof gelijk is aan de druk die door de omgeving wordt uitgeoefend, wordt het kookpunt van de vloeistof genoemd (Encyclopædia Britannica, 2017).
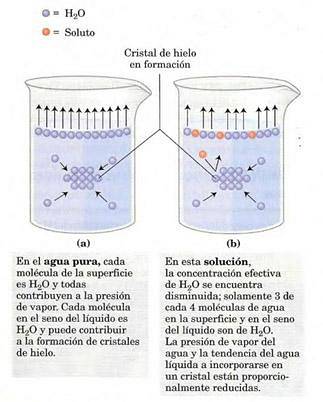
De dampspanning hangt af van de opgeloste stof die in oplossing is opgelost (het is een colligatieve eigenschap). Op het oppervlak van de oplossing (lucht-gasgrensvlak) hebben de meest oppervlakkige moleculen de neiging te verdampen, wisselen ze tussen fasen uit en genereren ze een dampspanning..
De aanwezigheid van opgeloste stof vermindert het aantal oplosmiddelmoleculen aan het grensvlak, waardoor de dampspanning afneemt..
De verandering in dampspanning kan worden berekend met de wet van Raoult voor niet-vluchtige opgeloste stoffen die wordt gegeven door:
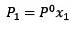
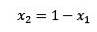
Waar X2 de molfractie van het oplosmiddel is. Als we beide kanten van de vergelijking vermenigvuldigen met P °, blijft het:
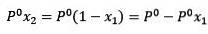
Het vervangen van (1) in (3) is:
(4)
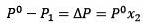
Dit is de variatie in dampspanning wanneer een opgeloste stof oplost (Jim Clark, 2017).
Gravimetrische analyse
Gravimetrische analyse is een klasse laboratoriumtechnieken die worden gebruikt om de massa of concentratie van een stof te bepalen door een verandering in massa te meten..
De chemische stof die we proberen te kwantificeren, wordt soms de analyt genoemd. We zouden gravimetrische analyse kunnen gebruiken om vragen te beantwoorden als:
- Wat is de concentratie van de analyt in een oplossing?
- Hoe puur is ons monster? Het monster hier kan een vaste stof of een oplossing zijn.
Er zijn twee veel voorkomende soorten gravimetrische analyse. Beide omvatten het veranderen van de fase van de analyt om deze te scheiden van de rest van een mengsel, wat leidt tot een verandering in massa..
Een van deze methoden is neerslaggravimetrie, maar degene waar we echt in geïnteresseerd zijn, is vervluchtigingsgravimetrie.
Vervluchtigingsgravimetrie is gebaseerd op het thermisch of chemisch ontleden van het monster en het meten van de resulterende verandering in zijn massa..
Als alternatief kunnen we een vluchtig afbraakproduct opvangen en wegen. Omdat het vrijkomen van een vluchtige soort een essentieel onderdeel is van deze methoden, classificeren we ze collectief als gravimetrische analysemethoden voor vervluchtiging (Harvey, 2016).
Gravimetrische analyseproblemen zijn gewoon stoichiometrieproblemen met een paar extra stappen.
Om een stoichiometrische berekening uit te voeren, hebben we de coëfficiënten van de uitgebalanceerde chemische vergelijking nodig.
Als een monster bijvoorbeeld bariumchloridedihydraat (BaCltwee● HtweeO), kan de hoeveelheid onzuiverheden worden verkregen door het monster te verwarmen om het water te verdampen.
Het verschil in massa tussen het originele monster en het verwarmde monster geeft ons in grammen de hoeveelheid water in het bariumchloride..
Met een eenvoudige stoichiometrische berekening wordt de hoeveelheid onzuiverheden in het monster verkregen (Khan, 2009).
Gefractioneerde destillatie
Gefractioneerde destillatie is een proces waarbij de componenten van een vloeibaar mengsel worden gescheiden in verschillende delen (fracties genoemd) op basis van hun verschillende kookpunten.
Het verschil in vluchtigheid van de verbindingen in het mengsel speelt een fundamentele rol bij hun scheiding..
Gefractioneerde destillatie wordt gebruikt om chemicaliën te zuiveren en ook om mengsels te scheiden om hun componenten te verkrijgen. Het wordt gebruikt als laboratoriumtechniek en in de industrie, waar het proces van groot commercieel belang is.
Dampen van een kokende oplossing worden door een hoge kolom geleid, een fractioneringskolom genoemd..
De kolom is gevuld met plastic of glasparels om de scheiding te verbeteren door meer oppervlakte te bieden voor condensatie en verdamping.
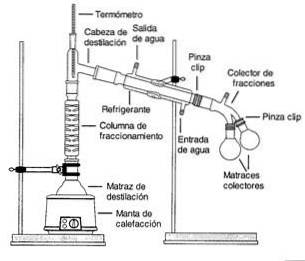
De temperatuur van de kolom neemt geleidelijk af over de lengte. Componenten met een hoger kookpunt condenseren in de kolom en keren terug naar oplossing.
Componenten met lagere kookpunten (meer vluchtig) passeren de kolom en worden bovenaan verzameld.
Theoretisch verbetert het hebben van meer kralen of platen de scheiding, maar het toevoegen van platen verhoogt ook de tijd en energie die nodig is om een destillatie te voltooien (Helmenstine, 2016)..
Referenties
- Anne Marie Helmenstine. (2014, 16 mei). Dampdruk definitie. Opgehaald van thoughtco.com.
- Encyclopædia Britannica. (2017, 10 februari). Dampdruk. Opgehaald van britannica.com.
- Harvey, D. (2016, 25 maart). Vervluchtiging Gravimetrie. Hersteld van chem.libretexts.
- Helmenstine, A. M. (2016, 8 november). Definitie en voorbeelden van fractionele destillatie. Opgehaald van thoughtco.com.
- Jim Clark, I. L. (2017, 3 maart). De wet van Raoult. Hersteld van chem.libretexts.
- Khan, S. (2009, 27 augustus). Inleiding tot gravimetrische analyse: gravimetrie van vervluchtiging. Opgehaald van khanacademy.
- Louis Gordon, R. W. (2014). Opgehaald van accessscience.com.
- Dampdruk. (S.F.). Opgehaald van chem.purdue.edu.



Niemand heeft nog op dit artikel gereageerd.