
Natriumsilicaat (Na2SiO3) structuur, eigenschappen, gebruik, risico's

De natriumsilicaat is een anorganische verbinding die wordt gevormd door twee natrium-Na-ionen+ en een silicaatanion SiO3twee-. Er wordt ook gezegd dat het bestaat uit een molecuul siliciumdioxide SiOtwee en een natriumoxide NatweeO. De chemische formule kan worden uitgedrukt als NatweeJa3 of ook NatweeOF.Jatwee.
De samenstelling van het natriumsilicaat kan echter variëren afhankelijk van de SiO-verhoudingtwee/ NatweeOfwel in gewicht of in moedervlekken. Het wordt ook wel oplosbaar silicaat of waterglas genoemd. Het kan worden verkregen in de vorm van poeder, grote kristalachtige stukjes of in de vorm van oplossingen.

Natriumsilicaat wordt veel gebruikt in wasmiddelen en zeep, omdat het het water verzacht en de reiniging effectiever maakt. Het maakt ook deel uit van producten zoals scheerschuim.
Het is de grondstof om SiO-silicakatalysatoren te bereidentwee. De oplossingen worden in veel toepassingen als lijm gebruikt, gaande van zelfklevend papier en karton tot glas, porselein, vuurvaste mallen, cement en schuurschijven..
Omdat het een volledig onbrandbaar materiaal is, wordt het gebruikt om brandwerende weefsels te maken, omdat het brandvertragend is en als coating voor beschermende uitrusting..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Dichtheid
- 3.5 Oplosbaarheid
- 3,6 pH
- 3.7 Chemische eigenschappen
- 3.8 Overige eigenschappen
- 4 Verkrijgen
- 5 toepassingen
- 5.1 In zeep en wasmiddelen
- 5.2 In katalysatoren en silicagels
- 5.3 Als lijm of lijm
- 5.4 In boorvloeistoffen voor oliebronnen
- 5.5 In verschillende toepassingen
- 6 Risico's
- 7 referenties
Structuur
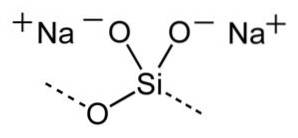
De algemene formule voor natriumsilicaten is xSiOtwee/ NatweeOf waar x de molaire of gewichtsverhouding is.
Molaire verhouding betekent aantal mol SiOtwee gedeeld door het aantal mol NatweeO. Gewichtsverhouding betekent het gewicht van SiOtwee gedeeld door het gewicht van NatweeOF.
Meer alkali (NatweeO) de molaire of gewichtsverhouding wordt gewijzigd.
Een natriumsilicaatoplossing met een lage molaire verhouding, bijvoorbeeld 1/1 (1 mol SiOtwee en 1 mol NatweeO) bevat voornamelijk SiO-monomeren44- en S-dimerentweeOF5twee- naast de Na-ionen+.
Een oplossing met een hoge molaire verhouding zoals 3,3 / 1 (3,3 mol SiOtwee voor elke mol NatweeO) heeft een hoog gehalte aan polymere soorten of polymeren van silicium en zuurstof.
Nomenclatuur
-Natriumsilicaat
-Natriummetasilicaat
-Oplosbaar glas
-Glas water (uit het Engels water glas
-Oplosbaar silicaat
Eigendommen
Fysieke toestand
-Stevig in grote stukken die lijken op blauwgroene kristallen
-Kleurloze tot witte poederachtige vaste stof
-Kleurloze waterige oplossingen.
Molecuulgewicht
Uit de formule NatweeJa3: 122,063 g / mol.
Smeltpunt
NatweeJa3: 1089 ° C
Dichtheid
Het hangt af van de SiO-verhoudingtwee/ NatweeOF.
Oplosbaarheid
In de vorm van grote stukjes groenachtig kristal is het oplosbaar in water bij verhitting en onder hoge druk. Het poeder is iets beter oplosbaar, maar in beide gevallen hangt de oplosbaarheid af van de hoeveelheid natrium of NatweeOf dat het bezit.
Hoe hoger het natriumgehalte (in de vorm van NatweeO) lost sneller op.
pH
De waterige oplossingen zijn sterk alkalisch.
Chemische eigenschappen
Commercieel voorbereid in SiO-relatiestwee/ NatweeOf in gewicht variërend van 1,5 tot 3,3. Als SiO toeneemttwee in de relatie vermindert de oplosbaarheid in water en alkaliteit.
Het oplossen van vast silicaat in water kan geleiachtige of zeer viskeuze mengsels vormen.
Natriumsilicaatpoeder kan vervloeiend zijn, dat wil zeggen als het een grote hoeveelheid Na bevattweeOf het heeft de neiging om gemakkelijk water uit de omgeving te absorberen.
Als de pH van zijn oplossingen wordt verlaagd door zuur toe te voegen, wordt een gel gevormd.
Andere eigenschappen
Het is niet brandbaar.
Het verkrijgen van
Silicazand SiO wordt gesmolten om natriumsilicaten te verkrijgentwee met natriumcarbonaat NatweeCO3 watervrij in een open oven. De molverhouding van zand tot natriumcarbonaat kan commercieel variëren van 0,5 tot 3,75.

Toepassingen
In zeep en wasmiddelen
Natriumsilicaten behoren tot de eerste verbindingen die werden gebruikt in wasmiddelformuleringen.

Natriumsilicaat sekwestreert calcium Ca-ionentwee+ en magnesium Mgtwee+, het elimineren van wat de hardheid van het water wordt genoemd, dat wil zeggen, het verzachten. Door dit te doen, worden onoplosbare neerslagen gevormd, dus het wordt in kleine hoeveelheden gebruikt.
Door de werking van het natriumsilicaat kan het wasmiddel functioneren zonder dat de genoemde ionen het reinigingsproces beïnvloeden.
In silicagels en katalysatoren
Silicagels worden gewoonlijk bereid door een natriumsilicaatoplossing aan te zuren tot een pH van minder dan 10 of 11. De tijd die nodig is om te geleren varieert..

Silica kan worden bereid door natriumsilicaat te mengen met een sterk mineraal zuur. Natriumsilicaat wordt gebruikt bij de vervaardiging van basen voor katalysatoren, omdat het de bron is van siliciumdioxide SiOtwee.
Als lijm of lijm
Geconcentreerde waterige natriumsilicaatoplossingen worden gebruikt als kleefstoffen en afdichtingsmiddelen. Ze zijn bestand tegen temperaturen tot 1100 ° C.
De belangrijkste toepassingen van natriumsilicaatlijmen zijn in zelfklevend papier, golf- of golfkarton, dozen en kartonnen dozen. Ook voor het verlijmen of samenklonteren van hout of voor het verlijmen van metaal op diverse soorten materialen.

Het wordt gebruikt voor het lijmen van glas, porselein, keramiek, textiel, leer, enz. Voor het verlijmen van glasvezel, optisch glas en slagvaste glascontainers.
Het maakt het mogelijk om vuurvaste cementen te maken om tanks, ketels, ovens en mallen te bouwen voor het gieten van metaal, evenals om waterdichte of zuurbestendige mortels of cementen te maken.
Natriumsilicaten kunnen reageren met siliciumfluoriden om zuurbestendige cementen te produceren met een lage neiging tot krimpen en thermische uitzetting, vergelijkbaar met die van staal..
Ze worden ook gebruikt om cement te maken voor schuurschijven die worden gebruikt voor polijsten..
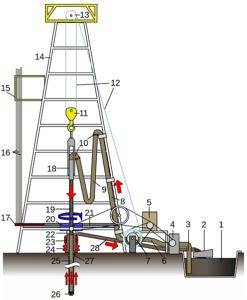
In boorvloeistoffen voor oliebronnen
Natriumsilicaat wordt al vele jaren gebruikt als chemische slurry bij het boren van bepaalde soorten formaties met een zeer hoge permeabiliteit, zoals die welke bestaan uit zand..
Door de hoge doorlaatbaarheid laat het vloeistoffen gemakkelijk door.
Het wordt samen met een verbinding toegevoegd die het silicaat activeert om een polymeer te vormen. Dit polymeer zorgt voor sterkte, stijfheid en vermindert de doorlaatbaarheid in korrelige bodems..
Omdat de grond minder doorlatend is, kan de vloeistof er niet vrij doorheen en wordt op deze manier het verlies van vloeistof tijdens de boorfase van de put vermeden..
In verschillende toepassingen
Natriumsilicaat heeft ook verschillende toepassingen. Hier zijn een paar.
-In dagelijkse verzorgingsproducten is het bijvoorbeeld een bestanddeel van scheerschuim.
-Bij waterbehandeling.
-Bij het bleken van textiel zoals wol.
-Bij het bleken van papierpulp. Om gemalen hout te bleken wordt bijvoorbeeld een mengsel gebruikt dat onder andere waterstofperoxide en natriumsilicaat bevat. Natriumsilicaat wordt gebruikt om metaalionen te sekwestreren, die de afbraak van peroxide versnellen..
-Voor het vervaardigen van brandwerende weefsels. Als brandvertragend middel en als coating voor beschermingsmiddelen.
-In silica pigmenten.
-Door insecten aangetaste maïskorrels opsporen. Een mengsel van natriumsilicaat en water wordt gebruikt waar de aangetaste korrels snel naar de oppervlakte drijven.
-In verzinkt.
-Om metalen te reinigen.
-Bij minerale flotatie wordt het gebruikt als dispergeermiddel voor slib en slib en als conditioner voor het oppervlak van mineralen..
-Om hout te impregneren.
Risico's
Natriumsilicaat is vanwege het hoge alkaligehalte sterk irriterend voor de huid, ogen en slijmvliezen. Bij inslikken kan het giftig zijn en de slijmvliezen irriteren, net als bijtende soda-oplossingen..
Het moet gescheiden worden opgeslagen van sterke zuren, metalen en halogenen zoals fluor, waarmee het heftig reageert.
Referenties
- Ebnesajjad, S. (2015). Kenmerken van zelfklevende materialen. Oplosbare silicaten (kalium- en natriumsilicaat). In Handbook of Adhesives and Surface Preparation. Opgehaald van sciencedirect.com.
- Fink, J.K. (2012). Additieven voor vloeistofverlies. Natriummetasilicaat. In Petroleum Engineer's Guide to Oil Field Chemicals and Fluids (Second Edition). Opgehaald van sciencedirect.com.
- ONS. Nationale bibliotheek van geneeskunde. (2019). Natriumsilicaat. Nationaal centrum voor informatie over biotechnologie. Opgehaald van pubchem.ncbi.nlm.nih.gov.
- Kirk-Othmer. (1984). Encyclopedia of Chemical Technology, 3e ed., John Wiley and Sons.
- Maeda, K. et al. (2007). Van zeolieten tot poreuze MOF-materialen - The 40th Verjaardag van de internationale zeolietconferentie. In Studies in Surface Science and Catalysis. Opgehaald van sciencedirect.com.
- Chopade, S.P. en Nagarajan, K. (2000). Wasmiddelformuleringen: ionenwisseling. In Encyclopedia of Separation Science. Opgehaald van sciencedirect.com.
- .



Niemand heeft nog op dit artikel gereageerd.