
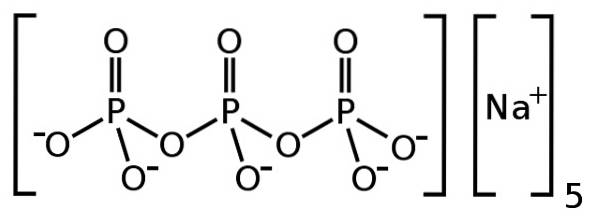
Natriumtripolyfosfaat (Na5P3O10) structuur, eigenschappen, gebruik, impact
De natriumtripolyfosfaat is een anorganische verbinding die wordt gevormd door vijf natrium-Na-ionen+ en een tripolyfosfaation P3OF105-. De chemische formule is Na5P.3OF10. Het tripolyfosfaation bevat drie aan elkaar gebonden fosfaateenheden en is een zogenaamd gecondenseerd fosfaat.
Het tripolyfosfaatanion P3OF105- heeft het vermogen om ionen zoals calcium Ca vast te houdentwee+ en magnesium Mgtwee+, Daarom wordt natriumtripolyfosfaat gebruikt als hulpmiddel in wasmiddelen, zodat ze beter werken in bepaalde soorten water..
Natriumtripolyfosfaat wordt ook gebruikt als bron van fosfor in de voeding van grazende dieren en bij de behandeling van bepaalde aandoeningen van andere diersoorten. Het wordt ook gebruikt om bepaalde bewerkte voedingsmiddelen zoals crèmes, pudding en kaas te verdikken en textuur te geven..
In de agrarische industrie wordt het gebruikt in korrelvormige meststoffen om te voorkomen dat ze aan elkaar kleven en los blijven..
Hoewel er discussies zijn geweest over de milieu-impact van natriumtripolyfosfaat dat aan detergentia wordt toegevoegd, wordt momenteel geschat dat het niet noemenswaardig bijdraagt aan de schade aan het milieu, althans niet via detergentia..
Artikel index
- 1 Chemische structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Dichtheid
- 3.5 Oplosbaarheid
- 3,6 pH
- 3.7 Chemische eigenschappen
- 3.8 Overige eigenschappen
- 4 Verkrijgen
- 5 toepassingen
- 5.1 In wasmiddelen
- 5.2 Voor veterinair gebruik
- 5.3 In de geneeskunde
- 5.4 In de voedingsindustrie
- 5.5 Andere toepassingen
- 6 Milieu-impact
- 7 Risico's
- 8 referenties
Chemische structuur
Natriumtripolyfosfaat is een van de zogenaamde gecondenseerde fosfaten omdat het bestaat uit meerdere aan elkaar gekoppelde fosfaateenheden. In dit geval is het tripolyfosfaation een lineair gecondenseerd fosfaat omdat het een lineaire ketenachtige structuur heeft, met fosfor-zuurstof-fosforbindingen (P-O-P).
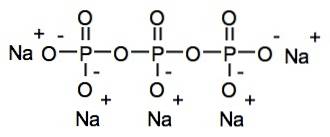
Nomenclatuur
- Natriumtripolyfosfaat
- Natriumtrifosfaat
- Pentanatriumtrifosfaat
- STPP (afkorting van het Engels NatriumtriPolyfosfaat
Eigendommen
Fysieke toestand
Kleurloze tot witte kristallijne vaste stof.
Molecuulgewicht
367,86 g / mol.
Smeltpunt
622 ° C.
Dichtheid
2,52 g / cm3
Oplosbaarheid
Oplosbaar in water: 20 g / 100 ml bij 25 ° C en 86,5 g / 100 ml bij 100 ° C.
pH
Een 1% -oplossing van natriumtripolyfosfaat heeft een pH van 9,7-9,8.
Chemische eigenschappen
Het is een ion-sekwestreermiddel, dat wil zeggen dat het ionen kan vangen en eraan gehecht kan blijven. Vormt complexen met veel metalen.
Als een oplossing van natriumtripolyfosfaat gedurende lange tijd wordt verwarmd, heeft deze de neiging zich om te zetten in natrium-Na-orthofosfaat.3PO4.
Andere eigenschappen
Het is enigszins hygroscopisch. Het vormt stabiele hydraten, dat wil zeggen verbindingen waaraan watermoleculen zijn gehecht (zonder ermee te hebben gereageerd) met de formule Na5P.3OF10.nHtweeOf waar n tussen 1 en 6 kan zijn.
Volgens sommige bronnen heeft een hoeveelheid van 20 mg natriumtripolyfosfaat in één liter water geen invloed op de geur, smaak of pH van genoemd water..
Het verkrijgen van
Natriumtripolyfosfaat wordt bereid door orthofosfaten (zoals mononatriumfosfaat NaHtweePO4 en dinatriumfosfaat NatweeHPO4) bij zeer hoge temperaturen (300-1200 ° C):
NaHtweePO4 + 2 NatweeHPO4 → Na5P.3OF10 + 2 uurtweeOF
Het kan ook worden verkregen door gecontroleerde calcinering (betekent verwarming op een zeer hoge temperatuur) van natrium Na-orthofosfaat.3PO4 met natriumcarbonaat NatweeCO3 en fosforzuur H3PO4.
Toepassingen
In wasmiddelen
Natriumtripolyfosfaat heeft de eigenschap om met bepaalde ionen verbindingen te vormen en deze vast te houden. Het heeft ook dispergerende eigenschappen voor vuildeeltjes en houdt ze in suspensie..
Om deze reden wordt het veel gebruikt in wasmiddelformuleringen om calcium-Ca-ionen op te vangen en te immobiliseren.twee+ en magnesium Mgtwee+ water (zogenaamd hard water) en om het vuil in het water te laten zweven.
De genoemde ionen verstoren de reinigende werking. Door ze op te vangen, voorkomt het tripolyfosfaat dat deze ionen samen met het reinigingsmiddel neerslaan of het vuil op de stof plakken, waardoor de vlek er niet van loslaat..
Natriumtripolyfosfaat zou in dit geval het water "verzachten". Hierdoor wordt het gebruikt in wasmiddelen en automatische vaatwasmiddelen..
Omdat het stabiele hydraten vormt, kunnen de wasmiddelen die het in hun formulering hebben onmiddellijk worden gedroogd door te sproeien (zeer fijne spray) om droge poeders te vormen..

Voor veterinair gebruik
Natriumtripolyfosfaat wordt gebruikt als supplement in vloeibare oplossingen als een bron van fosfor voor vee.

Het wordt ook gebruikt om nierstenen bij katten te voorkomen, waarvoor het oraal aan deze dieren wordt gegeven. Er moet echter op de dosering worden gelet, omdat deze diarree kan veroorzaken..

In de geneeskunde
Natriumtripolyfosfaat is gebruikt bij de bereiding van nanodeeltjes voor het juiste transport en levering van geneesmiddelen voor kankerchemotherapie. Het is ook gebruikt in nanodeeltjes om schimmelinfecties in de longen te behandelen..
In de voedingsindustrie
Gebruikt in zuivelproducten zoals pudding, slagroom, zure room en kaas.

In andere voedingsmiddelen wordt het gebruikt als ionbindend hars, om textuur te geven, als verdikkingsmiddel en als conserveermiddel.
Andere gebruiken
- Als peroxide-stabilisator
- In boorvloeistoffen voor oliebronnen werkt het als een emulgator en dispergeermiddel om de viscositeit van de modder te regelen.
- In de landbouw wordt het gebruikt als antiklontermiddel voor bepaalde meststoffen of landbouwproducten, dit betekent dat het voorkomt dat ze aan elkaar kleven en dat de mest gemakkelijk kan worden verdeeld. Het wordt ook gebruikt in formules voor pesticiden die worden toegepast op groeiende gewassen.

Milieu-impact
Het gebruik van fosfaatproducten is geïdentificeerd als een van de factoren die bijdragen aan de eutrofiëring van water op de planeet.
Eutrofiëring is de overdreven en versnelde groei van algen en waterplantensoorten die leidt tot een sterke afname van de beschikbare zuurstof in het water, wat leidt tot de vernietiging van het aangetaste ecosysteem (dood van de meeste diersoorten erin).

In de jaren tachtig ontstond er controverse dat het gebruik van natriumtripolyfosfaat in wasmiddelen bijdroeg aan eutrofiëring.
Tegenwoordig is bekend dat het beperken van het gebruik van detergentia met natriumtripolyfosfaat zeer weinig zou bijdragen tot het elimineren van eutrofiëring, aangezien fosfaten in grotere hoeveelheden uit andere landbouw- en industriële bronnen komen..
Er zijn zelfs landen die natriumtripolyfosfaat als een milieuvriendelijk bestanddeel van detergentia beschouwen en het gebruik ervan promoten.
Risico's
Natriumtripolyfosfaat is irriterend voor de huid en de ogen. Contact met de ogen kan oogletsel veroorzaken. Langdurig contact met de huid kan dermatitis veroorzaken.
Als het in grote hoeveelheden wordt ingenomen, kan het misselijkheid, braken en diarree veroorzaken, en ook een ernstige vermindering van calciumionen in het bloed veroorzaken. Bij dieren heeft het een afname van calcium in de botten veroorzaakt.
Het wordt als een veilige verbinding beschouwd zolang de productienormen van het product waarin het wordt gebruikt, worden gevolgd..
Referenties
- Liu, Y. en Chen, J. (2014). Fosforcyclus. Referentiemodule in aardesystemen en milieuwetenschappen. Encyclopedia of Ecology (Second Edition). Vol. 4, 2014, blz. 181-191. Opgehaald van sciencedirect.com
- ONS. Nationale bibliotheek van geneeskunde. (2019). Natriumtripolyfosfaat. Nationaal centrum voor informatie over biotechnologie. Opgehaald van pubchem.ncbi.nlm.nih.gov.
- Mukherjee, B. et al. (2017). Pulmonale toediening van biologisch afbreekbare geneesmiddel-nanodragers voor een efficiëntere behandeling van schimmelinfecties in de longen: inzichten op basis van recente bevindingen. In multifunctionele systemen voor gecombineerde levering, biosensing en diagnostiek. Opgehaald van sciencedirect.com.
- Kirk-Othmer. (1991). Encyclopedie van chemische technologie. 4th New York, John Wiley and Sons.
- Burckett St. Laurent, J. et al .; (2007). Wasserijreiniging van textiel. In handboek voor reiniging / decontaminatie van oppervlakken. Opgehaald van sciencedirect.com.
- Budavari, S. (redacteur). (1996). De Merck Index. NJ: Merck en Co., Inc.
- Salahuddin, N. en Galal, A. (2017). Verbetering van de afgifte van geneesmiddelen voor chemotherapie door middel van nanoprecisie-instrumenten. In nanostructuren voor kankertherapie. Opgehaald van sciencedirect.com.


Niemand heeft nog op dit artikel gereageerd.