
Natriumchloriet (NaClO2) structuur, eigenschappen, gebruik, risico's

De Natriumchloriet is een anorganische vaste stof gevormd door een natriumion Na+ en een chlorietion ClOtwee-. De chemische formule is NaClOtwee. Het is een witte kristallijne vaste stof, naast een sterk oxidatiemiddel. Daarom moet er met de grootste zorg mee worden omgegaan..
Het wordt voornamelijk gebruikt als desinfectiemiddel voor vele toepassingen. Elimineert microben op oppervlakken zoals vloeren, muren en laboratoriumapparatuur in ziekenhuizen en klinieken en in hun watersystemen.

Ook in landbouw- en veterinaire faciliteiten, om broedmachines voor pluimvee-eieren te ontsmetten, om infecties van de uiers van melkkoeien te bestrijden, om watersystemen voor dieren te desinfecteren, enz..
In de voedingsindustrie worden de aangezuurde waterige oplossingen gebruikt om vlees, kippen, fruit, groenten en de uitrusting van dergelijke faciliteiten te wassen..
Chloordioxide kan worden bereid met natriumchloriet.twee op de plaats van gebruik, waardoor microben, slechte geuren en smaken uit het water kunnen worden verwijderd, zodat het aangenaam is en zonder problemen kan worden gedronken.
Het wordt ook gebruikt om onder meer papierpulp, plantaardige textielvezels en oliën witter te maken..
NaClOtwee Met vaste stoffen moet voorzichtig worden omgegaan, aangezien bij contact met bepaalde materialen explosies kunnen optreden. Hun oplossingen zijn iets gemakkelijker te hanteren, maar zijn zeer oxiderend en corrosief..
Artikel index
- 1 Structuur
- 2 Nomenclatuur
- 3 Eigenschappen
- 3.1 Fysieke toestand
- 3.2 Molecuulgewicht
- 3.3 Smeltpunt
- 3.4 Dichtheid
- 3.5 Oplosbaarheid
- 3.6 Overige eigenschappen
- 4 Risico's
- 5 Verkrijgen
- 6 toepassingen
- 6.1 Als microbicide en desinfectiemiddel in meerdere toepassingen
- 6.2 Om drinkwater te desinfecteren
- 6.3 Voor verzorging van contactlenzen
- 6.4 In verschillende toepassingen
- 7 referenties
Structuur
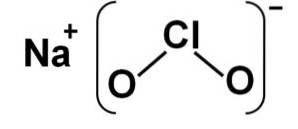
Natriumchloriet bestaat uit een natriumkation Na+ en een chlorietanion ClOtwee- daarom zijn ze verbonden door een ionische binding.
Het chlorietanion heeft één chlooratoom in een oxidatietoestand van +3 en twee zuurstofatomen met valentie -2 elk. Om deze reden heeft het chlorietanion een negatieve lading..
Het heeft ook een hoekvormige structuur.
Nomenclatuur
- Natriumchloriet
- Natriumchloriet
- Chloorzuur natriumzout
Eigendommen
Fysieke toestand
Stevig wit kristallijn.
Molecuulgewicht
90,44 g / mol.
Smeltpunt
Het ontleedt als het smelt tussen 180 en 200 ºC.
Dichtheid
2,468 g / cm3
Oplosbaarheid
Oplosbaar in water: 64 g / 100 g water van 17 ºC. Enigszins oplosbaar in methanol.
Andere eigenschappen
Het is enigszins hygroscopisch.
Het is een sterk oxidatiemiddel. Reageert heftig met brandbare en reducerende stoffen. Reageert heftig met zuren en vormt chloordioxide ClOtwee.
De alkalische oplossingen (betekent in aanwezigheid van bijvoorbeeld NaOH) zijn vrij stabiel, terwijl in een zuur milieu chloorzuur HClO wordt gevormdtwee, die snel afbreekt:
4 HClOtwee → 2 ClOtwee↑ + ClO3- + Cl- + 2 uur+ + H.tweeOF
Risico's
Beide NaClOtwee Vaste, aangezien de waterige oplossingen ervan potentieel gevaarlijk zijn en veel voorzichtigheid en ervaring vereisen tijdens hantering en opslag..
NaClOtwee vaste stof kan exploderen bij contact met organische stoffen, waaronder handschoenen en kleding, materialen voor het tegengaan van morsen zoals zaagsel en katoenafval, evenals oliën en vetten.
De vaste vorm is daarom erg moeilijk te transporteren en het verdient de voorkeur om deze in de vorm van waterige oplossingen te gebruiken..
Deze oplossingen zijn extreem corrosief. Ze moeten bij voorkeur worden bewaard op een pH van meer dan 8, dat wil zeggen een alkalische pH.
NaClOtwee versnelt de verbranding van ontvlambare verbindingen of materialen, tot het punt dat het daarmee explosieve mengsels kan vormen.
Bij verhitting geeft het giftige dampen af van zoutzuur HCl en natriumoxide NatweeO. Langdurige blootstelling aan hitte of vuur kan ontploffen.
Het verkrijgen van
Het wordt bereid te beginnen met de chemische of elektrochemische reductie van natriumchloraat NaClO3, in aanwezigheid van zoutzuur HCl om chloordioxide ClO te producerentwee.
De laatste wordt omgezet met waterstofperoxide HtweeOFtwee in waterige oplossing van natriumhydroxide NaOH en een oplossing van natriumchloriet NaClO wordt verkregentwee, die verdampt en de vaste stof kristalliseert.
Het kan ook worden verkregen door chloordioxidegas ClO te leidentwee door een NaOH-oplossing.
2 ClOtwee + 2 NaOH → NaClOtwee + NaClO3 + H.tweeOF
Toepassingen
Als microbicide en desinfectiemiddel in meerdere toepassingen
Het is een ingrediënt in tal van producten die worden gebruikt om bacteriën, schimmels en algenslib te bestrijden. De producten die het voor dit doel bevatten, worden gebruikt in de landbouw, handel, industrie en woningen of woningen..
Dient als ontsmettingsmiddel voor vele soorten materialen en oppervlakken.
In de landbouw, pluimvee en soortgelijke industrieën worden harde oppervlakken, apparatuur, faciliteiten voor het uitbroeden van vogeleieren, kassen voor schimmels zoals paddenstoelen en koelwater- en watersystemen voor pluimveestallen gedesinfecteerd..
Het heeft veterinair gebruik als een actueel ontsmettingsmiddel bij de bestrijding van mastitis bij melkvee, om de tepels van het dier onder te dompelen. Mastitis is een infectie van de uiers van koeien.

Het wordt ook gebruikt in natuurlijke onderzoeksinstellingen om laboratoria te ontsmetten.
Commercieel, industrieel en medisch gebruik omvat het desinfecteren van ventilatiesystemen, harde oppervlakken (zoals vloeren, muren, laboratoriumapparatuur) en watersystemen..
In zorginstellingen zoals klinieken en ziekenhuizen wordt het gebruikt om kamers, gangen, isolatieruimtes te ontsmetten en voor de sterilisatie van materialen.
Het is ook nuttig voor het ontsmetten in instellingen waar mensen gezondheidsbehandelingen ondergaan met water of spa.
In de voedingsindustrie wordt het gebruikt als ontsmettingsmiddel om voedsel te conserveren.
Het wordt gebruikt in de vorm van aangezuurd natriumchloriet. Dit wordt geproduceerd door zuur van voedingskwaliteit (bijvoorbeeld citroenzuur, fosforzuur, appelzuur of natriumzuursulfaat) toe te voegen aan een waterige oplossing van natriumchloriet..
Aangezuurd natriumchloriet heeft antimicrobiële eigenschappen en wordt gebruikt als spray of was- of weekoplossing voor kip, vlees, groenten, fruit en zeevruchten. Ook in water om kip of gevogelte in te vriezen.
In woningen kunnen harde oppervlakken, zoals vloeren en badkamers, verwarmings- of airconditioningsystemen en circulatiesystemen voor zwembaden, worden gedesinfecteerd..


Het wordt ook verkocht in kleine sachets, samen met andere verbindingen om gas af te geven en geuren in huizen te beheersen..
Om drinkwater te desinfecteren
Het wordt gebruikt bij de zuivering van drinkwater, werkt als een oxidatiemiddel en verbetert de smaak en geur van drinkwater.
Natriumchloriet wordt veel gebruikt als precursor voor het genereren van chloordioxide ClOtwee gebruikt om drinkwater voor menselijke consumptie te behandelen, dat wil zeggen om micro-organismen, geuren en onaangename smaken te elimineren en kan worden gedronken.
Om de ClO te genererentwee HCl kan worden gebruikt:
5 NaClOtwee + 4 HCl → 4 ClOtwee↑ + 5 NaCl + 2 HtweeOF
De ClOtwee het is een antimicrobieel middel met een sterk oxiderende werking en een breed spectrum. Dat wil zeggen, het werkt tegen een groot aantal micro-organismen.
Micro-organismen worden geïnactiveerd omdat ClOtwee het interfereert met belangrijke enzymen hiervan en met de eiwitten van de celmembranen. Het heeft ook het voordeel dat het geen organochloorverbindingen produceert, die giftig zijn..
Er zijn natriumchloriettabletten te koop gemengd met andere verbindingen die oplossen in water en direct ClO producerentwee op een gecontroleerde manier, waardoor het water wordt gedesinfecteerd.

Het belangrijkste probleem bij het behandelen van water om smaken en geuren te verwijderen met ClOtwee is dat tijdens de behandeling giftige chloriet- en chloraatzouten kunnen worden gevormd.
Voor het verzorgen van contactlenzen
NaClOtwee het is een onderdeel van de oplossingen die dienen om contactlenzen te desinfecteren.
Er wordt een combinatie van NaClO gebruikttwee en sporen (zeer kleine hoeveelheden) waterstofperoxide HtweeOFtwee.
De HtweeOFtwee stabiliseert ClOtwee dat wordt gevormd en de combinatie van beide is zeer effectief tegen bacteriën, schimmels en gisten. De resulterende producten zijn natriumchloride NaCl, water en zuurstof, die onschadelijk zijn, wat betekent dat ze niet schadelijk zijn voor het oog.
Wanneer de lenzen uit de oplossing worden gehaald, wordt de NaClOtwee Residu ontleedt snel tot NaCl en Otwee. Overgebleven peroxide irriteert het oog niet. Daarom zijn deze oplossingen erg veilig.

In verschillende toepassingen
Natriumchloriet wordt gebruikt voor de bereiding van chloordioxide ClOtwee voor onmiddellijk gebruik in een groot aantal toepassingen, waarvan er enkele in voorgaande paragrafen zijn besproken.
Het wordt gebruikt om houtpulp, textiel zoals katoen, plantaardige vezels, eetbare en niet-eetbare oliën, vetten, vernissen, lakken en wassen wit te maken.
Het is een bestanddeel van oogdruppels en sommige oplossingen voor mondwater..
Het wordt gebruikt in de leerverwerkende industrie en in middelen voor het galvaniseren van metalen (metaalcoating).
Referenties
- Williams, L. et al .; (2019). Microbiologie, verzorging en onderhoud van lenzen. In contactlenzen (zesde editie). Opgehaald van sciencedirect.com.
- ONS. Nationale bibliotheek van geneeskunde. (2019). Natriumchloriet. Opgehaald van pubchem.ncbi.nlm.nih.gov.
- Gray, N.F. (2014). Chloordioxide. Procestechnologie. In Microbiology of Waterborne Diseases (Second Edition). Opgehaald van sciencedirect.com.
- McKeen, L. (2012). Inleiding tot voedselbestraling en medische sterilisatie. Chloordioxide. In het effect van sterilisatie op plastic en elastomeren (derde editie). Opgehaald van sciencedirect.com.
- Ortenberg, E. en Telsch, B. (2003). Smaak- en geurproblemen in drinkwater. In Handbook of Water and Wastewater Microbiology. Opgehaald van sciencedirect.com.
- Karsa, D.R. (2007). Biociden. Chloordioxide. In handboek voor reiniging / decontaminatie van oppervlakken. Opgehaald van sciencedirect.com.
- Cotton, F. Albert en Wilkinson, Geoffrey. (1980). Geavanceerde anorganische chemie. Vierde druk. John Wiley & Sons.
- Ullmann's Encyclopedia of Industrial Chemistry. (1990). Vijfde editie. VCH Verlagsgesellschaft mbH.



Niemand heeft nog op dit artikel gereageerd.